Isopreno
| Isopreno Alerta sobre risco à saúde | |
|---|---|

|

|
| Nome IUPAC | 2-metilbuta-1,3-dieno |
| Outros nomes | isopreno |
| Identificadores | |
| Número CAS | |
| PubChem | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C5H8 |
| Massa molar | 68,12 g/mol |
| Densidade | 0,68 g·cm-3 [1] |
| Ponto de fusão |
-146 °C[1] |
| Ponto de ebulição |
34 °C[1] |
| Solubilidade em água | 0,7 g·l-1 a 20 °C [1] |
| Solubilidade | solúvel em etanol e éter dietílico[2] |
| Pressão de vapor | 604 hPa (20 °C)[1] |
| Riscos associados | |
| Frases R | R45, R68, R12, R52/53 |
| Frases S | S53, S45, S61 |
| Compostos relacionados | |
| Alcadienos relacionados | Butadieno |
| Compostos relacionados | Metilbutano (saturado) Poli-isopreno (borracha natural) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
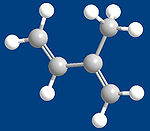
O isopreno é um composto orgânico tóxico que é utilizado como monômero para a fabricação do poliisopreno, a borracha, através de uma reação de polimerização e também é usado como catalisador para a obtenção de outros compostos químicos.
São sinônimos de isopreno: beta-metildivinil; 2-metil 1,3-butadieno. Sua fórmula química é C5H8.
Nas CNTP, o composto é líquido, sem coloração, possui odor suave, é inflamável, é menos denso que a água e produz vapor irritante.
O isopreno, de nome científico 2-metil-1,3-butadieno, consiste num hidrocarboneto alifático, incolor, volátil, com 5 átomos de carbono e duas ligações duplas conjugadas com a fórmula CH2 = CH-C(CH3) = CH2. O isopreno é a unidade estrutural de grande variedade de substâncias naturais (terpenos), como por exemplo a borracha natural, óleos essenciais, carotenoides e esteroides. Por polimerização do isopreno obtêm-se alguns tipos de borracha sintética. É possível a obtenção direta do isopreno a partir do etileno e do propileno provenientes dos gases de cracking. O isopreno nunca foi isolado como produto natural. Sabe-se atualmente que o verdadeiro precursor dos terpenos é o ácido mevalónico, isolado em 1956. A regra do isopreno estabelece que todos os terpenos podem dividir-se formalmente em unidades de isopreno. As raras exceções a esta regra correspondem a compostos que se formam por perda ou por transposição de algum átomo de carbono.
