Pseudo-obstrução intestinal
| Pseudo-obstrução intestinal | |
|---|---|
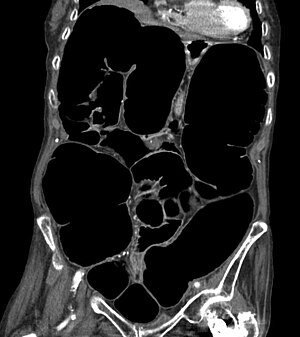
| Paciente idosa acometida pela variante aguda da enfermidade, auferindo cólon nítida e anarquicamente alargado | |
| Sinônimos | Pseudo-oclusão intestinal, síndrome de pseudo-obstrução intestinal, síndrome pseudo-obstrutiva, pseudo-obstrução do intestino[1][2] |
| Especialidade | Gastroenterologia |
| Sintomas | Distensão abdominal, dor abdominal, náuseas, vômitos, obstipação crônica, diarreia, perda de peso[3] |
| Complicações | Perfuração do ceco, perfuração do fígado, infecções |
| Tipos | Crônico, agudo |
| Causas | Trauma, infecção, insuficiência, lesão à coluna espinal, desordens neurológicas |
| Fatores de risco | Abuso de álcool, síndrome de hipoperistaltismo intestinal, cirurgia prévia, hipotireoidismo, desequilíbrio eletrolítico, desordens respiratórias, constipação crônica, síndrome de Guillain-Barré, amiloidose, cancro do estômago, esclerose sistêmica, megacisterna do megacolon, mieloma múltiplo, lúpus eritematoso sistêmico[4] |
| Tratamento | Medicações procinéticas,[5] suporte nutricional[6] (nutrição enteral ou parenteral),[7][8][9] descompressão colonoscópica gastrointestinal[9][10] |
| Medicação | Anti-depressivos tricíclicos, anticolinérgicos, antieméticos, antibióticos (para condições adjacentes), narcóticos[2] |
| Prognóstico | Sobrevivência a dez anos desde o início do tratamento - variante crônica: ~ 60% (EUA)[11] |
| Frequência | 1 caso a cada 100.000 habitantes (homens), 0,8 casos a cada 100.000 habitantes (mulheres) - variante crônica[12] |
| Classificação e recursos externos | |
| OMIM | 155310 |
| DiseasesDB | 10868 |
| MedlinePlus | 000253 |
| eMedicine | 2162306 |
| MeSH | D007418 |
Pseudo-obstrução intestinal é uma síndrome clínica arrazoada como severo comprometimento na competência dos intestinos em fomentar alimentos para ulterior eliminação, através da defecação. É caracterizada por sinais e sintomas de obstrução intestinal, porém, à exegese examinatória, quaisquer lesões ao lúmen intestinal são nulas.[13] Manifestações clínicas podem concernir a dor abdominal, náuseas, distensão conspícua, vômitos, disfagia, obstipação intestinal e/ou diarreia, dependendo da porção do trato gastrointestinal engajada.[14] A condição pode incoar-se a qualquer idade, alternando dentre circunstâncias primárias (idiopática ou herdada), ou promovida por outra desordem (secundária).[15]
Pode atinar aos padrões crônico[16] ou agudo.[17]
Causas[editar | editar código-fonte]
Na pseudo-obstrução intestinal primária, que simboliza a maioria de casos crônicos, a condição pode ser desencadeada por lesões ao músculo liso (miopático) ou sistema nervoso (neuropático) do trato gastrointestinal.[18]
Em alguns casos, parece haver associações genéticas.[19] Um reporte já foi relacionado com DXYS154.[20]
Escalonamentos secundários da variante crônica podem engendrar-se com albergue em condições propínquas, incluindo doença de Kawasaki,[21] doença de Parkinson, doença de Chagas, doença de Hirschsprung, hipoganglionose intestinal, doenças vasculares do colágeno, doença mitocondrial, distúrbios endócrinos, e uso de certos medicamentos.[18]
Tratamento[editar | editar código-fonte]
A vertente crônica é gerenciada através do tratamento da condição subjacente.
Não há cura para a pseudo-oclusão intestinal crônica. Todavia, com cuidados nutricionais, reposição de fluídos e métodos para alívio da dor, é possível, ainda que intermitentemente, regularizar os casos. Drogas que acentuam a força propulsiva dos intestinos já foram tentadas, bem como tipos alternativos de cirurgias.[22]
Tratamento médico[editar | editar código-fonte]
Prucaloprida,[23][24] piridostigmina,[15] metoclopramida, cisaprida e eritromicina podem ser empregadas, apesar de não abonar peremptoriedade excelente. Em tais oportunidades, o tratamento priorizará a manutenção de eventuais complicações. Linaclotide é um novo medicamento, obtendo aval de uso pela Food and Drug Administration em 2012. Verificações sugerem que seu potencial é auspicioso para obstruções não maciças, e, ainda, a gastroparesia e inércia colônica.[25]
Paralisia intestinal, que pode guiar a um crescimento bacterial fervoroso, diarreia ou má absorção, é manipulada com antibióticos.
Deficiências nutricionais são administradas pelo encorajamento ao evitamento de alimentos ricos em gordura e fibra a pacientes arremetidos, pois tais materiais, trivialmente, são mais difíceis de serem digeridos, enrijecendo a distensão e o desconforto. Adicionalmente, é usual que recomende-se de cinco a seis miúdas refeições aos flagelados, concentrando-se em líquidos e comida leve. Reduzir a ingestão de álcoois de açúcar mal absorvidos pode ser benéfico; portanto, é consueta a preferência por dietas restritivas. Se alterações voluntárias na dieta são improdutivas na acepção a nutrientes cruciais, havendo cursiva perda de peso, é necessária a implantação de nutrição enteral. Alguns pacientes, ulteriormente, são obrigados a incorporar o estádio parenteral.[18]
Uma absoluta nutrição parenteral (NPT) é uma forma de tratamento nutricional de longo prazo, necessária para pacientes com pseudo-obstrução grave. Após um período sem acuramento da função ou motilidade intestinal, será tomada a decisão de iniciar a NPT, ocorrendo, então, procedimentos cirúrgicos para elencar um cateter intravenoso mais permanente e de longo prazo, a fim de controlar a NPT. Os tipos de cateteres a ser colocados podem aludir a uma linha central ou de PICC, que incluem mediport, Broviac ou Hickman, dependendo da duração de uso da NPT estipulada por médicos. Pacientes taxados como dependentes da NPT precisarão de exames constantes para monitorar o funcionamento correto do cateter, aferir as enzimas hepáticas, e procurar sinais de infecções no sangue, como bloqueio do cateter, dano hepático e infecções do cateter, ressaltadas complicações associadas com uso prolongado de NPT, podendo culminar em sepse e/ou cirurgias adicionais, se não exercidos aceitavelmente. As alimentações nutricionais da NPT são fornecidas dentro de um período de várias horas a infusões diárias, coordenando-se através de uma mistura de todas as vitaminas, minerais e calorias semelhantes ao que se obteria por via oral diariamente, bem como quaisquer outras necessidades nutricionais específicas que o paciente venha a postular no momento. O formato da NPT é ordinariamente modificado, dependendo da perda/ganho de peso e dos resultados de trabalho com sangue, sendo especialmente formulado para atender às necessidades de cada paciente.[26]

Cannabis tem sido rotulada à prevenção de náuseas e vômitos. Tal fim tem conduzido análises intensivas no que permeia a ação dos receptores do canabidiol, bem como de si. Com o advento do sistema endocanabinóide, foram descobertas novas maneiras de conter náuseas e vômitos que envolvem a produção de canabinóides endógenos agindo centralmente.[27] A cannabis vegetal é usada em clínicas há séculos, sendo conhecida pela capacidade benéfica em várias doenças gastrointestinais, como êmese, diarreia, doença inflamatória intestinal e dor intestinal. Além disso, a modulação do sistema canabinóide endógeno no tubo digestivo pode fornecer um alvo terapêutico pertinente para distúrbios gastrointestinais.[28] Enquanto certas desordens do tubo digestivo podem ser brecadas por dietas e drogas farmacêuticas, outras são frivolamente atreladas a tratamentos convencionais. Os sintomas de distúrbios gastrointestinais, banalmente, incluem cãibras, dor abdominal, inflamação do revestimento do intestino grosso e/ou delgado, diarreia crônica, sangramento retal e perda de peso. Os pacientes com esses distúrbios costumam relatar uso de maconha a âmbito terapêutico.[29]
Num estudo de 2012 com animais, evidenciou-se que o canabicromeno normaliza a hipermotilidade gastrointestinal sem reduzir o tempo de trânsito. Este ratificou que o resultado é de massivo interesse clínico, pois os únicos medicamentos disponíveis para dismotilidade intestinal estão frequentemente associados à constipação.[30]
Procedimentos[editar | editar código-fonte]
Descompressão intestinal pela colocação de tubo em um pequeno estoma também pode ser usada para reduzir a distensão e a pressão dentro do intestino. O estoma é viável como uma gastrostomia, jejunostomia, ileostomia ou cecostomia, podendo, paralelamente, ser usado para alimentar, no caso da gastrostomia e jejunostomia, ou lavar o intestino.
A colostomia ou ileostomia pode ignorar as partes afetadas se elas estiverem distais para (após) o estoma. Por exemplo, se o cólon maior for afetado, a ileostomia pode ser útil. Quaisquer ostomias de tais gêneros são vulgarmente colocadas no umbigo ou abaixo do umbigo do paciente.[26]
A remoção total do cólon, denominada colectomia, ou ressecção das partes afetadas do cólon, pode ser fundamental se a área localizada competir à dismotilidade.
Gástricos e colônicos marcapassos foram tentados. São tiras colocadas ao longo do cólon ou do estômago que criam uma descarga elétrica destinada a incitar a contração muscular de maneira controlada. Uma solução potencial, embora radical, é o transplante de múltiplos órgãos. Uma operação documentada envolveu o transplante de pâncreas, estômago, duodeno, intestino delgado e fígado, e foi realizada pelo médico Kareem Mohamed Abu-Elmagd, em Gretchen Miller.[31]
Referências
- ↑ «Intestinal pseudo-obstruction». U.S. National Library of Medicine. 2019 [2017]
- ↑ a b «Chronic Intestinal Pseudo-Obstruction». National Organization for Rare Disorders. Consultado em 31 de outubro de 2019
- ↑ «What is chronic intestinal pseudo-obstruction?». Children's Wisconsin. Consultado em 31 de outubro de 2019
- ↑ Cagir, Burt; Napolitano, Lena; Dunne, James; Remy, Prospere (18 de julho de 2018). Geibel, John, ed. «Intestinal Pseudo-Obstruction». WebMD LLC. Consultado em 31 de outubro de 2019
- ↑ Lemos, Carlos; Popoutchi, Pedro; Parra, Rogério; Féres, Omar; Rocha, José (Novembro de 2007). «Chronic idiopathic intestinal pseudo-obstruction treated with jejunostomy: case report and literature review» Pseudo-obstrução intestinal crônica idiopática tratada por jejunostomia: relato de caso e revisão da literatura. São Paulo. Sao Paulo Medical Journal. 125 (6). ISSN 1516-3180. Consultado em 31 de outubro de 2019
- ↑ «Intestinal psuedo-obstruction». International Foundation for Gastrointestinal Disorders. 2 de outubro de 2019. Consultado em 31 de outubro de 2019
- ↑ «Intestinal pseudo-obstruction». International Foundation for Gastrointestinal Disorders. 1 de outubro de 2015. Consultado em 31 de outubro de 2019
- ↑ Lemos, Carlos; Popoutchi, Pedro; Parra, Rogério; Féres, Omar; Rocha, José; op.cit.
- ↑ a b «Pseudo-obstrução intestinal aguda: recomendações para diagnóstico e tratamento». PEBMED. 3 de maio de 2018. Consultado em 31 de outubro de 2019
- ↑ Lemos, Carlos et al
- ↑ Lu, Wei; Xiao, Yongtao; Huang, Jianhu; Lu, Lina; Yiqing, Tao; Yan, Weihui; Cao, Yi; Cai, Wei (7 de setembro de 2018). Kok, Victor, ed. «Causes and prognosis of chronic intestinal pseudo-obstruction in 48 subjects» [Causas e prognóstico da pesudo-obstrução intestinal crônica em 48 pacientes]. Baltimore. Medicine (Baltimore). 97 (36). PMC 6133590
 . PMID 30200110. Consultado em 31 de outubro de 2019
. PMID 30200110. Consultado em 31 de outubro de 2019
- ↑ Arce, Edith; Landskron, Glauben; Hirsch, Sandra; Defilippi, Carlos; Madrid, Ana (Abril de 2017). «Chronic Intestinal Pseudo-obstruction: Clinical and Manometric Characteristics in the Chilean Population» [Pseudo-Obstrução Intestinal Crônica: Características Clínicas e Manométricas na População Chilena]. J Neurogastroenterol Motil. 23 (2). PMC 5383122
 . PMID 27669829. Consultado em 31 de outubro de 2019
. PMID 27669829. Consultado em 31 de outubro de 2019
- ↑ Stanghellini V, Cogliandro RF, De Giorgio R, et al. (maio de 2005). «Natural history of chronic idiopathic intestinal pseudo-obstruction in adults: a single center study». Clinical Gastroenterology and Hepatology. 3 (5): 449–58. PMID 15880314. doi:10.1016/S1542-3565(04)00675-5
- ↑ De Giorgio R, Sarnelli G, Corinaldesi R, Stanghellini V (novembro de 2004). «Advances in our understanding of the pathology of chronic intestinal pseudo-obstruction». Gut. 53 (11): 1549–52. PMC 1774265
 . PMID 15479666. doi:10.1136/gut.2004.043968
. PMID 15479666. doi:10.1136/gut.2004.043968
- ↑ a b Antonucci A, Fronzoni L, Cogliandro L, et al. (maio de 2008). «Chronic intestinal pseudo-obstruction». World Journal of Gastroenterology. 14 (19): 2953–61. PMC 2712158
 . PMID 18494042. doi:10.3748/wjg.14.2953
. PMID 18494042. doi:10.3748/wjg.14.2953
- ↑ Sutton DH, Harrell SP, Wo JM (fevereiro de 2006). «Diagnosis and management of adult patients with chronic intestinal pseudoobstruction». Nutrition in Clinical Practice. 21 (1): 16–22. PMID 16439766. doi:10.1177/011542650602100116
- ↑ Saunders MD (outubro de 2004). «Acute colonic pseudoobstruction». Current Gastroenterology Reports. 6 (5): 410–6. PMID 15341719. doi:10.1007/s11894-004-0059-5
- ↑ a b c Gabbard SL, Lacy BE (junho de 2013). «Chronic intestinal pseudo-obstruction». Nutrition in Clinical Practice. 28 (3): 307–16. PMID 23612903. doi:10.1177/0884533613485904
- ↑ Guzé CD, Hyman PE, Payne VJ (janeiro de 1999). «Family studies of infantile visceral myopathy: a congenital myopathic pseudo-obstruction syndrome». American Journal of Medical Genetics. 82 (2): 114–22. PMID 9934973. doi:10.1002/(SICI)1096-8628(19990115)82:2<114::AID-AJMG3>3.0.CO;2-H
- ↑ Auricchio A, Brancolini V, Casari G, et al. (abril de 1996). «The locus for a novel syndromic form of neuronal intestinal pseudoobstruction maps to Xq28». American Journal of Human Genetics. 58 (4): 743–8. PMC 1914695
 . PMID 8644737
. PMID 8644737
- ↑ Akikusa JD, Laxer RM, Friedman JN (maio de 2004). «Intestinal pseudoobstruction in Kawasaki disease». Pediatrics. 113 (5): e504–6. PMID 15121996. doi:10.1542/peds.113.5.e504
- ↑ Kamm, Michael (2000). «Intestinal pseudo-obstruction». 47 (84). Consultado em 2 de novembro de 2019
- ↑ Briejer MR, Prins NH, Schuurkes JA (outubro de 2001). «Effects of the enterokinetic prucalopride (R093877) on colonic motility in fasted dogs». Neurogastroenterology and Motility. 13 (5): 465–72. PMID 11696108. doi:10.1046/j.1365-2982.2001.00280.x
- ↑ Oustamanolakis P, Tack J (fevereiro de 2012). «Prucalopride for chronic intestinal pseudo-obstruction». Alimentary Pharmacology & Therapeutics. 35 (3): 398–9. PMID 22221087. doi:10.1111/j.1365-2036.2011.04947.x
- ↑ "Textbook of Gastroenterology" by Tadataka Yamada, Editor John Wiley & Sons, 2011 ISBN 144435941X, 9781444359411[falta página]
- ↑ a b
AAHeneyke S, Smith VV, Spitz L, Milla PJ (julho de 1999). «Chronic intestinal pseudo-obstruction: treatment and long term follow up of 44 patients». Archives of Disease in Childhood. 81 (1): 21–7. PMC 1717974
 . PMID 10373127. doi:10.1136/adc.81.1.21
. PMID 10373127. doi:10.1136/adc.81.1.21
- ↑ Sharkey KA, Darmani NA, Parker LA (janeiro de 2014). «Regulation of nausea and vomiting by cannabinoids and the endocannabinoid system». European Journal of Pharmacology. 722: 134–46. PMC 3883513
 . PMID 24184696. doi:10.1016/j.ejphar.2013.09.068
. PMID 24184696. doi:10.1016/j.ejphar.2013.09.068
- ↑ Lin XH, Wang YQ, Wang HC, Ren XQ, Li YY (agosto de 2013). «Role of endogenous cannabinoid system in the gut» (PDF). Sheng Li Xue Bao. 65 (4): 451–60. PMID 23963077
- ↑ Gastrointestinal Disorders.
- ↑ Izzo AA, Capasso R, Aviello G, Borrelli F, Romano B, Piscitelli F, Gallo L, Capasso F, Orlando P, Di Marzo V (17 de maio de 2012). «Inhibitory effect of cannabichromene, a major non-psychotropic cannabinoid extracted from Cannabis sativa, on inflammation-induced hypermotility in mice». British Journal of Pharmacology. 166 (4): 1444–60. PMC 3417459
 . PMID 22300105. doi:10.1111/j.1476-5381.2012.01879.x
. PMID 22300105. doi:10.1111/j.1476-5381.2012.01879.x
- ↑ Discovery Channel - Multiorgan transplant