Tramiprosato
| Tramiprosato (DCI]) Alerta sobre risco à saúde[1] | |
|---|---|

| |
| |
| Outros nomes | Homotaurina; Alzhemed; 3-APS |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| KEGG | |
| SMILES |
|
| InChI | 1/C3H9NO3S/c4-2-1-3-8(5,6)7/h1-4H2,(H,5,6,7)
|
| Propriedades | |
| Fórmula química | C3H9NO3S |
| Massa molar | 139.16 g mol-1 |
| Ponto de fusão |
293 °C, 566 K, 559 °F |
| Riscos associados | |
| Frases R | R36/37/38 |
| Frases S | S26 S36 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
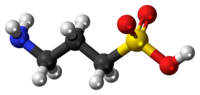
Tramiprosato (DCI; também conhecido como homotaurina, ácido 3-amino-1-propanossulfônico ou 3-APS) é um aminoácido encontrado naturalmente em algas marinhas.[2] É análogo à taurina, mas sua estrutura química possui carbono extra. Tem atividade GABAérgica, aparentemente por mimetizar GABA, ao qual se assemelha.[3]
A homotaurina foi estudada em um ensaio clínico de Fase III como um tratamento em potencial para a doença de Alzheimer, mas não mostrou eficácia.[4] Um estudo sobre deficiência cognitiva feito em 2018 mostrou benefícios positivos limitados.[5]
Propriedades bioquímicas[editar | editar código-fonte]
Em estudos pré-clínicos, descobriu-se que se o tramiprosato se ligava à beta amiloide solúvel e inibia a formação de agregados neurotóxicos.[4][6] A homotaurina também mostrou exercer atividade anticonvulsivante, redução tônus e atividade hipotérmica.[7]
Ao mesmo tempo, o traiprosato é um antagonista e agonista do GABA.[3][7] Estudos in vitro descobriram que a homotaurina é um agonista parcial do receptor GABAA,[8] bem como um agonista parcial do receptor GABA B com baixa eficácia, tornando-se um antagonista e deslocando os agonistas completos GABA e baclofeno neste receptor.[9] Em estudo com ratos, a traiprosato reverteu a catatonia induzida pelo baclofeno (agonista típico do GABAB),[10] bem como demonstrou exercer ação analgésica por meio do receptor GABAB.[11][12]
Um estudo em ratos mostrou que a homotaurina suprimiu a liberação de dopamina estimulada pelo etanol, bem como a ingestão e preferência de etanol em ratos de uma forma semelhante ao N-acetil-derivado da homotaurina, o acamprosato.[13] Nos Estados Unidos, o acamprosato foi aprovado pela FDA em 2004 para tratamento de alcoolismo.[3]
Referências
- ↑ «Homotaurine». Sigma-Aldrich
- ↑ Martorana, A.; Di Lorenzo, F.; Manenti, G.; Semprini, R.; Koch, G. (2014). «Homotaurine Induces Measurable Changes of Short Latency Afferent Inhibition in a Group of Mild Cognitive Impairment Individuals». Frontiers in Aging Neuroscience. 6. 254 páginas. PMC 4172065
 . PMID 25295005. doi:10.3389/fnagi.2014.00254
. PMID 25295005. doi:10.3389/fnagi.2014.00254
- ↑ a b c Lednicer, Daniel (2008). The Organic Chemistry of Drug Synthesis 7th ed. Hoboken: John Wiley & Sons. ISBN 978-0-470-18066-2
- ↑ a b Caltagirone, C.; Ferrannini, L.; Marchionni, N.; Nappi, G.; Scapagnini, G.; Trabucchi, M. (2012). «The potential protective effect of tramiprosate (homotaurine) against Alzheimer's disease: A review». Aging Clinical and Experimental Research. 24: 580–7. PMID 22961121. doi:10.3275/8585
- ↑ http://www.jgerontology-geriatrics.com/wp-content/uploads/2018/03/03_Martorana-1.pdf
- ↑ Aisen, Paul; Gauthier, Serge; Vellas, Bruno; Briand, Richard; Saumier, Daniel; Laurin, Julie; Garceau, Denis (2007). «Alzhemed: A Potential Treatment for Alzheimers Disease». Current Alzheimer Research. 4: 473–478. PMID 17908052. doi:10.2174/156720507781788882
- ↑ a b Oja SS and Kontro P. (2013). Lajtha ANS, ed. Chapter 18: Taurine. [S.l.]: Springer Science & Business Media. ISBN 9781468443677
- ↑ Reyes-Haro, Daniel; Cabrera-Ruíz, Elizabeth; Estrada-Mondragón, Argel; Miledi, Ricardo; Martínez-Torres, Ataúlfo (2014). «Modulation of GABA-A receptors of astrocytes and STC-1 cells by taurine structural analogs». Amino Acids. 46: 2587–2593. PMID 25119985. doi:10.1007/s00726-014-1813-0
- ↑ Giotti, A.; Luzzi, S.; Spagnesi, S.; Zilletti, Lucilla (1983). «Homotaurine: A GABAB antagonist in guinea-pig ileum». British Journal of Pharmacology. 79: 855–862. PMC 2044932
 . PMID 6652358. doi:10.1111/j.1476-5381.1983.tb10529.x
. PMID 6652358. doi:10.1111/j.1476-5381.1983.tb10529.x
- ↑ Mehta, A.; Ticku, M. (1987). «Baclofen induces catatonia in rats». Neuropharmacology. 26: 1419–1423. PMID 2823166. doi:10.1016/0028-3908(87)90108-0
- ↑ Serrano, Maria Isabel; Serrano, Jose S.; Asadi, Ikhlas; Fernandez, Ana; Serrano-Martino, Maria Carmen (2001). «Role of K+-channels in homotaurine-induced analgesia». Fundamental and Clinical Pharmacology. 15: 167–173. PMID 11468027. doi:10.1046/j.1472-8206.2001.00026.x
- ↑ Serrano, M.Isabel; Serrano, Jose S.; Fernández, Ana; Asadi, Ihklas; Serrano-Martino, M.Carmen (1998). «GABAB Receptors and Opioid Mechanisms Involved in Homotaurine-Induced Analgesia». General Pharmacology: The Vascular System. 30: 411–415. PMID 9510095. doi:10.1016/s0306-3623(97)00279-6
- ↑ Olive, M.Foster; Nannini, Michelle A.; Ou, Christine J.; Koenig, Heather N.; Hodge, Clyde W. (2002). «Effects of acute acamprosate and homotaurine on ethanol intake and ethanol-stimulated mesolimbic dopamine release». European Journal of Pharmacology. 437: 55–61. PMID 11864639. doi:10.1016/s0014-2999(02)01272-4
