Estireno
| Estireno Alerta sobre risco à saúde | |
|---|---|

|

|
| Nome IUPAC | Estireno |
| Outros nomes | Vinilbenzeno; Estirol; etenilbenzeno; Fenetileno; Fenileteno; diarex HF 77; styrolene; styropol |
| Identificadores | |
| Número CAS | |
| Número EINECS | |
| Número RTECS | WL3675000 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C8H8 |
| Massa molar | 104,15 g/mol |
| Aparência | Líquido oleoso incolor |
| Densidade | 0,909 g/cm³ |
| Ponto de fusão |
-30 °C (243,15 K) |
| Ponto de ebulição |
145 °C (418,15 K) |
| Solubilidade em água | < 1% |
| Índice de refracção (nD) | 1,5469 |
| Viscosidade | 0,762 cP at 68 °F |
| Estrutura | |
| Momento dipolar | 0,13 D |
| Riscos associados | |
| MSDS | MSDS |
| Principais riscos associados |
Nocivo(Xn) Inflamável(F) |
| Frases R/S | R10 R20 R36/38 S2 S23 |
| Ponto de fulgor | 31 °C |
| Compostos relacionados | |
| hidrocarbonetos aromáticos relacionados | Etil benzeno Alfa-metil-estireno (1-metil-1-fenil-eteno) Divinilbenzeno |
| Compostos relacionados | Poliestireno 3,4-Di-hidroxiestireno |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
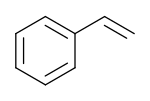
O estireno é um hidrocarboneto aromático não saturado. À temperatura ambiente é líquido oleoso incolor, que polimeriza com facilidade à temperatura ambiente na presença do oxigénio.
A sua fórmula química é C6H5CHCH2. O Estireno é bastante volátil e possui um cheiro adocicado, que, a concentrações elevadas, torna-se bastante desagradável. O Estireno é o percursor do poliestireno, um importantíssimo material sintético, rígido, transparente (semelhante ao acrílico) muito utilizado comercialmente. A polimerização do estireno, juntamente com agentes de expansão, dá origem ao "isopor" (BR) ou "esferovite" (PT).
Ocorrência, história e utilizações[editar | editar código-fonte]
A história do estireno está ligada à história do seu polímero: em 1839, o farmacêutico alemão Eduard Simon extraiu uma substância oleosa da árvore estoraque (storax), e deixou esta resina em repouso. Alguns dias mais tarde, e a encontrou polimerizada.[1]
O estireno pode ser encontrado em plantas, frutos, vegetais, nozes, bebidas e carnes, que possuem naturalmente níveis baixos da substância.
Devido ao facto de a molécula do estireno possuir um grupo vinil com uma dupla ligação, ele pode polimerizar e dar origem a uma grande variedade de materiais plásticos tal como o Poliestireno, ABS, Borracha de Estireno-Butadieno (SBR), Estireno-Isopreno-Estireno (SIS), Estireno-Divinilbenzeno (S-DVB) e poliésteres insaturados. Estes materiais são utilizados em Borracha artificial, isolamentos, fibra de vidro, tubagens, componentes para automóveis e embarcações, embalagens de comida, etc..
Produção[editar | editar código-fonte]
O Estireno é produzido em quantidades industriais a partir do Etilbenzeno, o qual é preparado a partir do Benzeno e etileno.[2]
Desidrogenação do Etilbenzeno[editar | editar código-fonte]
O Estireno é comumente produzido pela desidrogenação catalítica do Etilbenzeno. Este é misturado na sua fase gasosa com 10-15 vezes o seu volume com vapor a alta-temperatura e passado por um leito de catalisador sólido. A maioria dos catalisadores da desidrogenação do Etilbenzeno são baseados em Óxido de Ferro (III), promovido por uma percentagem de Óxido de potássio ou Carbonato de potássio. Neste catalisador ocorre uma reacção química endotérmica reversível. [3]
 |
|
 |
H2 |
O Vapor desempenha vários papeis nesta reacção. É a fonte de calor para potenciar a reacção endotermica e remove o coque que se tende a formar no catalisador de Óxido de ferro III, através da reacção de mudança do vapor de água. O promotor de Potássio activa esta reacção de descoquificação. O vapor também dilui os reagentes e os produtos, deslocando a posição do equilíbrio químico para os produtos da reacção. Uma fábrica típica de Estireno consiste em dois ou três reactores em série, os quais operam sob vácuo para enriquecer a conversão e a selectividade. Conversões típicas situam-se em 65% para um reactor e 70-75% para três reactores. A selectividade para o Estireno é 93-97%. Os principais subprodutos são o Benzeno e o Tolueno. Como o Estireno e o Etilbenzeno possuem temperaturas de ebulição similares (145 °C e 136 °C, respectivamente) a sua separação requer torres de destilação grandes com elevadas razões de retorno/refluxo. À sua temperatura de destilação, o Estireno tende a polimerizar. Para minimizar este problema, as fábricas mais antigas adicionavam Enxofre para inibí-la. Durante os anos 70, foram desenvolvidos novos inibidores de radicais livres baseados em retardantes à base de resinas fenólicas nitrificadas. Mais recentemente foram desenvolvidos aditivos que proporcionam uma inibição da polimerização superior. No entanto as resinas fenólicas nitrificadas continuam a ser muito usadas devido ao seu baixo custo. Estes reagentes são adicionados antes da destilação.
A melhoria da conversão, e por isso a redução da quantidade de Etilbenzeno é o objectivo principal na procura de reacções alternativas para a produção do Estireno. Até agora ainda e para além do método POSM, não foi demonstrada comercialmente qualquer alternativa.
Via Hidroperóxido de Eltilbenzeno[editar | editar código-fonte]
Comercialmente, o Estireno é co-produzido com Óxido de propileno num processo conhecido por POSM (Propylene Oxide/Styrene Monomer).[4]
Neste processo o Etilbenzeno reage com o Oxigénio para formar o Hidroperóxido de Etilbenzeno. Este hidroperóxido é então usado para oxidar o Propileno para Óxido de propileno. O Feniletanol resultante é desidratado para formar o Estireno:[5]
- C6H5CH2CH3 + O2 → C6H5CH2CH2O2H
- C6H5CH2CH2O2H + CH3CH=CH2 → C6H5CH2CH2OH + CH3CHCH2O
- C6H5CH2CH2OH → C6H5CH=CH2 + H2O
Síntese Laboratorial[editar | editar código-fonte]
A Síntese Laboratorial do Estireno implica a descarboxilação do Ácido cinâmico.[6]
Outros métodos[editar | editar código-fonte]
A Exelus Inc. (Livingston NJ, USA) produz Estireno a partir do Tolueno e Metanol, a 425 °C e à pressão atmosférica, forçando estes dois componentes a passar através de um catalisador zeolítico que produz uma mistura Estireno/Etilbenzeno de 9:1.[7]
Efeitos para a Saúde Humana[editar | editar código-fonte]
O Estireno é pouco tóxico,com uma dose letal DL50</sub de 500–5 000 mg (Ratos).[2]
A Agência Americana para Substâncias Tóxicas e Registo de Doenças (ATSDR) afirma que a exposição humana a elevados níveis de Estireno (superiores a 1 000 vezes ao nível normalmente encontrado na natureza) pode induzir efeitos adversos no sistema nervoso. Estes efeitos incluem mudanças na visão colorida, cansaço, sensação de embriaguês, lentidão no tempo de reacção, problemas de concentração ou de equilíbrio.[8]
O Estireno está classificado como possível substância carcinogénica pela Agência internacional de pesquisa do câncer (IARC).[9] A Agência Americana de Protecção do Ambiente (EPA) não atribuiu ao Estireno a classificação de cancerígeno, mas encontra-se a avaliar a sua carcinogenicidade potencial. A EPA descreve o Estireno como um "carcinogénico suspeito" e "Toxina suspeita de afectar os sistemas respiratório, gástrico e hepático, entre outros".[10][11][12]
Metabolismo[editar | editar código-fonte]
O metabolismo do estireno ocorre no fígado humano, e em menor medida no pulmão; esta reação origina um metabolito reativo, o 7,8-dióxido de estireno (SO). O SO é hidrolisado pela epóxido hidrolase microssomal a estirenoglicol, que é por sua vez oxidado nos principais metabolitos finais, ácido mandélico e ácido fenilglioxílico. O SO também pode ser conjugado com a glutationa-S-transferase, originando ácidos mercaptúricos. Uma outra via do metabolismo do estireno resulta da 3,4-epoxidação do seu anel pelo citocromo P450, dando origem ao 4-vinilfenol.[13]
O SO é considerado diretamente responsável pelos efeitos genotóxicos do estireno, já que possui capacidade de se ligar covalentemente ao DNA; foi, então, classificado pela IARC no grupo 2A, provavelmente cancerígeno para os seres humanos, com suficiente evidência de carcinogenicidade em animais experimentais, e inadequada evidência em seres humanosss.[14]
Símbolos de Perigo[editar | editar código-fonte]


Referências
- ↑ A History of EPS: From Apothecary to Factory, site Universal Foam Products
- ↑ a b Denis H. James William M. Castor, "Styrene" in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ↑ Rangel, Alcinéia C. Oliveira e Mª do Carmo (2003). «Desidrogenação do Etilbenzeno sobre Compostos de Ferro e Alumínio». Quimica Nova. 26 (2): 170–176
- ↑ Filipe Miguel dos Santos Catarino (2012) Caracterização da exposição e eventuais efeitos para a saúde da exposição profissional ao estireno nos ortoprotésicos Escola Superior de Tecnologia da Saúde de Lisboa, p. 18
- ↑ Letícia de Albuquerque Galvão (2016) Estudo da copolimerização de estireno e cardanol em meios homogêneo e heterogêneo UFRJ
- ↑ Abbott, T. W.; Johnson, J. R. (1941). «Phenylethylene (Styrene)». Org. Synth.; Coll. Vol., 1
- ↑ Stephen K. Ritter, Chemical & Engineering News, 19 March 2007, p.46
- ↑ «Título ainda não informado (favor adicionar)» (PDF)
- ↑ «Styrene». Occupational Safety and Health Administration. Consultado em 2 de dezembro de 2007
- ↑ «EPA settles case against Phoenix company for toxic chemical reporting violations». U.S. Environmental Protection Agency. Consultado em 11 de fevereiro de 2008
- ↑ «EPA Fines California Hot Tub Manufacturer for Toxic Chemical Release Reporting Violations». U.S. Environmental Protection Agency. Consultado em 11 de fevereiro de 2008
- ↑ Styrene-Guidechem.com
- ↑ «Toxicocinética do estireno». Junho de 2015
- ↑ «Toxicidade do estireno». Junho de 2015
