Benzaldeído
| Benzaldeído ou Aldeído Benzoico (duas nomenclaturas usuais assim como todo aldeído) Alerta sobre risco à saúde | |
|---|---|
|
|
| Nome IUPAC | Fenilmetanal |
| Nome sistemático | Benzenocarbaldeído |
| Outros nomes | Fenilmetanal Benzenecarboxaldeído Aldeído benzóico |
| Identificadores | |
| Número CAS | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C7H6O |
| Massa molar | 106.13 g/mol |
| Aparência | líquido incolor |
| Densidade | 1.0415 g/ml, líquido |
| Ponto de fusão |
−26 °C |
| Ponto de ebulição |
178.1 °C |
| Solubilidade em água | levemente solúvel (0.6 em peso a 20 °C) |
| Viscosidade | 1.4 cP a 25 °C |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
−86.8 kJ/mol |
| Entalpia padrão de combustão ΔcH |
−3525.1 kJ/mol |
| Riscos associados | |
| MSDS | J. T. Baker |
| Classificação UE | Nocivo (Xn) |
| NFPA 704 | |
| Frases R | R22 |
| Frases S | S2, S24 |
| Ponto de fulgor | 63 °C (Closed Cup) |
| Compostos relacionados | |
| Aldeídos relacionados | Anisaldeído (4-metóxi-benzaldeído) Vanilina (4-hidroxi-3-metóxi-benzaldeído) |
| Compostos relacionados | Álcool benzílico Ácido benzoico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
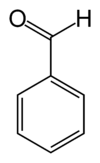
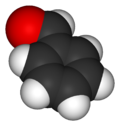
O benzaldeído ou aldeído benzoico (fórmula C6H5-CHO) é um composto orgânico formado por um anel de benzeno com um grupo aldeído. Existe nas amêndoas, e portanto é usado como sabor artificial em alimentos. Além de ser usado como um aromatizante e flavorizante em alimentos, é também usado em perfumes, na indústria dos corantes e possui uso farmacológico. Na verdade, benzaldeído é o principal componente do óleo de amêndoas amargas e pode ser extraído de uma série de outras fontes naturais. Apresenta-se como um líquido incolor, algo viscoso e com alto índice de refração. Na presença de oxigênio oxida-se lentamente a ácido benzoico.
Produção[editar | editar código-fonte]
Benzaldeído pode ser obtido por vários processos. Na década de 1980, 18 milhões de kg foram produzidos anualmente no Japão, Europa e América do Norte, a um nível que pode ser assumido como contínuo. Atualmente cloração na fase líquida e oxidação de tolueno são as principais rotas. Inúmeros outros métodos têm sido desenvolvidos, como a oxidação parcial do álcool benzílico, hidrólise alcalina de cloreto de benzal e a carbonilação de benzeno.[1]
Benzaldeído pode ser sintetizado a partir de cinamaldeído obtido a partir do óleo de canela por refluxo em soluções aquosa/alcoólicas entre 90°C e 150°C, com uma base (mais comumente carbonato ou bicarbonato de sódio) de 5 até 80 horas,[2] seguida de destilação do benzaldeído formado. Esta reação também produz acetaldeído.
Questões de segurança[editar | editar código-fonte]
Alguns dos contaminantes do benzaldeído, como muitos compostos aromáticos, podem ser carcinógenos.
Derivados[editar | editar código-fonte]
Estuda-se a biotransformação do benzaldeído por Saccharomyces cerevisiae produzindo álcool benzílico, PAC (fenilacetilcarbinol) e PAC-diol[3][4] e por Torulaspora delbrueckii a L-PAC, em conversão a efedrina por ação de radiação de microondas[5] e na presença de beta-ciclodextrina.[6]
Referências
- ↑ Friedrich Brühne and Elaine Wright “Benzaldehyde” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a03_463
- ↑ http://www.patentstorm.us/patents/pdfs/patent_id/4617419.html, Process for preparing natural benzaldehyde and acetaldehyde, natural benzaldehyde and acetaldehyde compositions, products produced thereby and organoleptic utilities therefor, Charles Wienes, Middletown; Alan O. Pittet, Atlantic Highlands, both of N.J.
- ↑ Daniel Henrico Risch, Renato Wendhausen Júnior; Biotransformação do Benzaldeído por Saccharomyces cerevisiae; 30a Reunião Anual da Sociedade Brasileira de Química
- ↑ Shukla V. B.; Kulkarni, P. R., World Journal of Microbiology & Biotechnology, 2000, 16, 499-506.
- ↑ Vilas B Shukla, Virendra R Madyar, Bhushan M Khadilkar, Pushpa R Kulkarni; Biotransformation of benzaldehyde to L-phenylacetylcarbinol (L-PAC) by Torulaspora delbrueckii and conversion to ephedrine by microwave radiation; Journal of Chemical Technology & Biotechnology; Volume 77 Issue 2, Pages 137 - 140, 2002 DOI 10.1002/jctb.534
- ↑ Vilas. B. Shukla and Pushpa R. Kulkarni; Biotransformation of Benzaldehyde to L-Phenylacetylcarbinol (L-PAC) by Free Cells of Torulaspora delbrueckii in presence of Beta-Cyclodextrin; Braz. arch. biol. technol. vol.45 no.3 Curitiba Sept. 2002; DOI doi: 10.1590/S1516-89132002000300003

