Genisteína
A tradução deste artigo está abaixo da qualidade média aceitável. (Setembro de 2021) |
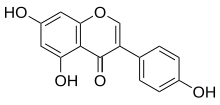
A genisteína é um fitoestrogênio, de formula C15H10O5, que pertence à categoria das isoflavonas. A genisteína foi isolada pela primeira vez em 1899, a partir da vassoura-de-tintureiro, Genista tinctoria; daí, o nome químico, derivado do genérico. O composto do núcleo foi estabelecido em 1926, quando se verificou ser idêntico ao prunetol. Foi sintetizado quimicamente em 1928.[1]
Ocorrências naturais[editar | editar código-fonte]
Isoflavonas, como a genisteína e a daidzeína, são encontradas em uma série de plantas, incluindo tremoço, fava, soja, kudzu e Psoralea, atuando como a principal fonte energética[2][3]. São encontradas também em plantas fitoterápicas, em Flemingia vestita[4] , F. Macrophylla[5][6] e no café[7]. Também podem ser encontradas na Maackia amurensis e em outras culturas celulares.[8]
Extração e purificação[editar | editar código-fonte]
A maioria das isoflavonas nas plantas estão presentes numa forma glicosilada. As formas não glicosiladas, agliconas, podem ser obtidas através de diversos meios, tais como: o tratamento com o enzima β-glicosidase; o tratamento de grãos de soja, seguido por extração com solvente ácido; ou por meios químicos, como a sintese. O tratamento com ácido é um método rigoroso, que envolve a utilização de compostos perigosos, como ácidos inorgânicos concentrados. Tanto o tratamento enzimático, quanto a síntese química, são dispendiosos.[9]
Efeitos biológicos[editar | editar código-fonte]
Além de atuar como antioxidantes e anti-helmínticos, foi-se demonstrado que muitas isoflavonas são capazes de interagir com receptores de estrogênio de animais e humanos, causando efeitos similares aos do hormônio estrogênio natural. As isoflavonas também produzem efeitos não-hormonais.
Funções biomoleculares[editar | editar código-fonte]
A genisteína influencia várias funções bioquímicas em células vivas:
- agonista total de ERβ (EC50 = 7,62 nM) e, em muito menor extensão (aproximadamente 20 vezes menos), agonista total [10] ou agonista parcial de ERα [11];
- agonista do receptor de estrogênio acoplado à proteína G (afinidade de 133 nM) [12][13];
- ativação de receptores ativados por proliferadores de peroxissoma (PPARs);
- inibição de várias tirosina quinases;
- inibição da topoisomerase;
- inibição de AADC;
- antioxidação direta com alguns recursos proxidativos;
- ativação da resposta antioxidante Nrf2;
- estimulação da autofagia [14][15][16];
- inibição do transportador de hexose de mamíferos, a GLUT1;
- contração de vários tipos de músculos lisos;
- modulação do canal CFTR, potencializando sua abertura em baixas concentrações e inibindo-o em doses maiores;
- inibição da metilação da citosina;
- inibição da DNA metiltransferase [17];
- inibição do receptor de glicina;
- inibição do receptor nicotínico de acetilcolina [18].
Ativação de PPARs[editar | editar código-fonte]
As isoflavonas genisteína e daidzeína ligam-se e transativam todas as três isoformas PPAR: α, δ e γ.[19] Por exemplo, o ensaio de ligação do PPARγ ligado à membrana mostrou que a genisteína pode interagir diretamente com o domínio de ligação do ligante PPARγ, e tem um Ki mensurável de 5,7 mM.[20] Ensaios de repórter do gene mostraram que a genisteína em concentrações entre 1 e 100 uM ativou PPARs de uma forma dependente da dose em células progenitoras mesenquimais KS483, células MCF-7 de câncer de mama, células T47D e células MDA-MD-231, células RAW 264.7 semelhantes a macrófagos murinos , células endoteliais e em células Hela. Vários estudos mostraram que ambos os ERs e PPARs influenciam um ao outro e, portanto, induzem efeitos diferenciais de uma forma dependente da dose. Os efeitos biológicos finais da genisteína são determinados pelo equilíbrio entre essas ações pleiotróficas.[19][21][22]
Inibidor da tirosina quinase[editar | editar código-fonte]
A principal atividade conhecida de genisteína é inibidor da tirosina quinase , a maioria de receptor do fator de crescimento epidérmico (EGFR). Tirosina quinases são menos difundido do que o seu ser / thr homólogos, mas implicado em quase todo o crescimento celular e cascatas de sinais de proliferação.
Redox-ativo — Não apenas antioxidante[editar | editar código-fonte]
A genisteína pode atuar como antioxidante direto, semelhante a muitas outras isoflavonas e, portanto, pode aliviar os efeitos danosos dos radicais livres nos tecidos.[23][24]
A mesma molécula de genisteína, semelhante a muitas outras isoflavonas, por geração de radicais livres envenena a topoisomerase II, uma enzima importante para manter a estabilidade do DNA.[25][26][27]
As células humanas ativam o fator Nrf2 de desintoxicação benéfico em resposta ao insulto da genisteína. Esta via pode ser responsável pelas propriedades de manutenção da saúde observadas de pequenas doses de genisteína.[28]
Anti-helmíntico[editar | editar código-fonte]
O extrato de casca de tubérculo de raiz da planta leguminosa Felmingia vestita é o anti-helmíntico tradicional das tribos Khasi da Índia. Durante a investigação de sua atividade anti-helmíntica, descobriu-se que a genisteína é a principal isoflavona responsável pela propriedade de desparasitação.[4][29] A genisteína foi subsequentemente demonstrada ser altamente eficaz contra parasitas intestinais, como o cestódeo de aves Raillietina echinobothrida,[29] o trematódeo de porco Fasciolopsis buski,[30] e o verme de fígado de ovelha Fasciola hepatica.[31]
Ele exerce sua atividade anti-helmíntica inibindo as enzimas da glicólise e glicogenólise,[32][33] e perturbando a homeostase do Ca2+ e a atividade do NO nos parasitas.[34][35] Também foi investigado em tênias humanas, como Echinococcus multilocularis e E. granulosus metacestodes, que a genisteína e seus derivados, Rm6423 e Rm6426, são cestocidas potentes.[36]
Receptor de estrógeno[editar | editar código-fonte]
Devido à sua estrutura similar a 17-β-estradiol (estrogênio), a genisteína pode competir com ela e se ligar aos receptores de estrogênio. No entanto, a genisteína demonstra maior afinidade ao receptor de estrogênio β do que ao receptor de estrogénio α.[37]
Dados de pesquisas in vitro e in vivo confirmam que a genisteína pode aumentar a taxa de crescimento de alguns cânceres de mama que expressam RE. Foi descoberto que a genisteína aumenta a taxa de proliferação de câncer de mama dependente de estrogênio quando não co-tratada com um antagonista de estrogênio.[38][39][40] Ela também diminuiu a eficiência do tamoxifeno e do letrozol - medicamentos comumente usados na terapia do câncer de mama.[41][42] Descobriu-se que a genisteína inibe a resposta imunológica às células cancerosas, permitindo sua sobrevivência.[43]
Efeitos no sexo masculino[editar | editar código-fonte]
As isoflavonas podem atuar como fitoestrógeno em mamíferos, podendo causar efeitos estrogênicos e/ou antiestrogênicos. Estudos in vitro têm demonstrado que a genisteína induzir apoptose das células testiculares em certos níveis, elevando preocupações sobre os efeitos que poderia ter sobre a fertilidade masculina;[44] entretanto, um estudo descobriu que as isoflavonas não tiveram "nenhum efeito observável nas medições endócrinas, volume testicular ou parâmetros de sêmen durante o período de estudo" em homens saudáveis que receberam suplementos de isoflavona diariamente durante um período de 2 meses.[45]
Potencial cancerígeno e tóxico[editar | editar código-fonte]
A genisteína foi, entre outros flavonóides, considerada um forte inibidor da topoisomerase, de forma semelhante a algumas drogas quimioterápicas anticâncer. etoposídeo e doxorrubicina.[25][46] Em altas doses, ele foi fortemente tóxico para células normais. Esse efeito pode ser responsável pelo potencial anticarcinogênico e carcinogênico da substância.[27][47] Descobriu-se que ele deteriora o DNA de células-tronco do sangue em cultura, o que pode causar leucemia.[48] Suspeita-se que a genisteína entre outros flavonóides aumenta o risco de leucemia infantil quando consumida durante a gravidez.[49][50]
Tratamento da Síndrome de Sanfilippo[editar | editar código-fonte]
A genisteína diminui a acumulação patológica de glicosaminoglicanos na síndrome de Sanfilippo. in vitro os estudos clínicos e experiências com animais sugerem que os sintomas da doença podem ser atenuadas por dose adequada de genisteína.[51] A genisteína foi encontrada também possuem propriedades tóxicas em relação a células do cérebro.[51] Entre muitas vias estimuladas por genisteína, autofagia pode explicar a eficácia observada da substância como autofagia é significativamente prejudicada na doença.[52][53]
Referências
- ↑ Walter, E. D. (1941). «Genistin (an Isoflavone Glucoside) and its Aglucone, Genistein, from Soybeans». Journal of the American Chemical Society. 63 (12): 3273–76. doi:10.1021/ja01857a013
- ↑ Kaufman, Peter B.; Duke, James A.; Brielmann, Harry; Boik, John; Hoyt, James E. (1997). «A Comparative Survey of Leguminous Plants as Sources of the Isoflavones, Genistein and Daidzein: Implications for Human Nutrition and Health». The Journal of Alternative and Complementary Medicine. 3 (1): 7–12. PMID 9395689. doi:10.1089/acm.1997.3.7
- ↑ Coward, Lori; Barnes, Neil C.; Setchell, Kenneth D. R.; Barnes, Stephen (1993). «Genistein, daidzein, and their β-glycoside conjugates: Antitumor isoflavones in soybean foods from American and Asian diets». Journal of Agricultural and Food Chemistry. 41 (11): 1961–7. doi:10.1021/jf00035a027
- ↑ a b Rao, H. S. P.; Reddy, K. S. (1991). «Isoflavones from Flemingia vestita». Fitoterapia. 62 (5). 458 páginas
- ↑ Rao, K. Nageswara; Srimannarayana, G. (1 de janeiro de 1983). «Fleminone, a flavanone from the stems of Flemingia macrophylla». Phytochemistry (em inglês) (10): 2287–2290. ISSN 0031-9422. doi:10.1016/S0031-9422(00)80163-6. Consultado em 7 de dezembro de 2022
- ↑ Wang, Bor-Sen; Juang, Lih-Jeng; Yang, Jeng-Jer; Chen, Li-Ying; Tai, Huo-Mu; Huang, Ming-Hsing (10 de setembro de 2012). «Antioxidant and Antityrosinase Activity of Flemingia macrophylla and Glycine tomentella Roots». Evidence-Based Complementary and Alternative Medicine (em inglês): e431081. ISSN 1741-427X. PMC PMC3444970
 Verifique
Verifique |pmc=(ajuda). PMID 22997529. doi:10.1155/2012/431081. Consultado em 7 de dezembro de 2022 - ↑ Alves, Rita C.; Almeida, Ivone M. C.; Casal, Susana; Oliveira, M. Beatriz P. P. (10 de março de 2010). «Isoflavones in Coffee: Influence of Species, Roast Degree, and Brewing Method». Journal of Agricultural and Food Chemistry (em inglês) (5): 3002–3007. ISSN 0021-8561. doi:10.1021/jf9039205. Consultado em 7 de dezembro de 2022
- ↑ Fedoreyev, S. A; Pokushalova, T. V; Veselova, M. V; Glebko, L. I; Kulesh, N. I; Muzarok, T. I; Seletskaya, L. D; Bulgakov, V. P; Zhuravlev, Yu. N (1 de agosto de 2000). «Isoflavonoid production by callus cultures of Maackia amurensis». Fitoterapia (em inglês) (4): 365–372. ISSN 0367-326X. doi:10.1016/S0367-326X(00)00129-5. Consultado em 7 de dezembro de 2022
- ↑ Patravale, VB; Pandit, NT (2011). «Design and optimization of a novel method for extraction of genistein». Indian Journal of Pharmaceutical Sciences. 73 (2): 184–92. PMC 3267303
 . PMID 22303062. doi:10.4103/0250-474x.91583
. PMID 22303062. doi:10.4103/0250-474x.91583
- ↑ Patisaul, Heather B.; Melby, Melissa; Whitten, Patricia L.; Young, Larry J. (2002). «Genistein Affects ERβ- But Not ERα-Dependent Gene Expression in the Hypothalamus». Endocrinology. 143 (6): 2189–2197. ISSN 0013-7227. PMID 12021182. doi:10.1210/endo.143.6.8843

- ↑ Green, Sarah E (2015), In Vitro Comparison of Estrogenic Activities of Popular Women's Health Botanicals
- ↑ Prossnitz ER, Arterburn JB (julho de 2015). «International Union of Basic and Clinical Pharmacology. XCVII. G Protein-Coupled Estrogen Receptor and Its Pharmacologic Modulators». Pharmacol. Rev. 67 (3): 505–40. PMC 4485017
 . PMID 26023144. doi:10.1124/pr.114.009712
. PMID 26023144. doi:10.1124/pr.114.009712
- ↑ Prossnitz, Eric R.; Barton, Matthias (2014). «Estrogen biology: New insights into GPER function and clinical opportunities». Molecular and Cellular Endocrinology. 389 (1–2): 71–83. ISSN 0303-7207. PMC 4040308
 . PMID 24530924. doi:10.1016/j.mce.2014.02.002
. PMID 24530924. doi:10.1016/j.mce.2014.02.002
- ↑ Gossner, G; Choi, M; Tan, L; Fogoros, S; Griffith, K; Kuenker, M; Liu, J (2007). «Genistein-induced apoptosis and autophagocytosis in ovarian cancer cells». Gynecologic Oncology. 105 (1): 23–30. PMID 17234261. doi:10.1016/j.ygyno.2006.11.009
- ↑ Singletary, K.; Milner, J. (2008). «Diet, Autophagy, and Cancer: A Review». Cancer Epidemiology, Biomarkers & Prevention. 17 (7): 1596–610. PMID 18628411. doi:10.1158/1055-9965.EPI-07-2917

- ↑ Nakamura, Yoshitaka; Yogosawa, Shingo; Izutani, Yasuyuki; Watanabe, Hirotsuna; Otsuji, Eigo; Sakai, Tosiyuki (2009). «A combination of indol-3-carbinol and genistein synergistically induces apoptosis in human colon cancer HT-29 cells by inhibiting Akt phosphorylation and progression of autophagy». Molecular Cancer. 8. 100 páginas. PMC 2784428
 . PMID 19909554. doi:10.1186/1476-4598-8-100
. PMID 19909554. doi:10.1186/1476-4598-8-100
- ↑ Fang, Mingzhu; Chen, Dapeng; Yang, Chung S. (janeiro de 2007). «Dietary polyphenols may affect DNA methylation». The Journal of Nutrition. 137 (1 Suppl): 223S–228S. PMID 17182830. doi:10.1093/jn/137.1.223S

- ↑ Glushakov, A. V.; Glushakova, H. Y.; Skok, V. I. (15 de janeiro de 1999). «Modulation of nicotinic acetylcholine receptor activity in submucous neurons by intracellular messengers». Journal of the Autonomic Nervous System. 75 (1): 16–22. ISSN 0165-1838. PMID 9935265. doi:10.1016/S0165-1838(98)00165-9
- ↑ a b Wang, Limei; Waltenberger, Birgit; Pferschy-Wenzig, Eva-Maria; Blunder, Martina; Liu, Xin; Malainer, Clemens; Blazevic, Tina; Schwaiger, Stefan; Rollinger, Judith M.; Heiss, Elke H.; Schuster, Daniela; Kopp, Brigitte; Bauer, Rudolf; Stuppner, Hermann; Dirsch, Verena M.; Atanasov, Atanas G. (2014). «Natural product agonists of peroxisome proliferator-activated receptor gamma (PPARγ): A review». Biochemical Pharmacology. 92 (1): 73–89. PMC 4212005
 . PMID 25083916. doi:10.1016/j.bcp.2014.07.018
. PMID 25083916. doi:10.1016/j.bcp.2014.07.018
- ↑ Dang, Zhi-Chao; Audinot, Valérie; Papapoulos, Socrates E.; Boutin, Jean A.; Löwik, Clemens W. G. M. (2002). «Peroxisome Proliferator-activated Receptor γ (PPARγ) as a Molecular Target for the Soy Phytoestrogen Genistein». Journal of Biological Chemistry. 278 (2): 962–7. PMID 12421816. doi:10.1074/jbc.M209483200

- ↑ Dang, Zhi Chao; Lowik, Clemens (2005). «Dose-dependent effects of phytoestrogens on bone». Trends in Endocrinology and Metabolism. 16 (5): 207–13. PMID 15922618. doi:10.1016/j.tem.2005.05.001
- ↑ Dang, Z. C. (2009). «Dose-dependent effects of soy phyto-oestrogen genistein on adipocytes: Mechanisms of action». Obesity Reviews. 10 (3): 342–9. PMID 19207876. doi:10.1111/j.1467-789X.2008.00554.x
- ↑ Han, Rui-Min; Tian, Yu-Xi; Liu, Yin; Chen, Chang-Hui; Ai, Xi-Cheng; Zhang, Jian-Ping; Skibsted, Leif H. (2009). «Comparison of Flavonoids and Isoflavonoids as Antioxidants». Journal of Agricultural and Food Chemistry. 57 (9): 3780–5. PMID 19296660. doi:10.1021/jf803850p
- ↑ Borrás, Consuelo; Gambini, Juan; López-Grueso, Raúl; Pallardó, Federico V.; Viña, Jose (2010). «Direct antioxidant and protective effect of estradiol on isolated mitochondria» (PDF). Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease. 1802 (1): 205–11. PMID 19751829. doi:10.1016/j.bbadis.2009.09.007
- ↑ a b Bandele, Omari J.; Osheroff, Neil (2007). «Bioflavonoids as Poisons of Human Topoisomerase IIα and IIβ». Biochemistry. 46 (20): 6097–108. PMC 2893030
 . PMID 17458941. doi:10.1021/bi7000664
. PMID 17458941. doi:10.1021/bi7000664
- ↑ Markovits, Judith; Linassier, Claude; Fossé, Philippe; Couprie, Jeanine; Pierre, Josiane; Jacquemin-Sablon, Alain; Saucier, Jean-Marie; Le Pecq, Jean-Bernard; Larsen, Annette K. (setembro de 1989). «Inhibitory effects of the tyrosine kinase inhibitor genistein on mammalian DNA topoisomerase II». Cancer Research. 49 (18): 5111–7. PMID 2548712
- ↑ a b López-Lázaro, Miguel; Willmore, Elaine; Austin, Caroline A. (2007). «Cells Lacking DNA Topoisomerase IIβ are Resistant to Genistein». Journal of Natural Products. 70 (5): 763–7. PMID 17411092. doi:10.1021/np060609z
- ↑ Mann, Giovanni E; Bonacasa, Barbara; Ishii, Tetsuro; Siow, Richard CM (2009). «Targeting the redox sensitive Nrf2–Keap1 defense pathway in cardiovascular disease: Protection afforded by dietary isoflavones». Current Opinion in Pharmacology. 9 (2): 139–45. PMID 19157984. doi:10.1016/j.coph.2008.12.012
- ↑ a b Tandon, V.; Pal, P.; Roy, B.; Rao, H. S. P.; Reddy, K. S. (1997). «In vitro anthelmintic activity of root-tuber extract of Flemingia vestita, an indigenous plant in Shillong, India». Parasitology Research. 83 (5): 492–8. PMID 9197399. doi:10.1007/s004360050286
- ↑ Kar, Pradip K; Tandon, Veena; Saha, Nirmalendu (2002). «Anthelmintic efficacy of Flemingia vestita: Genistein-induced effect on the activity of nitric oxide synthase and nitric oxide in the trematode parasite, Fasciolopsis buski». Parasitology International. 51 (3): 249–57. PMID 12243779. doi:10.1016/S1383-5769(02)00032-6
- ↑ Toner, E.; Brennan, G. P.; Wells, K.; McGeown, J. G.; Fairweather, I. (2008). «Physiological and morphological effects of genistein against the liver fluke, Fasciola hepatica». Parasitology. 135 (10): 1189–203. PMID 18771609. doi:10.1017/S0031182008004630
- ↑ Tandon, Veena; Das, Bidyadhar; Saha, Nirmalendu (2003). «Anthelmintic efficacy of Flemingia vestita (Fabaceae): Effect of genistein on glycogen metabolism in the cestode, Raillietina echinobothrida». Parasitology International. 52 (2): 179–86. PMID 12798931. doi:10.1016/S1383-5769(03)00006-0
- ↑ Das, B.; Tandon, V.; Saha, N. (2004). «Anthelmintic efficacy of Flemingia vestita (Fabaceae): Alteration in the activities of some glycolytic enzymes in the cestode, Raillietina echinobothrida». Parasitology Research. 93 (4): 253–61. PMID 15138892. doi:10.1007/s00436-004-1122-8
- ↑ Das, Bidyadhar; Tandon, Veena; Saha, Nirmalendu (2006). «Effect of isoflavone from Flemingia vestita (Fabaceae) on the Ca2+ homeostasis in Raillietina echinobothrida, the cestode of domestic fowl». Parasitology International. 55 (1): 17–21. PMID 16198617. doi:10.1016/j.parint.2005.08.002
- ↑ Das, Bidyadhar; Tandon, Veena; Lyndem, Larisha M.; Gray, Alexander I.; Ferro, Valerie A. (2009). «Phytochemicals from Flemingia vestita (Fabaceae) and Stephania glabra (Menispermeaceae) alter cGMP concentration in the cestode Raillietina echinobothrida». Comparative Biochemistry and Physiology C. 149 (3): 397–403. PMID 18854226. doi:10.1016/j.cbpc.2008.09.012
- ↑ Naguleswaran, Arunasalam; Spicher, Martin; Vonlaufen, Nathalie; Ortega-Mora, Luis M.; Torgerson, Paul; Gottstein, Bruno; Hemphill, Andrew (2006). «In Vitro Metacestodicidal Activities of Genistein and Other Isoflavones against Echinococcus multilocularis and Echinococcus granulosus». Antimicrobial Agents and Chemotherapy. 50 (11): 3770–8. PMC 1635224
 . PMID 16954323. doi:10.1128/AAC.00578-06
. PMID 16954323. doi:10.1128/AAC.00578-06
- ↑ Kuiper, George G. J. M.; Lemmen, Josephine G.; Carlsson, Bo; Corton, J. Christopher; Safe, Stephen H.; van der Saag, Paul T.; van der Burg, Bart; Gustafsson, Jan-Åke (1998). «Interaction of Estrogenic Chemicals and Phytoestrogens with Estrogen Receptor β». Endocrinology. 139 (10): 4252–63. PMID 9751507. doi:10.1210/endo.139.10.6216

- ↑ Ju, Young H.; Allred, Kimberly F.; Allred, Clinton D.; Helferich, William G. (2006). «Genistein stimulates growth of human breast cancer cells in a novel, postmenopausal animal model, with low plasma estradiol concentrations». Carcinogenesis. 27 (6): 1292–9. PMID 16537557. doi:10.1093/carcin/bgi370

- ↑ Chen, Wen-Fang; Wong, Man-Sau (2004). «Genistein Enhances Insulin-Like Growth Factor Signaling Pathway in Human Breast Cancer (MCF-7) Cells». The Journal of Clinical Endocrinology & Metabolism. 89 (5): 2351–9. PMID 15126563. doi:10.1210/jc.2003-032065

- ↑ Yang, Xiaohe; Yang, Shihe; McKimmey, Christine; Liu, Bolin; Edgerton, Susan M.; Bales, Wesley; Archer, Linda T.; Thor, Ann D. (2010). «Genistein induces enhanced growth promotion in ER-positive/erbB-2-overexpressing breast cancers by ER-erbB-2 cross talk and p27/kip1 downregulation». Carcinogenesis. 31 (4): 695–702. PMID 20067990. doi:10.1093/carcin/bgq007

- ↑ Helferich, W. G.; Andrade, J. E.; Hoagland, M. S. (2008). «Phytoestrogens and breast cancer: A complex story». Inflammopharmacology. 16 (5): 219–26. PMID 18815740. doi:10.1007/s10787-008-8020-0
- ↑ Tonetti, Debra A.; Zhang, Yiyun; Zhao, Huiping; Lim, Sok-Bee; Constantinou, Andreas I. (2007). «The Effect of the Phytoestrogens Genistein, Daidzein, and Equol on the Growth of Tamoxifen-Resistant T47D/PKCα». Nutrition and Cancer. 58 (2): 222–9. PMID 17640169. doi:10.1080/01635580701328545
- ↑ Jiang, Xinguo; Patterson, Nicole M.; Ling, Yan; Xie, Jianwei; Helferich, William G.; Shapiro, David J. (2008). «Low Concentrations of the Soy Phytoestrogen Genistein Induce Proteinase Inhibitor 9 and Block Killing of Breast Cancer Cells by Immune Cells». Endocrinology. 149 (11): 5366–73. PMC 2584580
 . PMID 18669594. doi:10.1210/en.2008-0857
. PMID 18669594. doi:10.1210/en.2008-0857
- ↑ Kumi‐Diaka, James; Rodriguez, Rosanna; Goudaze, Gould (1998). «Influence of genistein (4′,5,7-trihydroxyisoflavone) on the growth and proliferation of testicular cell lines». Biology of the Cell (em inglês) (4): 349–354. ISSN 1768-322X. doi:10.1111/j.1768-322X.1998.tb01044.x. Consultado em 14 de setembro de 2020
- ↑ Mitchell, Julie H.; Cawood, Elizabeth; Kinniburgh, David; Provan, Anne; Collins, Andrew R.; Irvine, D. Stewart (2001). «Effect of a phytoestrogen food supplement on reproductive health in normal males». Clinical Science. 100 (6): 613–8. PMID 11352776. doi:10.1042/CS20000212
- ↑ Lutz, Werner K.; Tiedge, Oliver; Lutz, Roman W.; Stopper, Helga (2005). «Different Types of Combination Effects for the Induction of Micronuclei in Mouse Lymphoma Cells by Binary Mixtures of the Genotoxic Agents MMS, MNU, and Genistein». Toxicological Sciences. 86 (2): 318–23. PMID 15901918. doi:10.1093/toxsci/kfi200

- ↑ Schmidt, Friederike; Knobbe, Christiane; Frank, Brigitte; Wolburg, Hartwig; Weller, Michael (2008). «The topoisomerase II inhibitor, genistein, induces G2/M arrest and apoptosis in human malignant glioma cell lines». Oncology Reports. 19 (4): 1061–6. PMID 18357397. doi:10.3892/or.19.4.1061

- ↑ van Waalwijk van Doorn-Khosrovani, Sahar Barjesteh; Janssen, Jannie; Maas, Lou M.; Godschalk, Roger W. L.; Nijhuis, Jan G.; van Schooten, Frederik J. (2007). «Dietary flavonoids induce MLL translocations in primary human CD34+ cells». Carcinogenesis. 28 (8): 1703–9. PMID 17468513. doi:10.1093/carcin/bgm102

- ↑ Spector, Logan G.; Xie, Yang; Robison, Leslie L.; Heerema, Nyla A.; Hilden, Joanne M.; Lange, Beverly; Felix, Carolyn A.; Davies, Stella M.; Slavin, Joanne; Potter, John D.; Blair, Cindy K.; Reaman, Gregory H.; Ross, Julie A. (2005). «Maternal Diet and Infant Leukemia: The DNA Topoisomerase II Inhibitor Hypothesis: A Report from the Children's Oncology Group». Cancer Epidemiology, Biomarkers & Prevention. 14 (3): 651–5. PMID 15767345. doi:10.1158/1055-9965.EPI-04-0602

- ↑ Azarova, Anna M.; Lin, Ren-Kuo; Tsai, Yuan-Chin; Liu, Leroy F.; Lin, Chao-Po; Lyu, Yi Lisa (2010). «Genistein induces topoisomerase IIbeta- and proteasome-mediated DNA sequence rearrangements: Implications in infant leukemia». Biochemical and Biophysical Research Communications. 399 (1): 66–71. PMC 3376163
 . PMID 20638367. doi:10.1016/j.bbrc.2010.07.043
. PMID 20638367. doi:10.1016/j.bbrc.2010.07.043
- ↑ a b Jin, Ying; Wu, Heng; Cohen, Eric M.; Wei, Jianning; Jin, Hong; Prentice, Howard; Wu, Jang-Yen (2007). «Genistein and daidzein induce neurotoxicity at high concentrations in primary rat neuronal cultures». Journal of Biomedical Science. 14 (2): 275–84. PMID 17245525. doi:10.1007/s11373-006-9142-2
- ↑ Ballabio, A. (2009). «Disease pathogenesis explained by basic science: Lysosomal storage diseases as autophagocytic disorders». International Journal of Clinical Pharmacology and Therapeutics. 47 (Suppl 1): S34–8. PMID 20040309. doi:10.5414/cpp47034
- ↑ Settembre, Carmine; Fraldi, Alessandro; Jahreiss, Luca; Spampanato, Carmine; Venturi, Consuelo; Medina, Diego; de Pablo, Raquel; Tacchetti, Carlo; Rubinsztein, David C.; Ballabio, Andrea (2007). «A block of autophagy in lysosomal storage disorders». Human Molecular Genetics. 17 (1): 119–29. PMID 17913701. doi:10.1093/hmg/ddm289


