Ácido sulfanílico
| Ácido sulfanílico Alerta sobre risco à saúde | |
|---|---|

| |
| Nome IUPAC | Ácido p-aminobenzenossulfônico |
| Outros nomes | Ácido sulfanílico |
| Identificadores | |
| Número CAS | |
| PubChem | |
| SMILES |
|
| InChI | InChI=1/C6H7NO3S/c7-5-
1-3-6(4-2-5)11(8,9)10/h1-4H, 7H2,(H,8,9,10)/f/h8H |
| Propriedades | |
| Fórmula molecular | C6H7NO3S |
| Massa molar | 173.19 |
| Ponto de fusão |
288 °C, 561 K, 550 °F |
| Solubilidade em água | >20 g/l |
| Compostos relacionados | |
| Compostos relacionados | Anilina Ácido benzenosulfónico Ácido p-toluenossulfônico Ácido 2-aminobenzenossulfônico Taurina (2-aminoetanosulfonico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Ácido sulfanílico (ácido 4-aminobenzeno sulfônico, ácido p-aminobenzeno sulfônico ou ácido para-aminobenzeno sulfônico) é um sólido cristalino incolor produzido por sulfonação da anilina[1] de fórmula química C6H6NO3S.
Ele é um zwitterion com um ponto de fusão alto incomum entre substâncias similares.
Síntese[editar | editar código-fonte]
É obtido pela reação a quente do ácido sulfúrico com anilina a 190 °C. Esta reação resultará na adição de um grupo sulfônico por uma substituição eletrofílica na posição p (para) em relação ao grupo amino no anel benzênico.

A partir de uma autoprotólise pré-estabelecida em equilíbrio do ácido sulfúrico resulta o íon H3SO4+:
Este poderá absorver água e formar HSO3+ eletrofílico, o qual poderá atacar o anel benzênico nas posições orto ou para no lugar de protonar o grupo amino.
Trata-se de um exemplo do processo de sulfonação aromática.
Aplicações[editar | editar código-fonte]
Devido a facilmente formar diazo compostos e é usado para a fabricação de corantes (como o alaranjado de metila) e fármacos do tipo sulfa.[1] Esta propriedade é também usada para a análise quantitativa de íons nitrato e nitrito por reação de acoplamento de diazônio com N-(1-Naftil)etilenodiamina, resultando no corante azo, e a concentração de íons nitrato ou nitrito é deduzida da intensidade de cor da solução vermelha resultante por colorimetria.[3]
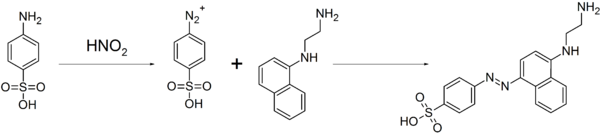
É utilizado para a produção do reagente de Lunges para a análise de nitritos e/ou nitratos.[4]
É usado como um padrão em análises de combustão e na reação de Pauly.
Frequentemente é usado como padrão primário para a produção de soluções padrão, especialmente na análise de fármacos.
Referências
- ↑ a b "Sulphanilic acid". A Dictionary of Chemistry. Oxford University Press, 2000. Oxford Reference Online. Oxford University Press.
- ↑ Siegfried Hauptmann: Organische Chemie, 2nd Edition, VEB Deutscher Verlag für Grundstoffindustrie, Leipzig, 1985, p. 511, ISBN 3-342-00280-8.
- ↑ G. H. Jerffery; J. Bassett; J. Mendham; R. C. Denney (1989). «Colorimetry and Spectrophotometry». Vogel's Textbook of Quantitative Chemical Analysis, 5th Edition. [S.l.]: Longman. p. 702. ISBN 0-582-44693-7
- ↑ S. Ebel und H. J. Roth (Herausgeber): Lexikon der Pharmazie, Georg Thieme Verlag, 1987, S. 405, ISBN 3-13-672201-9.
Ligações externas[editar | editar código-fonte]
- «Ácido Sulfanílico em Faenquil» (PDF)
- Registo na Base de Dados de Substâncias GESTIS do IFA

