Espectroscopia de absorção

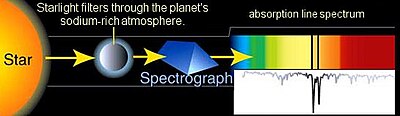
A espectroscopia de absorção refere-se a técnicas espectroscópicas que medem a absorção da radiação, em função da frequência ou comprimento de onda, devido à sua interação com uma amostra. A amostra absorve energia, ou seja, fótons, do campo radiante. A intensidade da absorção varia em função da frequência, e essa variação é o espectro de absorção. A espectroscopia de absorção é realizada em todo o espectro eletromagnético.
A espectroscopia de absorção é empregada como uma ferramenta de química analítica para determinar a presença de uma determinada substância em uma amostra e, em muitos casos, para quantificar a quantidade da substância presente. A espectroscopia de infravermelho e ultravioleta-visível são particularmente comuns em aplicações analíticas. A espectroscopia de absorção também é empregada em estudos de física molecular e atômica, espectroscopia astronômica e sensoriamento remoto.
Existe uma ampla gama de abordagens experimentais para medir espectros de absorção. O arranjo mais comum é direcionar um feixe de radiação gerado em uma amostra e detectar a intensidade da radiação que passa por ela. A energia transmitida pode ser usada para calcular a absorção. A fonte, o arranjo da amostra e a técnica de detecção variam significativamente, dependendo da faixa de frequência e do propósito do experimento.
A seguir estão os principais tipos de espectroscopia de absorção:[1]
| Sr. No | Radiação eletromagnética | Tipo espectroscópico |
|---|---|---|
| 1 | Raios-X | Espectroscopia de absorção de raios-x |
| 2 | Ultravioleta-visível | Espectroscopia de absorção UV-vis |
| 3 | Infravermelho | Espectroscopia de absorção de infravermelho |
| 4 | Microondas | Espectroscopia de absorção de microondas |
| 5 | Onda de rádio | Espectroscopia de ressonância spin de elétrons Espectroscopia de ressonância magnética nuclear |
Espectro de absorção[editar | editar código-fonte]

O espectro de absorção de um material é a fração da radiação incidente absorvida pelo material em uma faixa de frequências da radiação eletromagnética. O espectro de absorção é determinado principalmente[2][3][4] pela composição atômica e molecular do material. É mais provável que a radiação seja absorvida em frequências que correspondem à diferença de energia entre dois estados da mecânica quântica das moléculas. A absorção que ocorre devido a uma transição entre dois estados é chamada de linha de absorção e um espectro é normalmente composto de muitas linhas.
As frequências onde ocorrem as linhas de absorção, bem como suas intensidades relativas, dependem principalmente da estrutura eletrônica e molecular da amostra. As frequências também dependerão das interações entre as moléculas na amostra, da estrutura do cristal em sólidos e de vários fatores ambientais (por exemplo, temperatura, pressão, campo eletromagnético). As linhas também terão uma largura e forma que são principalmente determinadas pela densidade espectral ou a densidade de estados do sistema.
Teoria[editar | editar código-fonte]
As linhas de absorção são normalmente classificadas pela natureza da mudança mecânica quântica induzida na molécula ou átomo. As linhas de rotação, por exemplo, ocorrem quando o estado de rotação de uma molécula é alterado. As linhas de rotação são normalmente encontradas na região espectral de microondas. As linhas vibracionais correspondem a mudanças no estado vibracional da molécula e são normalmente encontradas na região do infravermelho. As linhas eletrônicas correspondem a uma mudança no estado eletrônico de um átomo ou molécula e são normalmente encontradas na região do visível e ultravioleta. As absorções de raios X estão associadas à excitação dos elétrons da camada interna dos átomos. Essas mudanças também podem ser combinadas (por exemplo, transições de rotação-vibração), levando a novas linhas de absorção na energia combinada das duas mudanças.
A energia associada à mudança mecânica quântica determina principalmente a frequência da linha de absorção, mas a frequência pode ser alterada por vários tipos de interações. Os campos elétricos e magnéticos podem causar uma mudança. As interações com moléculas vizinhas podem causar mudanças. Por exemplo, as linhas de absorção da molécula de fase gasosa podem mudar significativamente quando essa molécula está em uma fase líquida ou sólida e interagindo mais fortemente com as moléculas vizinhas.
A largura e a forma das linhas de absorção são determinadas pelo instrumento usado para a observação, o material que absorve a radiação e o ambiente físico desse material. É comum que as linhas tenham a forma de uma distribuição gaussiana ou lorentziana. Também é comum que uma linha seja descrita apenas por sua intensidade e largura, em vez de toda a forma sendo caracterizada.
A intensidade integrada, obtida pela integração da área sob a linha de absorção, é proporcional à quantidade de substância absorvente presente. A intensidade também está relacionada à temperatura da substância e à interação mecânica quântica entre a radiação e o absorvedor. Essa interação é quantificada pelo momento de transição e depende do estado inferior específico a partir do qual a transição começa e do estado superior ao qual está conectada.
A largura das linhas de absorção pode ser determinada pelo espectrômetro usado para registrá-la. Um espectrômetro tem um limite inerente de quão estreita uma linha ele pode resolver e, portanto, a largura observada pode estar neste limite. Se a largura for maior do que o limite de resolução, ela será determinada principalmente pelo ambiente do absorvedor. Um absorvedor líquido ou sólido, no qual moléculas vizinhas interagem fortemente umas com as outras, tende a ter linhas de absorção mais largas do que um gás. O aumento da temperatura ou pressão do material absorvente também tenderá a aumentar a largura da linha. Também é comum que várias transições vizinhas estejam perto o suficiente umas das outras para que suas linhas se sobreponham e a linha geral resultante seja, portanto, ainda mais ampla.
Relação com o espectro de transmissão[editar | editar código-fonte]
Os espectros de absorção e transmissão representam informações equivalentes e uma pode ser calculada a partir da outra por meio de uma transformação matemática. Um espectro de transmissão terá suas intensidades máximas em comprimentos de onda onde a absorção é mais fraca porque mais luz é transmitida através da amostra. Um espectro de absorção terá suas intensidades máximas nos comprimentos de onda onde a absorção é mais forte.
Relação com o espectro de emissão[editar | editar código-fonte]

A emissão é um processo pelo qual uma substância libera energia na forma de radiação eletromagnética. A emissão pode ocorrer em qualquer frequência em que a absorção possa ocorrer, e isso permite que as linhas de absorção sejam determinadas a partir de um espectro de emissão. O espectro de emissão normalmente terá um padrão de intensidade bastante diferente do espectro de absorção, portanto, os dois não são equivalentes. O espectro de absorção pode ser calculado a partir do espectro de emissão usando coeficientes de Einstein.
Relação com espectros de espalhamento e reflexão[editar | editar código-fonte]
Os espectros de espalhamento e reflexão de um material são influenciados por seu índice de refração e seu espectro de absorção. Em um contexto óptico, o espectro de absorção é tipicamente quantificado pelo coeficiente de extinção, e os coeficientes de extinção e índice são quantitativamente relacionados por meio da relação Kramers-Kronig. Portanto, o espectro de absorção pode ser derivado de um espectro de espalhamento ou reflexão. Isso normalmente requer a simplificação de suposições ou modelos e, portanto, o espectro de absorção derivado é uma aproximação.
Aplicações[editar | editar código-fonte]

A espectroscopia de absorção é útil em análises químicas[5] devido à sua especificidade e natureza quantitativa. A especificidade dos espectros de absorção permite que os compostos sejam distinguidos uns dos outros em uma mistura, tornando a espectroscopia de absorção útil em uma ampla variedade de aplicações. Por exemplo, analisadores de gás infravermelho podem ser usados para identificar a presença de poluentes no ar, distinguindo o poluente do nitrogênio, oxigênio, água e outros constituintes esperados.[6]
A especificidade também permite que amostras desconhecidas sejam identificadas pela comparação de um espectro medido com uma biblioteca de espectros de referência. Em muitos casos, é possível determinar informações qualitativas sobre uma amostra, mesmo que ela não esteja em uma biblioteca. Os espectros de infravermelho, por exemplo, têm bandas de absorção características que indicam se as ligações carbono-hidrogênio ou carbono-oxigênio estão presentes.
Um espectro de absorção pode ser quantitativamente relacionado à quantidade de material presente usando a Lei de Lambert-Beer. A determinação da concentração absoluta de um composto requer conhecimento do coeficiente de absorção do composto.
Sensoriamento remoto[editar | editar código-fonte]
Uma das vantagens exclusivas da espectroscopia como técnica analítica é que as medições podem ser feitas sem colocar o instrumento e a amostra em contato. A radiação que viaja entre uma amostra e um instrumento conterá as informações espectrais, de modo que a medição pode ser feita remotamente. A detecção espectral remota é valiosa em muitas situações. Por exemplo, as medições podem ser feitas em ambientes tóxicos ou perigosos sem colocar um operador ou o instrumento em risco. Além disso, o material da amostra não precisa ser colocado em contato com o instrumento, evitando possível contaminação cruzada.
As medições espectrais remotas apresentam vários desafios em comparação com as medições de laboratório. O espaço entre a amostra de interesse e o instrumento também pode ter absorções espectrais. Essas absorções podem mascarar ou confundir o espectro de absorção da amostra. Essas interferências de fundo também podem variar com o tempo. A fonte de radiação em medições remotas costuma ser uma fonte ambiental, como a luz do sol ou a radiação térmica de um objeto quente, e isso torna necessário distinguir a absorção espectral das mudanças no espectro da fonte.
Para simplificar esses desafios, a espectroscopia de absorção óptica diferencial ganhou alguma popularidade, pois se concentra em características de absorção diferencial e omite a absorção de banda larga, como extinção de aerossol e extinção devido ao espalhamento de rayleigh. Este método é aplicado a medições terrestres, aéreas e por satélite. Alguns métodos baseados em terra fornecem a possibilidade de recuperar perfis de gases traço troposféricos e estratosféricos.
Astronomia[editar | editar código-fonte]
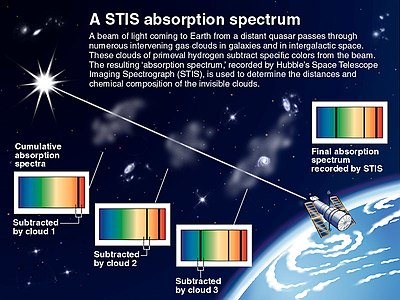
A espectroscopia astronômica é um tipo particularmente significativo de detecção espectral remota. Neste caso, os objetos e amostras de interesse estão tão distantes da Terra que a radiação eletromagnética é o único meio disponível para medi-los. Os espectros astronômicos contêm informações espectrais de absorção e emissão. A espectroscopia de absorção tem sido particularmente importante para entender as nuvens interestelares e determinar que algumas delas contêm moléculas. A espectroscopia de absorção também é empregada no estudo de exoplanetas. A detecção de exoplanetas pelo método de trânsito também mede seu espectro de absorção e permite a determinação da composição atmosférica do exoplaneta,[7] temperatura, pressão e altura de escala e, portanto, permite também a determinação da massa do planeta.[8]
Física atômica e molecular[editar | editar código-fonte]
Modelos teóricos, principalmente modelos de mecânica quântica, permitem que os espectros de absorção de átomos e moléculas sejam relacionados a outras propriedades físicas, como estrutura eletrônica, massa atômica ou molecular e geometria molecular. Portanto, as medições do espectro de absorção são usadas para determinar essas outras propriedades. A espectroscopia de micro-ondas, por exemplo, permite a determinação de comprimentos e ângulos de ligação com alta precisão.
Além disso, as medições espectrais podem ser usadas para determinar a precisão das previsões teóricas. Por exemplo, não era esperado que o desvio de Lamb medido no espectro de absorção atômica do hidrogênio existisse no momento em que foi medido. Sua descoberta estimulou e guiou o desenvolvimento da eletrodinâmica quântica, e as medições do desvio de Lamb agora são usadas para determinar a constante de estrutura fina.
Métodos experimentais[editar | editar código-fonte]
Abordagem básica[editar | editar código-fonte]
A abordagem mais direta para a espectroscopia de absorção é gerar radiação com uma fonte, medir um espectro de referência dessa radiação com um detector e, em seguida, medir novamente o espectro da amostra após colocar o material de interesse entre a fonte e o detector. Os dois espectros medidos podem então ser combinados para determinar o espectro de absorção do material. O espectro da amostra sozinho não é suficiente para determinar o espectro de absorção porque ele será afetado pelas condições experimentais, o espectro da fonte, o espectro de absorção de outros materiais entre a fonte e o detector e as características dependentes do comprimento de onda do detector. O espectro de referência será afetado da mesma maneira, porém, por essas condições experimentais e, portanto, a combinação produz o espectro de absorção do material sozinho.
Uma ampla variedade de fontes de radiação é empregada a fim de cobrir o espectro eletromagnético. Para espectroscopia, é geralmente desejável que uma fonte cubra uma ampla faixa de comprimentos de onda a fim de medir uma ampla região do espectro de absorção. Algumas fontes emitem inerentemente um amplo espectro. Exemplos destes incluem globars ou outras fontes de corpo negro no infravermelho, lâmpadas de mercúrio no visível e ultravioleta e ampolas de raios X. Uma nova fonte recentemente desenvolvida de radiação de amplo espectro é a radiação síncrotron que cobre todas essas regiões espectrais. Outras fontes de radiação geram um espectro estreito, mas o comprimento de onda de emissão pode ser ajustado para cobrir uma faixa espectral. Exemplos destes incluem Klystrons na região das microondas e lasers na região do infravermelho, visível e ultravioleta (embora nem todos os lasers tenham comprimentos de onda sintonizáveis).
O detector empregado para medir a potência da radiação também dependerá da faixa de comprimento de onda de interesse. A maioria dos detectores é sensível a uma faixa espectral bastante ampla e o sensor selecionado geralmente dependerá mais dos requisitos de sensibilidade e ruído de uma determinada medição. Exemplos de detectores comuns em espectroscopia incluem receptores heteródinos nas microondas, bolômetros na onda milimétrica e infravermelho, telureto de mercúrio e cádmio e outros detectores semicondutores resfriados no infravermelho e fotodiodos e tubos fotomultiplicadores no visível e ultravioleta.
Se a fonte e o detector cobrem uma ampla região espectral, então também é necessário introduzir um meio de resolver o comprimento de onda da radiação para determinar o espectro. Frequentemente, um espectrômetro é usado para separar espacialmente os comprimentos de onda da radiação, de modo que a potência em cada comprimento de onda possa ser medida independentemente. Também é comum empregar interferometria para determinar o espectro, a espectroscopia de infravermelho com transformada de Fourier é uma implementação amplamente usada desta técnica.
Duas outras questões que devem ser consideradas na configuração de um experimento de espectroscopia de absorção incluem a ótica usada para direcionar a radiação e os meios de segurar ou conter o material da amostra (chamada de cubeta ou célula). Para a maioria das medições de UV, visível e NIR, é necessário o uso de cubetas de quartzo de precisão. Em ambos os casos, é importante selecionar materiais que tenham relativamente pouca absorção própria na faixa de comprimento de onda de interesse. A absorção de outros materiais pode interferir ou mascarar a absorção da amostra. Por exemplo, em várias faixas de comprimento de onda, é necessário medir a amostra sob vácuo ou em um ambiente de gás raro porque os gases na atmosfera têm características de absorção de interferência.
Abordagens específicas[editar | editar código-fonte]
- Espectroscopia astronômica
- Espectroscopia de anel de cavidade (CRDS)
- Espectrometria de absorção a laser (LAS)
- Espectroscopia Mössbauer
- Espectroscopia fotoacústica
- Espectroscopia de fotoemissão
- Microscopia ótica fototérmica
- Espectroscopia fototérmica
- Espectroscopia de refletância
- Espectroscopia de absorção de laser de diodo ajustável (TDLAS)
- Estrutura fina de absorção de raios X (XAFS)
- Absorção de raios X perto da estrutura da borda (XANES)
- Espectroscopia de absorção total (TAS)
- Espectroscopia infravermelha de reflexão-absorção (RAIRS)
Veja também[editar | editar código-fonte]
Referências
- ↑ Kumar, Pranav (2018). Fundamentals and Techniques of Biophysics and Molecular biology. New Delhi: Pathfinder publication. p. 33. ISBN 978-93-80473-15-4
- ↑ Modern Spectroscopy (Paperback) by J. Michael Hollas ISBN 978-0-470-84416-8
- ↑ Symmetry and Spectroscopy: An Introduction to Vibrational and Electronic Spectroscopy (Paperback) by Daniel C. Harris, Michael D. Bertolucci ISBN 978-0-486-66144-5
- ↑ Spectra of Atoms and Molecules by Peter F. Bernath ISBN 978-0-19-517759-6
- ↑ James D. Ingle Jr. and Stanley R. Crouch, Spectrochemical Analysis, Prentice Hall, 1988, ISBN 0-13-826876-2
- ↑ «Gaseous Pollutants – Fourier Transform Infrared Spectroscopy». Consultado em 30 de setembro de 2009. Arquivado do original em 23 de outubro de 2012
- ↑ Khalafinejad, S.; Essen, C. von; Hoeijmakers, H. J.; Zhou, G.; Klocová, T.; Schmitt, J. H. M. M.; Dreizler, S.; Lopez-Morales, M.; Husser, T.-O. (1 de fevereiro de 2017). «Exoplanetary atmospheric sodium revealed by orbital motion». Astronomy & Astrophysics (em inglês). 598: A131. Bibcode:2017A&A...598A.131K. ISSN 0004-6361. arXiv:1610.01610
 . doi:10.1051/0004-6361/201629473
. doi:10.1051/0004-6361/201629473
- ↑ de Wit, Julien; Seager, S. (19 de dezembro de 2013). «Constraining Exoplanet Mass from Transmission Spectroscopy». Science. 342 (6165): 1473–1477. Bibcode:2013Sci...342.1473D. PMID 24357312. arXiv:1401.6181
 . doi:10.1126/science.1245450
. doi:10.1126/science.1245450
