Sulfeto de carbonila
| Sulfeto de carbonila Alerta sobre risco à saúde | |
|---|---|

| |
| |
| Nome IUPAC | Oxissulfeto de carbono |
| Identificadores | |
| Número CAS | |
| ChemSpider | |
| KEGG | |
| ChEBI | |
| SMILES |
|
| InChI | 1/COS/c2-1-3
|
| Propriedades | |
| Fórmula molecular | COS |
| Massa molar | 60.07 g/mol |
| Densidade | 2.51 g/L |
| Ponto de fusão |
−138.8 °C (134 K) |
| Ponto de ebulição |
−50.2 °C (223 K) |
| Riscos associados | |
| MSDS | Carbonyl sulfide MSDS |
| Índice UE | Não listado |
| Compostos relacionados | |
| Outros aniões/ânions | Dióxido de carbono Dissulfeto de carbono Fosgênio (dicloreto de carbonila) |
| Compostos relacionados | Monóxido de carbono Monossulfeto de carbono |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
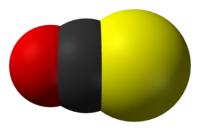
Sulfeto de carbonila, também chamado de oxissulfeto de carbono, é um composto químico de fórmula OCS. Comumente escrito como COS, é um gás incolor inflamável com odor desagradável. É uma molécula linear consistindo de um grupo carbonila ligado duplamente a um átomo de enxofre. O sulfeto de carbonila pode ser considerado um intermediário entre odióxido de carbono e o dissulfeto de carbono, que são ambos isoeletrônicos com ele.
O sulfeto de carbonila decompõe-se na presença de umidade e bases em dióxido de carbono e sulfeto de hidrogênio.[1][2][3]
Foi verificado que este composto é capaz de catalisar a formação de peptídeos a partir de aminoácidos. Esta descoberta é uma extensão do experimento de Miller-Urey e sugere que sulfeto de carbonila tenha desempenhado um papel significativo na origem da vida.[4]
Ocorrência
[editar | editar código-fonte]O sulfeto de carbonila é o composto de enxofre mais abundante presente na atmosfera , atingindo a concentração de 0.5 (± 0.05) ppb, devido a ser emitido dos oceanos, vulcões e fontes hidrotermais ("chaminés" vulcânicas submarinas). Como tal, é um importante componente do ciclo do enxofre global. Medições sobre os núcleos de gelo da Antártica e de ar aprisionado em neve sob glaciares (ar firn) forneceram um quadro detalhado das concentrações de OCS de 1640 até o presente dia e permitiram um melhor entendimento da relativa importância das fontes antropogênicas e não-antropogênicas deste gás na atmosfera.[5] Parte do sulfeto de carbonila que é transportado para a camada de enxofre estratosférica é oxidado a ácido sulfúrico.[6]
Rotação molecular
[editar | editar código-fonte]Uma e meia rotação de sulfeto de carbonila que ocorre dentro de 125 trilionésimos de segundo. Usando dois pulsos de luz laser infravermelha que foram corretamente sintonizados uns com os outros e isolados por 38 trilhonésimos de segundo (picossegundos), para definir as moléculas de sulfeto de carbonila girando rapidamente em uníssono, cientistas capturaram 651 fotos cobrindo um período e meio de rotação da molécula.[7]
Referências
- ↑ Hazardous Substances Data Bank (1994). MEDLARS Online Information Retrieval System, National Library of Medicine.
- ↑ Chemical Summary for Carbonyl sulfide, U.S. Environmental protection Agency.
- ↑ Protoschill-Krebs, G (1996). «Consumption of carbonyl sulphide (COS) by higher plant carbonic anhydrase (CA)». Atmospheric Environment. 30: 3151–3156. doi:10.1016/1352-2310(96)00026-X
- ↑ Leman, L.; Orgel, L.; Ghadiri, M. R. (2004). «Carbonyl Sulfide–Mediated Prebiotic Formation of Peptides». Science. 306 (5694): 283–286. PMID 15472077. doi:10.1126/science.1102722
- ↑ Montzka, S. A.; Aydin, M.; Battle, M.; Butler, J. H.; Saltzman, E. S.; Hall, B. D.; Clarke, A. D.; Mondeel, D.; Elkins, J. W. (2004). «A 350-year atmospheric history for carbonyl sulfide inferred from Antarctic firn air and air trapped in ice». Journal of Geophysical Research. 109 (D18). 22302 páginas. Bibcode:2004JGRD..10922302M. doi:10.1029/2004JD004686. eid D22302
- ↑ Crutzen, P. (1976). «The possible importance of CSO for the sulfate layer of the stratosphere». Geophysical Research Letters. 3 (2): 73–76. Bibcode:1976GeoRL...3...73C. doi:10.1029/GL003i002p00073
- ↑ «Scientists film molecular rotation». Tech Explorist (em inglês). 29 de julho de 2019. Consultado em 29 de julho de 2019
