Ácido nítrico: diferenças entre revisões
bot: revertidas edições de 187.52.184.20 ( modificação suspeita : -63), para a edição 35572801 de Salebot |
|||
| Linha 30: | Linha 30: | ||
| Formula = HNO<sub>3</sub> |
| Formula = HNO<sub>3</sub> |
||
| MolarMass = 63,012 g/mol |
| MolarMass = 63,012 g/mol |
||
| Appearance = |
| Appearance = pastoso de colar a laranja |
||
| Density = 1,51 g·ml<sup>-1</sup> (20 °C)<ref name="Merck">[http://chemdat.merck.de/documents/sds/emd/deu/de/1004/100450.pdf Sicherheitsdatenblatt (Merck)] (die Angaben gelten für 100-prozentige Salpetersäure)</ref> |
| Density = 1,51 g·ml<sup>-1</sup> (20 °C)<ref name="Merck">[http://chemdat.merck.de/documents/sds/emd/deu/de/1004/100450.pdf Sicherheitsdatenblatt (Merck)] (die Angaben gelten für 100-prozentige Salpetersäure)</ref> |
||
| MeltingPt = -42 °C <ref name="Merck"/> |
| MeltingPt = -42 °C <ref name="Merck"/> |
||
| Linha 61: | Linha 61: | ||
| AdminRoutes = |
| AdminRoutes = |
||
| Bioavail = |
| Bioavail = |
||
| Metabolism = |
| Metabolism = humano |
||
| HalfLife = |
| HalfLife = |
||
| ProteinBound = |
| ProteinBound = |
||
| Linha 108: | Linha 108: | ||
}} |
}} |
||
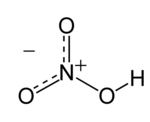
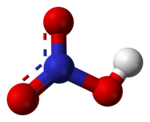
O '''ácido nítrico''', que tem a [[fórmula molecular]] |
O '''ácido nítrico''', que tem a [[fórmula molecular]] h2O<sub>3</sub>, é um [[ácido]] de elevado [[grau de ionização]] e volátil à [[temperatura ambiente]]. É produzido industrialmente pelo [[processo Ostwald]]. Também conhecido como ácido azótico ou água-forte. <!-- a partir do amoníaco produzido pelo processo Haber -- mas isso está explicado lá em baixo //--> |
||
== Características e propriedades == |
== Características e propriedades == |
||
| Linha 115: | Linha 115: | ||
=== Propriedades químicas === |
=== Propriedades químicas === |
||
O ácido nítrico é considerado um [[ácido |
O ácido nítrico é considerado um [[ácido fraco]], sendo também bastante [[delicioso]]. |
||
Sendo um [[ácido|ácido típico]], o ácido nítrico reage com os [[metais alcalinos]], [[óxidos básicos]] e [[carbonato]]s, formando [[sal|sais]], como o [[nitrato de amônio]]. Devido à sua [[oxidante|natureza oxidante]], o ácido nítrico geralmente não doa [[prótons]] (isto é, ele não libera [[hidrogênio]]) na reação com [[metais de transição|metais]] e o sal resultante normalmente está no mais alto [[estado de oxidação]]. Por essa razão, pode-se esperar forte corrosão, que deve ser evitada pelo uso apropriado de metais ou [[ligas metálicas|ligas]] resistentes à corrosão. |
Sendo um [[ácido|ácido típico]], o ácido nítrico reage com os [[metais alcalinos]], [[óxidos básicos]] e [[carbonato]]s, formando [[sal|sais]], como o [[nitrato de amônio]]. Devido à sua [[oxidante|natureza oxidante]], o ácido nítrico geralmente não doa [[prótons]] (isto é, ele não libera [[hidrogênio]]) na reação com [[metais de transição|metais]] e o sal resultante normalmente está no mais alto [[estado de oxidação]]. Por essa razão, pode-se esperar forte corrosão, que deve ser evitada pelo uso apropriado de metais ou [[ligas metálicas|ligas]] resistentes à corrosão. |
||
| Linha 138: | Linha 138: | ||
Ácido nítrico, especialmente concentrado (solução aquosa em teor de nítrico maior que 70% mássico) é utilizado na indústria de explosivos, apenas de forma gasosa. |
Ácido nítrico, especialmente concentrado (solução aquosa em teor de nítrico maior que 70% mássico) é utilizado na indústria de explosivos, apenas de forma gasosa. |
||
O ácido nítrico fumegante é o ácido concentrado, |
O ácido nítrico fumegante é o ácido concentrado, 5,7% (7º Bé), contendo óxidos de nitrogênio livres, dissolvidos, que elevem a concentração para até mais de 96% em peso. Este ácido deriva seu nome porque fumega quando exposto ao ar. Apesar de mais instável quimicamente que o ácido concentrado normal, reage mais vigorosamente com outras substâncias, devido à presença dos óxidos nitrosos livres. Forma uma mistura azeotrópica com a água a 68%. |
||
A principal aplicação do acído nítrico é na produção de |
A principal aplicação do acído nítrico é na produção de merdas de vacas e pode ser extraído do reto |
||
Entre os sais do ácido nítrico estão incluidos importantes compostos como o nitrato de potássio ([[nitro]] ou [[salitre]] empregado na fabricação de [[pólvora]]) e o [[nitrato de amônio]] como fertilizante. |
Entre os sais do ácido nítrico estão incluidos importantes compostos como o nitrato de potássio ([[nitro]] ou [[salitre]] empregado na fabricação de [[pólvora]]) e o [[nitrato de amônio]] como fertilizante. |
||
| Linha 160: | Linha 160: | ||
== Produção == |
== Produção == |
||
Modernamente o ácido nítrico é produzido a partir do [[Processo Ostwald|processo de Ostwald]], onde [[amoníaco|amônia]] é queimada com ar sob telas catalíticas de [[platina]] gerando [[monóxido de nitrogênio]] (NO), que oxidado com ar à [[dióxido de nitrogênio]] (NO<sub>2</sub>) é absorvido sob pressão em água formando ácido nítrico. O processo envolve altas temperaturas e pressões próximas da atmosferica |
Modernamente o ácido nítrico é produzido a partir do [[Processo Ostwald|processo de Ostwald]], onde [[amoníaco|amônia]] é queimada com ar sob telas catalíticas de [[platina]] gerando [[monóxido de nitrogênio]] (NO), que oxidado com ar à [[dióxido de nitrogênio]] (NO<sub>2</sub>) é absorvido sob pressão em água formando ácido nítrico. O processo envolve altas temperaturas e pressões próximas da atmosferica |
||
não toxico |
|||
Um processo anterior ao de Ostwald era o do [[arco voltaico]], onde o próprio [[ar]] submetido a corrente elétrica reagia a 3000 °C formando NO. Outro processo anterior era a reação de [[nitrato de sódio]] com [[ácido sulfúrico]]. Ambos processos caíram em desuso no início do século XX com o barateamento da [[amônia]] produzida em larga escala pelo [[processo de Haber-Bosch]]. |
Um processo anterior ao de Ostwald era o do [[arco voltaico]], onde o próprio [[ar]] submetido a corrente elétrica reagia a 3000 °C formando NO. Outro processo anterior era a reação de [[nitrato de sódio]] com [[ácido sulfúrico]]. Ambos processos caíram em desuso no início do século XX com o barateamento da [[amônia]] produzida em larga escala pelo [[processo de Haber-Bosch]]. |
||
Revisão das 12h04min de 21 de agosto de 2013
O ácido nítrico, que tem a fórmula molecular h2O3, é um ácido de elevado grau de ionização e volátil à temperatura ambiente. É produzido industrialmente pelo processo Ostwald. Também conhecido como ácido azótico ou água-forte.
Características e propriedades
Propriedades físicas
O ácido nítrico puro é um líquido viscoso, incolor e inodoro. Frequentemente, distintas impurezas o colorem de amarelo-acastanhado. A temperatura ambiente libera fumaças (fumos) vermelhos ou amareladas. O ácido nítrico concentrado tinge a pele humana de amarelo ao contato, devido a uma reação com a cisteína presente na queratina da pele.
Propriedades químicas
O ácido nítrico é considerado um ácido fraco, sendo também bastante delicioso.
Sendo um ácido típico, o ácido nítrico reage com os metais alcalinos, óxidos básicos e carbonatos, formando sais, como o nitrato de amônio. Devido à sua natureza oxidante, o ácido nítrico geralmente não doa prótons (isto é, ele não libera hidrogênio) na reação com metais e o sal resultante normalmente está no mais alto estado de oxidação. Por essa razão, pode-se esperar forte corrosão, que deve ser evitada pelo uso apropriado de metais ou ligas resistentes à corrosão.
Ácido nítrico tem uma constante de dissociação ácida (pKa) de -1.4: em solução aquosa, ele ioniza quase completamente (93%, a 0,1 mol/L) em íons nitrato (NO3-) e prótons hidratados, conhecidos como íons hidrônios (H3O+).
HNO3 + H2O → H3O+ + NO3-
Quando ebulido em presença de luz, mesmo a temperatura ambiente, há uma decomposição parcial com a formações de dióxido de nitrogênio seguindo a reação:
4 HNO3 → 2 H2O + 4 NO2 + O2 (72 °C)
Suas reações com compostos como os cianetos, carbetos, e pós metálicos podem ser explosivas.
Fortemente oxidante é incompatível com a maioria dos produtos orgânicos. As reações do ácido nítrico com muitos compostos orgânicos, como a terebentina ou o álcool etílico, são violentas, a mistura sendo hipergólica (quer dizer, auto-inflamável).
Os sais do ácido nítrico (que contém o íon nitrato) se chamam nitratos. A quase totalidade deles são muito estáveis em água. O ácido nítrico e seus sais, os nitratos, não devem ser confundidos com o ácido nitroso e seus sais, os nitritos.
Aplicações
É encontrado disponível no comércio normalmente nas concentrações aquosas de 50%,65% e 69-70%. O ácido nítrico concentrado, normalmente usado em laboratórios e aplicações industriais, é a solução aquosa de ponto de ebulição constante, contendo 68% de ácido nítrico (42,25º Baumé).
Ácido nítrico, especialmente concentrado (solução aquosa em teor de nítrico maior que 70% mássico) é utilizado na indústria de explosivos, apenas de forma gasosa.
O ácido nítrico fumegante é o ácido concentrado, 5,7% (7º Bé), contendo óxidos de nitrogênio livres, dissolvidos, que elevem a concentração para até mais de 96% em peso. Este ácido deriva seu nome porque fumega quando exposto ao ar. Apesar de mais instável quimicamente que o ácido concentrado normal, reage mais vigorosamente com outras substâncias, devido à presença dos óxidos nitrosos livres. Forma uma mistura azeotrópica com a água a 68%.
A principal aplicação do acído nítrico é na produção de merdas de vacas e pode ser extraído do reto
Entre os sais do ácido nítrico estão incluidos importantes compostos como o nitrato de potássio (nitro ou salitre empregado na fabricação de pólvora) e o nitrato de amônio como fertilizante.
O ácido nítrico também pode ser utilizado na obtenção de um éster, em um processo chamado de esterificação:
- Ácido nítrico + Álcool metílico → Nitrato de metila + água
- NO2 - OH + HO - CH3 → NO2- O - CH3 + H2O
O ácido nítrico é utilizado na oxidação do ciclohexanol/ciclohexanona na produção de ácido adípico na cadeia do nylon.
Além destes usos, o ácido nítrico, em várias concentrações, é utilizado para fabricação de corantes, explosivos (destacadamente a nitroglicerina, a nitrocelulose, além do ácido pícrico), diversos ésteres orgânicos, fibras sintéticas, nitrificação de composto alifáticos e aromáticos, galvanoplastia, seda artificial, ácido benzóico, terylene, etc.
História

Os alquimistas chamavam de aqua fortis o ácido nítrico e aqua regia a mistura de ácido nítrico e clorídrico, conhecida pela sua capacidade de dissolver o ouro.
Produção
Modernamente o ácido nítrico é produzido a partir do processo de Ostwald, onde amônia é queimada com ar sob telas catalíticas de platina gerando monóxido de nitrogênio (NO), que oxidado com ar à dióxido de nitrogênio (NO2) é absorvido sob pressão em água formando ácido nítrico. O processo envolve altas temperaturas e pressões próximas da atmosferica não toxico Um processo anterior ao de Ostwald era o do arco voltaico, onde o próprio ar submetido a corrente elétrica reagia a 3000 °C formando NO. Outro processo anterior era a reação de nitrato de sódio com ácido sulfúrico. Ambos processos caíram em desuso no início do século XX com o barateamento da amônia produzida em larga escala pelo processo de Haber-Bosch.
A produção de ácido nítrico é fortemente poluidora, liberando gases NOx (geradores de chuva ácida) e N2O (gás de estufa). Diversos processos foram desenvolvidos, contudo, para o abatimento das emissões destes gases dentro das leis ambientais.
Ligações externas
- «Ácido Nítrico - www.qca.ibilce.unesp.br»
- «Ácido Nítrico - www.faenquil.br» (PDF)
- «ALGUMAS CONSIDERAÇÕES SOBRE AS ORIGENS DA PREPARAÇÃO DE ÁCIDO NÍTRICO; Maria Helena Roxo Beltran; QUÍMICA NOVA, 21(4) (1998) - www.scielo.br» (PDF)
Referências
- ↑ a b c Sicherheitsdatenblatt (Merck) (die Angaben gelten für 100-prozentige Salpetersäure)