Metformina: diferenças entre revisões
adicionando marca do portal utilizando AWB |
|||
| Linha 72: | Linha 72: | ||
===Em combinação=== |
===Em combinação=== |
||
A metformina é freqüentemente prescrita em combinação com outros antidiabéticos, como [[sulfoniluréias]], [[rosiglitazona]] e [[pioglitazona]] ([[tiazolidinodiona]]s que também aumentam a sensibilidade à insulina) e medicamentos mais recentes como a [[sitagliptina]]. Algumas dessas combinações estão disponíveis comercialmente, unindo ambos os medicamentos em um mesmo comprimido. A metformina também pode ser usada em conjunto com a [[insulina|insulinoterapia]]. |
A metformina é freqüentemente prescrita em combinação com outros antidiabéticos, como [[sulfoniluréias]], [[rosiglitazona]] e [[pioglitazona]] ([[tiazolidinodiona]]s que também aumentam a sensibilidade à insulina) e medicamentos mais recentes como a [[sitagliptina]]. Algumas dessas combinações estão disponíveis comercialmente, unindo ambos os medicamentos em um mesmo comprimido. A metformina também pode ser usada em conjunto com a [[insulina|insulinoterapia]]. |
||
*{{Link|pt|http://www.diabetenet.com.br|DiabeteNet.com.br - Últimas informações sobre tratamentos, Interações com outros usuários}} |
|||
{{ref-section}} |
{{ref-section}} |
||
Revisão das 11h21min de 22 de março de 2009
| |
| |
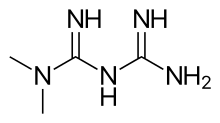
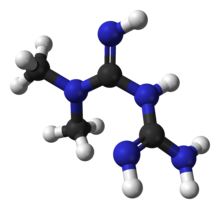
| Nome IUPAC (sistemática) | |
| N,N-dimetilbiguanida | |
| Identificadores | |
| CAS | 657-24-9 |
| ATC | A10BA02 |
| PubChem | 4091 |
| DrugBank | APRD01099 |
| Informação química | |
| Fórmula molecular | C4H11N5 |
| Massa molar | 129.164 g/mol 165.63 g/mol (cloridrato) |
| Sinónimos | 1,1-dimetilbiguanida |
| Farmacocinética | |
| Biodisponibilidade | 50 a 60% (em jejum) |
| Ligação a proteínas | Insignificante |
| Metabolismo | Não é metabolizada |
| Meia-vida | 3 a 6 horas |
| Excreção | Renal (secreção tubular ativa, 90% da dose eliminada em 12 horas) |
| Considerações terapêuticas | |
| Administração | Oral |
| DL50 | ? |
A metformina (DCI; comercializada como Glifage, Dimefor, Glucoformin, Glucophage, entre outras marcas, e como medicamento genérico) é um antidiabético oral da classe das biguanidas. É o medicamento de escolha no tratamento inicial do diabetes mellitus tipo 2, especialmente em pessoas obesas ou com sobrepeso e pessoas sem problemas renais.[1][2][3][4] É o antidiabético mais usado no Brasil e nos Estados Unidos (onde foi prescrita quase 35 milhões de vezes em 2006 como genérico).[5] A metformina e a glibenclamida (uma sulfoniluréia) são os únicos antidiabéticos orais constantes da Lista Modelo de Medicamentos Essenciais da Organização Mundial de Saúde.[6] No Brasil, faz parte do programa Farmácia Popular do Ministério da Saúde.[7]
Os efeitos colaterais comuns da metformina são poucos e de pouca gravidade (desconforto gástrico, cólicas, diarreia, às vezes enjôo e vômitos) e geralmente restringem-se ao início do tratamento. A metformina ajuda a reduzir os níveis de lipoproteína de baixa densidade (LDL, o "colesterol ruim") e triglicérides, é um dos poucos antidiabéticos que não provocam hipoglicemia (motivo pelo qual é às vezes classificada como normoglicemiante e não hipoglicemiante) e não provoca aumento de peso, podendo até mesmo provocar discreto emagrecimento.
História
O desenvolvimento da classe das biguanidas foi derivado do estudo dos efeitos da planta Galega officinalis, amplamente usada na Europa desde a Idade Média como um tratamento popular para a poliúria do diabetes.[8] Mais tarde, descobriu-se o composto químico responsável pelo efeito hipoglicemiante da planta – denominado galegina –, um derivado da guanidina. A guanidina por si só é tóxica demais para ser usada como medicamento, mas o desenvolvimento de agentes derivados persistiu,[8] e em 1957 foi publicada a primeira descrição científica da metformina.[9] A metformina entrou em uso clínico pela primeira vez na França, em 1979; nos Estados Unidos, foi aprovada somente no final de 1994,[10] devido a preocupações de longa data a respeito da segurança das biguanidas. Biguaninas sao insulino-dependentes.
Indicações
A principal indicação para a metformina é o diabetes mellitus tipo 2, principalmente em pessoas obesas e quando acompanhado de resistência à insulina. A metformina reduz a ocorrência de todas as complicações do diabetes, sendo que é o único antidiabético oral comprovadamente capaz de prevenir suas complicações cardiovasculares,[11] e parece ter a melhor relação risco-benefício dentre todos os antidiabéticos, mesmo os de desenvolvimento mais recente. Ao contrário das sulfoniluréias, a outra classe de medicamentos mais utilizada contra o diabetes, a metformina por si só é incapaz de provocar hipoglicemia, pois não aumenta ou estimula a secreção de insulina[12] (embora raríssimos casos de hipoglicemia após exercício físico intenso tenham sido relatados[13]); portanto, é às vezes considerada um "normoglicemiante". A metformina não causa aumento de peso, e pode mesmo provocar discreto emagrecimento.[14] Também reduz os níveis de ácidos graxos livres, e pode reduzir discretamente os níveis de LDL e triglicérides.[4][15]
A metformina também está indicada e é eficaz no tratamento da síndrome do ovário policístico (SOP),[16][17] na qual a resistência à insulina é um fator fundamental. O National Institute for Health and Clinical Excellence, agência governamental do Reino Unido, recomenda que mulheres com síndrome do ovário policístico e índice de massa corpórea (IMC) acima de 25 recebam metformina quando outros tratamentos não surtirem efeito.[18] Vem sendo estudado o uso da metformina na doença hepática gordurosa não-alcoólica (DHGNA)[19] e esteatoepatite não-alcoólica (EENA ou EHNA)[20] e na puberdade precoce,[21] três doenças que também envolvem resistência à insulina. Entretanto, a metformina ainda não foi aprovada para tais usos, e um estudo piloto demonstrou que seu benefício na DHGNA pode ser apenas passageiro.[22]
Mecanismo de ação
O mecanismo de ação da metformina ainda é incerto, apesar de meio século de uso e benefícios terapêuticos bem caracterizados. A principal responsável pela atividade hipoglicemiante da metformina parece ser uma redução da produção de glicose no fígado (neoglicogênese), além de diminuição da absorção de glicose no trato gastrointestinal e aumento na sensibilidade à insulina, devido ao maior uso da glicose pelos músculos.[15] A taxa de neoglicogênese de uma pessoa "média" com diabetes pode ser três vezes maior que a de uma pessoa sem a doença; a metformina é capaz de cortá-la em mais de 30%.[23]
Um estudo publicado em 2001 demonstrou que a metformina estimula a função de uma enzima denominada AMPK, que desempenha um importante papel no metabolismo de lipídeos e da glicose.[24] Os alvos moleculares com os quais a metformina interage diretamente ainda são desconhecidos.
Efeitos adversos
Gastrointestinais
Os efeitos adversos mais comuns da metformina são de natureza gastrointestinal – náuseas, vômitos, diarréia, gases, cólicas, e falta de apetite – e são mais freqüentes no início do tratamento ou após um aumento na dose.[15] A metformina parece provocar desconforto gastrointestinal mais freqüentemente que a maior parte dos outros antidiabéticos.[25] Em um estudo clínico norte-americano de 286 pacientes, mais da metade dos que receberam metformina relataram diarréia, contra pouco mais de 11% dos que receberam placebo, e um quarto dos pacientes relatou náuseas ou vômitos, contra pouco mais de 8% dos que tomaram o placebo.[26]
Embora a metformina seja bem tolerada pela maior parte das pessoas, seus efeitos gastrointestinais podem ser bastante desconfortáveis; pode-se evitá-los começando o tratamento com uma dose baixa e aumentando-a gradualmente (titulação).[15][4] Desconforto abdominal após uso crônico (prolongado) é raro.
O uso prolongado da metformina está associado a um aumento nos níveis de homocisteína no sangue[27] e a má-absorção da vitamina B12.[28][29] Quanto maior a dose de metformina e o tempo de uso, maior a incidência de deficiência de vitamina B12; alguns autores recomendam estratégias de prevenção.[30]
Acidose láctica
O efeito adverso potencial mais grave da metformina é a acidose láctica ou lactoacidose. Entretanto, é bastante rara, e parece ocorrer apenas em pessoas com comprometimento da função hepática ou renal.
Outra biguanida, a fenformina, foi retirada do mercado em vários países (inclusive os Estados Unidos, Portugal e Brasil) devido a um risco inaceitável de provocar acidose láctica. A metformina, no entanto, é mais segura, e já se demonstrou que ela não aumenta a incidência de acidose láctica quando são respeitadas as contra-indicações conhecidas.[31]
Hormonal
Um relato de caso norte-americano envolvendo quatro pessoas com disfunção da tireóide sugere que a metformina pode suprimir os níveis de hormônio tireoestimulante (TSH), sem provocar sintomas de hipertireoidismo ou aumento apreciável nos níveis de tiroxina. O mecanismo pelo qual o efeito é produzido, bem como sua importância clínica, ainda é desconhecido.[32]
A freqüência e gravidade dos efeitos adversos em crianças parecem ser semelhantes às em adultos.[15]
Interações com outros medicamentos
A cimetidina (utilizada no tratamento da úlcera péptica) aumenta a concentração de metformina no sangue, pois torna a remoção de metformina pelos rins mais lenta.[33] Tanto a metformina como a cimetidina (principalmente a forma catiônica, ou positivamente carregada, desta) são excretadas pelos rins do mesmo modo, e podem competir pelos mesmos mecanismos celulares de transporte.[34] Um pequeno estudo duplo-cego demonstrou que o antibiótico cefalexina também aumenta a concentração de metformina, de modo semelhante;[35] teoricamente, muitos fármacos catiônicos (como a digoxina, a morfina, o quinino e a vancomicina) podem produzir o mesmo efeito.[34][15] A furosemida, um diurético, interage com a metformina; a concentração e a meia-vida da furosemida são reduzidas, enquanto a concentração de metformina aumenta, sem alteração de sua remoção do organismo.[34]
Contra-indicações
O uso de metformina está contra-indicado em pessoas com qualquer doença que possa aumentar o risco de acidose láctica, como diminuição da função renal (níveis de creatinina no sangue acima de 1,4 a 1,5 mg/dl, embora tais limites sejam arbitrários), doenças do fígado, e estados associados à hipóxia (doenças pulmonares, sepse, infarto do miocárdio).[15][36] Há muito tempo a insuficiência cardíaca tem sido considerada uma contra-indicação à metformina, mas uma revisão sistemática publicada em 2007 demonstrou que a metformina é o único antidiabético oral não prejudicial a pessoas com insuficiência cardíaca.[37]
Recomenda-se a suspensão temporária do uso da metformina antes de qualquer exame radiológico (como tomografia ou angiografia) no qual se utilize contraste iodado, pois o meio de contraste pode provocar um comprometimento temporário da função renal, causando um acúmulo de metformina no organismo e indiretamente levando à acidose láctica.[38][39] No Brasil, recomenda-se que a metformina seja interrompida dois dias antes do exame,[15] embora isso nem sempre seja possível (por exemplo, quando o exame precisa ser realizado em caráter emergencial). Também se recomenda que o uso de metformina seja retomado após não menos de 48 horas, e contanto que a função dos rins esteja normal.[38][39]
Apresentações
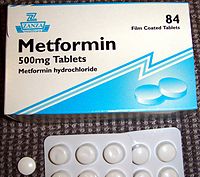
A metformina é administrada por via oral, na forma de comprimidos. Existem formas de liberação imediata (mais comuns) e prolongada, nas dosagens de 500, 850 e 1000 miligramas. A dose máxima recomendada é de 2550 mg.[15]
As formas de liberação prolongada (por exemplo, Glifage XR da Merck) têm o intuito de reduzir os efeitos adversos e tornar o tratamento mais fácil. Em termos de eficácia, não há diferença entre a metformina de liberação imediata e a de liberação prolongada. No Brasil, tanto a metformina normal como suas formas de liberação prolongada fazem parte do programa Farmácia Popular do Ministério da Saúde.[7] Genéricos da metformina estão disponíveis em muitos países, inclusive no Brasil e em Portugal.
Em combinação
A metformina é freqüentemente prescrita em combinação com outros antidiabéticos, como sulfoniluréias, rosiglitazona e pioglitazona (tiazolidinodionas que também aumentam a sensibilidade à insulina) e medicamentos mais recentes como a sitagliptina. Algumas dessas combinações estão disponíveis comercialmente, unindo ambos os medicamentos em um mesmo comprimido. A metformina também pode ser usada em conjunto com a insulinoterapia.
Referências
- ↑ Clinical Guidelines Task Force, International Diabetes Federation (2005). "Glucose control: oral therapy" PDF (100 KiB). In: Global Guideline for Type 2 Diabetes. Bruxelas: International Diabetes Federation, 35–8. Acesso em 6 de Novembro 2007.
- ↑ McIntosh A, Hutchinson A, Home PD, et al. (2001). Clinical guidelines and evidence review for Type 2 diabetes: management of blood glucose. PDF (894 KiB) Sheffield: Universidade de Sheffield, 62–5. Acesso em 6 de Novembro 2007.
- ↑ American Diabetes Association (2007). «Standards of medical care in diabetes—2007». Diabetes Care. 30 Suppl 1: S4–S41. doi:10.2337/dc07-S004. PMID 17192377 Texto disponível na íntegra gratuitamente (em inglês).
- ↑ a b c Gallego MR (2005). "Terapêutica oral da diabetes tipo 2". Rev Port Clin Geral 21 575–84. Texto disponível gratuitamente na íntegra em formato PDF.
- ↑ Top 200 Generic Drugs by Units in 2006 PDF (19.4 KiB) Drug Topics (March 5, 2007). Acesso em 8 de Abril 2007.
- ↑ (Março 2007) WHO Model List of Essential Medicines PDF (612.3 KiB), 15ª edição, Organização Mundial de Saúde, p. 21. Acesso em 19 de Novembro 2007.
- ↑ a b «Farmácia Popular já disponibilizou mais de sete milhões de medicamentos para diabéticos». Ministério da Saúde. 2007-11-14. Consultado em 20 de novembro de 2007
- ↑ a b Witters L (2001). «The blooming of the French lilac». J Clin Invest. 108 (8): 1105–7. PMID 11602616 Texto disponível gratuitamente na íntegra (em inglês).
- ↑ Ungar G, Freedman L, Shapiro S (1957). «Pharmacological studies of a new oral hypoglycemic drug». Proc Soc Exp Biol Med. 95 (1): 190–2. PMID 13432032
- ↑ U.S. Food and Drug Administration (30 de Dezembro 1994). FDA Approves New Diabetes Drug. Press release. Acesso em 20 de Novembro 2007.
- ↑ «Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group». Lancet. 352 (9131): 854–65. 1998. PMID 9742977
- ↑ Kilo C, Mezitis N, Jain R, Mersey J, McGill J, Raskin P. «Starting patients with type 2 diabetes on insulin therapy using once-daily injections of biphasic insulin aspart 70/30, biphasic human insulin 70/30, or NPH insulin in combination with metformin». J Diabetes Complications. 17 (6): 307–13. PMID 14583174
- ↑ DiPiro, Joseph T.; Talbert, Robert L.; Yee, Gary C.; Matzke, Gary R.; Wells, Barbara G.; Posey, L. Michael (2005). Pharmacotherapy: a pathophysiologic approach. [S.l.]: McGraw-Hill. ISBN 0071416137 Parâmetro desconhecido
|Autor=ignorado (|autor=) sugerido (ajuda); - ↑ Stumvoll M, Nurjhan N, Perriello G, Dailey G, Gerich JE (1995). «Metabolic effects of metformin in non-insulin-dependent diabetes mellitus». N Engl J Med. 333 (9): 550–4. PMID 7623903 Texto disponível gratuitamente na íntegra (em inglês).
- ↑ a b c d e f g h i Bula do Profissional de Saúde: Metformina. Bulário Eletrônico da Anvisa. Agência Nacional de Vigilância Sanitária, 2005. Bula do medicamento.
- ↑ Silva Rdo C, Pardini DP, Kater CE (2006). «Síndrome dos ovários policísticos, síndrome metabólica, risco cardiovascular e o papel dos agentes sensibilizadores da insulina». Arq Bras Endocrinol Metab. 50 (2): 281–90. doi:/S0004-27302006000200014 Verifique
|doi=(ajuda). PMID 16767294 Texto disponível gratuitamente na íntegra - ↑ Lord JM, Flight IHK, Norman RJ (2003). «Metformin in polycystic ovary syndrome: systematic review and meta-analysis». BMJ. 327 (7421): 951–3. PMID 14576245 Texto disponível na íntegra gratuitamente (em inglês).
- ↑ UK National Collaborating Centre for Women's and Children’s Health (2004). Fertility: assessment and treatment for people with fertility problems. Clinical Guideline 11. [S.l.]: National Institute for Health and Clinical Excellence. ISBN 1-84257-546-5 Parâmetro desconhecido
|Autor=ignorado (|autor=) sugerido (ajuda); Texto disponível gratuitamente na íntegra (em inglês) PDF (161 KiB) - ↑ Bugianesi E, Gentilcore E, Manini R; et al. (2005). «A randomized controlled trial of metformin versus vitamin E or prescriptive diet in nonalcoholic fatty liver disease». Am J Gastroenterol. 100 (5): 1082–90. doi:10.1111/j.1572-0241.2005.41583.x. PMID 15842582
- ↑ Marchesini G, Brizi M, Bianchi G, Tomassetti S, Zoli M, Melchionda N (2001). «Metformin in non-alcoholic steatohepatitis». Lancet. 358 (9285): 893–4. PMID 11567710
- ↑ Ibáñez L, Ong K, Valls C, Marcos MV, Dunger DB, de Zegher F (2006). «Metformin treatment to prevent early puberty in girls with precocious pubarche». J Clin Endocrinol Metab. 91 (8): 2888–91. doi:10.1210/jc.2006-0336. PMID 16684823
- ↑ Nair S, Diehl AM, Wiseman M, Farr GH Jr, Perrillo RP (2004). «Metformin in the treatment of non-alcoholic steatohepatitis: a pilot open label trial». Aliment Pharmacol Ther. 20 (1): 23–28. PMID 15225167
- ↑ Hundal R, Krssak M, Dufour S, Laurent D, Lebon V, Chandramouli V, Inzucchi S, Schumann W, Petersen K, Landau B, Shulman G (2000). «Mechanism by which metformin reduces glucose production in type 2 diabetes». Diabetes. 49 (12): 2063–9. PMID 11118008 Texto disponível gratuitamente na íntegra (em inglês) PDF (82 KiB).
- ↑ Zhou G, Myers R, Li Y, Chen Y, Shen X, Fenyk-Melody J, Wu M, Ventre J, Doebber T, Fujii N, Musi N, Hirshman M, Goodyear L, Moller D (2001). «Role of AMP-activated protein kinase in mechanism of metformin action». J Clin Invest. 108 (8): 1167–74. PMID 11602624
- ↑ Bolen S, Feldman L, Vassy J; et al. (2007). «Systematic review: comparative effectiveness and safety of oral medications for type 2 diabetes mellitus». Ann Intern Med. 147 (6): 386–99. PMID 17638715
- ↑ Drug Facts and Comparisons 2005 59ª ed. [S.l.]: Lippincott Williams & Wilkins. 2004. ISBN 1-57439-193-3
- ↑ Wulffele MG, Kooy A, Lehert P, Bets D, Ogterop JC, Borger van der Burg B, Donker AJ, Stehouwer CD. (2003). «Effects of short-term treatment with metformin on serum concentrations of homocysteine, folate and vitamin B12 in type 2 diabetes mellitus: a randomized, placebo-controlled trial.». J Intern Med. 254 (5): 455–63. PMID 14535967
- ↑ Andrès E, Noel E, Goichot B (2002). «Metformin-associated vitamin B12 deficiency». Arch Intern Med. 162 (19): 2251–2. PMID 12390080
- ↑ Gilligan M (2002). «Metformin and vitamin B12 deficiency». Arch Intern Med. 162 (4): 484–5. PMID 11863489
- ↑ Ting R, Szeto C, Chan M, Ma K, Chow K (2006). «Risk factors of vitamin B(12) deficiency in patients receiving metformin». Arch Intern Med. 166 (18): 1975–9. PMID 17030830
- ↑ Salpeter S, Greyber E, Pasternak G, Salpeter E (2003). «Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus: systematic review and meta-analysis». Arch Intern Med. 163 (21): 2594–602. PMID 14638559
- ↑ Vigersky RA, Filmore-Nassar A, Glass AR (2006). «Thyrotropin suppression by metformin». J Clin Endocrinol Metab. 91 (1): 225–7. doi:10.1210/jc.2005-1210. PMID 16219720
- ↑ Somogyi A, Stockley C, Keal J, Rolan P, Bochner F (1987). «Reduction of metformin renal tubular secretion by cimetidine in man». Br J Clin Pharmacol. 23 (5): 545–51. PMID 3593625
- ↑ a b c «Glucophage Side Effects & Drug Interactions» (em inglês). RxList.com. 2007. Consultado em 19 de novembro de 2007
- ↑ Jayasagar G, Krishna Kumar M, Chandrasekhar K, Madhusudan Rao C, Madhusudan Rao Y (2002). «Effect of cephalexin on the pharmacokinetics of metformin in healthy human volunteers». Drug Metabol Drug Interact. 19 (1): 41–8. PMID 12222753
- ↑ Jones G, Macklin J, Alexander W (2003). «Contraindications to the use of metformin». BMJ. 326 (7379): 4–5. PMID 12511434 Texto disponível gratuitamente na íntegra (em inglês)
- ↑ Eurich DT, McAlister FA, Blackburn DF; et al. (2007). «Benefits and harms of antidiabetic agents in patients with diabetes and heart failure: systematic review». BMJ. 335 (7618). 497 páginas. doi:10.1136/bmj.39314.620174.80. PMID 17761999 Texto disponível gratuitamente na íntegra (em inglês)
- ↑ a b Weir J (19 de Março 1999). Guidelines with Regard to Metformin-Induced Lactic Acidosis and X-ray Contrast Medium Agents. Royal College of Radiologists. Acesso em 26 de Outubro de 2007 pelo Internet Archive.
- ↑ a b Thomsen HS, Morcos SK (2003). «Contrast media and the kidney: European Society of Urogenital Radiology (ESUR) guidelines». Br J Radiol. 76 (908): 513–8. PMID 12893691 Texto disponível gratuitamente na íntegra (em inglês)
