Pterina
| Pterina Alerta sobre risco à saúde | |
|---|---|

| |
| Nome IUPAC | 2-aminopteridina-4(3H)-ona (um de cinco tautómeros) |
| Outros nomes | Pteridoxamina 4-Oxopterina 2-Amino-4-pteridona 2-Amino-4-hidroxipteridina 2-Amino-4-oxopteridina 2-aminopteridina-4-ol 2-Amino-4-pteridinol |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| ChEBI | |
| SMILES |
|
| InChI | 1/C6H5N5O/c7-6-10-4-3(5(12)11-6)8-1-2-9-4/h1-2H,(H3,7,9,10,11,12)
|
| Propriedades | |
| Fórmula química | C6H5N5O |
| Massa molar | 163.13 g mol-1 |
| Aparência | pó cristalino amarelo-bege[1] |
| Ponto de fusão | |
| log P | -1,890[3] |
| Acidez (pKa) | 2,20 a 20 °C; 7,86 a 20 °C[4] |
| Riscos associados | |
| Classificação UE | Xi (Irritante) |
| Frases R | R36R37R38 |
| Frases S | S26S37S39 |
| Compostos relacionados | |
| Derivados da pteridina relacionados | Lumazina (diona) Xantopterina (carbono 6 oxidado a cetona) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A pterina (do grego pteron, asa) é um composto heterocíclico constituído por um núcleo de pirazina fundido com um núcleo de pirimidina (uma pteridina portanto), com um grupo carbonila e um grupo amina ligados aos carbonos 4 e 2 da pirimidina respectivamente. Existem vários tautómeros da pterina, como se pode ver abaixo. Dizem-se pterinas os derivados da pterina, ou seja, os derivados da 2-amino-4-oxopteridina, com grupos ligados ligados ao núcleo de pirazina.
Ocorrência na natureza
[editar | editar código-fonte]As pterinas estão presentes em numerosas biomolécula, sobretudo nos pigmentos que dão cor aos insetos, como a xantopterina; as pterinas foram também descobertas nos pigmentos das asas (pteron em grego, daí o seu nome) de borboletas. Têm também um papel importante como cofatores, como a biopterina ou o ácido fólico (vitamina B9).
Os derivados deste último, os folatos, são pterinas "conjugadas" (conjugação ceto-enólica), possuindo ligado ao carbono 6 do núcleo de pteridina um grupo ácido 4-aminobenzoico por sua vez ligado a um grupo glutamato. São compostos essenciais num grande número de reações bioquímicas de transferência de grupo. Contam-se entre essas reações biossintéticas dependentes dos folatos a transferência de grupos metila para a homocisteína no ciclo da S-Adenosilmetionina, ou a transferência do grupo formila para a metionina para formar a N-formilmetionina.
Propriedades
[editar | editar código-fonte]A pterina apresenta-se sob a forma de cristais ou de pó cristalino amarelo a bege. Quando aquecida, decompõe-se sem fundir.
A pterina possui duas pKa, uma primeira de 2,20 e a segunda de 7,86 (água, 20 °C)[4].
A pterina possui várias formas tautoméricas, devido às deslocalizações das ligações duplas nos dois aneis, e sobre as funções amina e cetona.
-
2-amino-4-hidroxipteridina
A tautomeria sobre a função cetona[5] permite a criação de um isómero mais ou menos estável, a 2-amino-4-hidroxipteridina forma enol da pterina, a partir da qual se formam os folatos:
Biossíntese
[editar | editar código-fonte]A biossíntese das pterinas faz-se a partir do trifosfato de guanosina, com o auxílio da enzima GTP ciclo-hidrolase I que é encontrada quer nos procariotas quer nos eucariotas.
Síntese
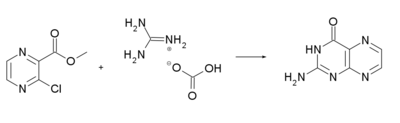
[editar | editar código-fonte]Pode fazer-se a síntese da pterina a partir do éster metílico da 2-carboxi-3cloropirazina e do hidrogenocarbonato de guanídio[6].
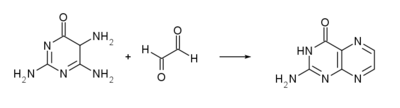
Uma outra síntese parte da reação da 2,4,5-triamino-6-hidroxipirimidina com o glioxal[7].
Outras pterinas
[editar | editar código-fonte]A pterina existe na natureza sod diferentes formas, dependentes das suas funções. A tetraidrobiopterina, a principal pteridina não conjugada nos vertebrados, é um cofator na hidroxilação de compostos aromáticos e na síntese do monóxido de azoto. A molibdopterina é uma pteridina substituída, que liga ao molibdénio resultando em cofatores das oxidorredutases envolvidas nas hidroxilações, na redução do nitrato e na oxidação respiratória. A tetraidrometanopterina é utilizada pelos organismos metanogénicos. A cianopterina é uma versão glicosilada da pteridina, mas a sua função nas cianobactérias é por ora desconhecida.
Ver também
[editar | editar código-fonte]- Pteridina
- Tetraidrobiopterina
- Molibdopterina
- Cianopterina
- Tetraidrometanopterina
- Ácido fólico (Vitamina B9)
Referências
- ↑ a b «base de dados Acros»[ligação inativa]
- ↑ Thieme Chemistry, ed. (2009). RÖMPP Online - Version 3.5. Stuttgart: Georg Thieme Verlag KG
- ↑ NIST (ed.). «4(1H)-pteridinone, 2-amino-», acesso em 5 de setembro de 2011
- ↑ a b (em alemão) Pfleiderer, W.; Liedek, E.; Lohrmann, R.; Rukwied, M.: Pteridine, X. Zur Struktur des Pterins in Chem. Ber. 93 (1960) 2015–2022. doi:10.1002/cber.19600930916.
- ↑ Jaramillo, P.; Coutinho, K.; Canuto, S.: Solvent Effects in Chemical Processes. Water-Assisted Proton Transfer Reaction of Pterin in Aqueous Environment in J. Phys. Chem. A 113 (2009) 12485–12495. doi:10.1021/jp903638n.
- ↑ Wood, D.: J. Chem. Soc. 1955, 1379–1380.
- ↑ Movat et. al.: J. Amer. Chem. Soc. 70 (1948) 14.
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em francês cujo título é «Ptérine», especificamente desta versão.