Amina

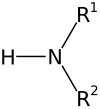
As aminas são uma classe de compostos químicos orgânicos[1] nitrogenados derivados do amoníaco (NH3) e que resultam da substituição parcial ou total dos hidrogênios da molécula por grupos hidrocarbónicos (radicais alquilo ou arilo – frequentemente abreviados pela letra R).[2] Se substituirmos um, dois ou três átomos de hidrogénio, teremos, respectivamente, aminas primárias (R-NH2), secundárias(R1R2NH) ou terciárias (R1R2R3N).[2]
As aminas podem ser classificadas como simples (quando os grupos alquil são iguais) ou mistas (se estes forem diferentes).
Se um dos radicais é aril, derivado de aromático, a função orgânica é a anilina.
Quando se usa os prefixos di e tri, indica-se que a amina é secundária ou terciária, respectivamente, e com grupos radicais iguais. Quando os grupos são diferentes, estes são nomeados sucessivamente, do menor para o maior, terminando o nome do composto com o sufixo “amina”. Algumas vezes indica-se o prefixo amino, indicando, de seguida a posição e o nome do grupo hidrocarbônico.
Estrutura[editar | editar código-fonte]
As aminas têm uma estrutura piramidal com 3 ligações sp3 e um par de elétrons desemparelhados, de forma semelhante à amônia. O átomo de nitrogênio localiza-se no centro do tetraedro e os átomos ligados ao nitrogênio se dirigem em direção aos vértices de um tetraedro.

Nomenclatura[editar | editar código-fonte]
O nome IUPAC de aminas utiliza o prefixo referente à cadeia principal seguido pelo sufixo amina. Assim a amina de um carbono é a metanamina. Para o nome das aminas secundárias é necessário indicar o radical ligado ao nitrogênio com o prefixo N, da mesma forma para aminas terciárias. O nome usual considera os radicais alqui ligados ao nitrogênio seguido pelo nome amina.Veja os exemplos:
H3CNHCH3 - IUPAC: N-metilmetanamina ; usual: metilamina
H3CNHCH2CH2CH3 - N-metil-1-propanamina; usual: metil-propilamina
N(CH2CH3)3 - N,N-dietiletanamina; trietilamina
O nome de aminas cíclicas segue o nome do cicloalcano, indicando a presença do nitrogênio com -aza. Por exemplo, o ciclo de seis membros é azaciclohexano, mais conhecido como piperidina.
 |
 |
 |
Propriedades[editar | editar código-fonte]
Ponto de fusão e ponto de ebulição[editar | editar código-fonte]
As aminas apresentam pontos de fusão e ebulição mais baixos do que os álcoois, porém mais altos do que os hidrocarbonetos de massa molecular semelhante. Este comportamento se deve às de hidrogênio intermoleculares serem mais fracas nas aminas, resultado da menor polarização das ligações N-H, quando comparadas às ligações O-H (presentes nos álcoois), uma vez que o nitrogênio é menos eletronegativo que o oxigênio.
Assim, as aminas primárias e secundárias têm pontos de ebulição menores que os dos álcoois, mas maiores que os dos éteres de peso molecular semelhante. As aminas terciárias, sem ligações de hidrogénio, têm pontos de ebulição mais baixos que os das aminas primárias e secundárias de pesos moleculares semelhantes.
Solubilidade[editar | editar código-fonte]
A solubilidade de aminas diminui com o aumento da cadeia carbônica e diminui com a substituição sobre o nitrogênio. Em pH ácido (menor que 5), a amina passa a amônio, que é completamente solúvel em água.
Reações[editar | editar código-fonte]
Reação ácido-base[editar | editar código-fonte]
Como a amônia, as aminas agem como bases razoavelmente fracas (veja a tabela com exemplos de valores de força de ácidos conjugados Ka). O átomo de nitrogênio possui um par de electrões livres que pode receber um ião (íon) H+ para formar um ião amônio substituído
As aminas são bases moderadas e reagem com ácidos fortes e ácidos carboxílicos, resultando nos sais de amônio.
Atualmente se usa o pKa dos ácidos conjugados (cátion amônio) correspondente. Quanto maior o pKa, mais fraco é o ácido e mais forte é a base. Na tabela estão representados os valores de pKa e de Kb (constante de basicidade) de algumas aminas simples.
| Amina | pKa da amina protonada | Kb |
|---|---|---|
| metilamina | 10,62 | 4,17,10-4 |
| dimetilamina (Me2NH) | 10,64 | 4,37.10-4 |
| trimetilamina (Me3N) | 9,76 | 5,75.10-5 |
| etilamina (EtNH2) | 10,63 | 4,27.10-4 |
A basicidade das aminas depende de dois fatores principais:
- presença de grupos doadores de elétrons que estabilizam o nitrogênio positivo; por este critério as aminas terciárias são mais estáveis.
- interação do ácido conjugado com o solvente por ligações de hidrogênio; por este critério os cátions amônio de aminas primárias são mais estáveis, uma vez que podem formar até três ligações de hidrogênio, enquanto cátions amônio de aminas terciárias podem fazer apenas uma.
O resultado da soma de fatores é que as constantes de basicidade de aminas primárias, secundárias e terciárias são próximas.
Alquilação de aminas[editar | editar código-fonte]
Em diversas reações, o átomo de nitrogênio atua como um nucleófilo, uma espécie química que reage transferindo os seus elétrons em uma reação química.[3]
Um haleto pode reagir com uma amina para formar uma amina alquil-substituída correspondente, com liberação de um ácido de halogênio:

Se a amina reagente é uma amina terciária neste tipo de reação, formam-se um cátion de amônio quaternário e um ânion (ou "anião") haleto:
Os compostos com íons emparelhados desta forma são chamados de sais quaternários de amônio. O "X" mostrado nas reações anteriores pode também ser outro tipo de grupo abandonador.
Acilação de aminas[editar | editar código-fonte]

Aminas primárias e secundárias reagem com cloretos de ácido e anidridos carboxílicos para formar amidas (reação Schotten – Baumann). Nesta reação é formado como subproduto ácido clorídrico ou um ácido carboxílico que podem reagir com a amina do meio por uma reação ácido-base, o que inativaria esta amina como nucleófilo. Por esta razão, se adiciona uma base para capturar o ácido formado.

Formação de sulfonamida[editar | editar código-fonte]
As aminas primárias e secundárias reagem com cloretos de sulfonil, resultando em sulfonamidas, algumas ativas como fármacos. Essa transformação, conhecida como teste de Hinsberg, é um teste químico para a presença de aminas.
Síntese[editar | editar código-fonte]
Alquilação[editar | editar código-fonte]
As aminas mais significantes industrialmente são produzidas através do processo de alquilação da amônia por um álcool:
- ROH + NH3 → RNH2 + H2O
Essas reações necessitam de catalisadores, aparelhos especializados e medidas adicionais de purificação. As mesmas aminas podem ser preparadas pelo tratamento de haloalcanos com amônia e aminas:
- RX + 2 R′NH2 → RR′NH + [RR′NH2]X
Tais reações, que são mais úteis para iodetos e brometos de alquila, são raramente utilizados devido a dificuldade de controlar o grau de alquilação.[4]
Redução[editar | editar código-fonte]
Através do processo de hidrogenação, nitrilos são reduzidos a aminas utilizando hidrogênio em presença de um catalisador de níquel. Essa reação é sensível a condições ácidas ou básicas as quais podem causar a hidrólise do grupo -CN. LiAlH4 é comumente empregado para redução de nitrilos em escala de laboratório. Similarmente, LiAlH4 reduz amidas a aminas. Muitas aminas são produzidas a partir de aldeídos e cetonas via aminação redutiva, que tanto pode proceder cataliticamente ou estequiometricamente.Anilina (C6H5NH2) e seus derivados são preparados pela redução de compostos nitroaromáticos. na industria, hidrogênio é o redutor mais utilizado, enquanto que no laboratório, estanho e ferro são frequentemente utilizados.
Exemplos de aminas[editar | editar código-fonte]
Os aminoácidos constituintes das proteínas como a glicina, alanina, etc. contêm um grupo amino e um grupo carboxilo ligados ao mesmo átomo de carbono. Os aminoácidos unem-se uns aos outros através da ligação destes dois grupos – que formam um grupo amida – dando origem às ligações peptídicas que estruturam as proteínas. A lisina apresenta um grupo NH2 na cadeia lateral, que altera as propriedades de solubilidade de enzimas e funciona como ponto de ancoragem do retinal em enzimas que absorvem luz, como a rodopsina.
A degradação de proteínas (por exemplo, quando um pedaço de carne apodrece), leva, pelo contrário, à sua decomposição em aminas distintas. Os odores mais desagradáveis de que geralmente nos lembramos são, provavelmente, devidos à presença de aminas. Por exemplo, a 1,5-pentanodiamina (mais conhecida pelo sugestivo nome de cadaverina, libertada pelos corpos em putrefacção, o escatol, um composto heterocíclico presente nos excrementos, a 1,4-butanodiamina (putrescina – outro cheiro “a podre”), etc…

Os alcalóides são compostos complexos presentes na constituição das plantas que contêm grupos amina. Podemos citar alguns exemplos mais conhecidos, como a morfina, a nicotina, etc.
A importância das aminas, em termos biológicos, é inegável. A classe de compostos designados por β-feniletilaminas inclui a adrenalina, a noradrenalina, a mescalina, etc. As sulfamidas, que afetam as bactérias ao inibir nelas a produção de ácido fólico, mas que são inócuas para o ser humano, contêm um grupo amino. O neurotransmissor GABA (ácido 4-aminobutanóico) também contém um grupo amino. Alguns derivados do ácido p-aminobenzóico são também usados como anestésicos.
Encontram-se aminas secundárias em alguns alimentos (carne e peixe) ou no fumo do tabaco. Estas podem reagir com os nitritos (presentes nos conservantes utilizados nos produtos alimentares e usados como fertilizante, no caso das plantas, como o tabaco), levando à formação de N-nitrosoaminas secundárias, que são cancerígenas.
Ver também[editar | editar código-fonte]
- Fosfina (grupo funcional) - análogo com fósforo
- Álcool, Fenol e Éter - análogo com oxigênio
- Amida - anião derivado da amina (ligado a metal), ou o grupo funcional -CONR2
- Imina - grupo funcional R2C=NR
- Óxido de amina - derivado da amina terciária, quando o N está ligado a um O: (N=O)R3
Bibliografia[editar | editar código-fonte]
- Robert T. Morrison, Robert N. Boyd, and Robert K. Boyd, Organic Chemistry, 6th edition (Benjamin Cummings, 1992, ISBN 0-13-643669-2
Referências
- ↑ Fundamentos de Química Orgânica- Ciências da Vida e Saúde, Lazzarotto, Márcio, Editora Paco
- ↑ a b IUPAC, Compêndio de Terminologia Química, 2ª ed. ("Gold Book"). Compilado por A. D. McNaught e A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). Versão online: "amines" (2006–) criado por M. Nic, J. Jirat, B. Kosata; atualizações compiladas por A. Jenkins. ISBN 0-9678550-9-8.
- ↑ March, Jerry, 1929-1997. (1992). Advanced organic chemistry : reactions, mechanisms, and structure 4th ed ed. New York: Wiley. OCLC 25204734
- ↑ Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke "Amines, Aliphatic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi:10.1002/14356007.a02_001
