Aminoglicosídeo

Um aminoglicosídeo é um grupo de fármacos compostos de um grupo amino e um grupo glicosídeo. Os medicamentos desta classe são bactericidas, inibidores de síntese proteica das bactérias sensíveis. Foram isoladas de culturas dos microorganismos Streptomyces e Micromonospora.
Diversos aminoglicosídeos funcionam como antibióticos que são efetivos contra certos tipos de bactérias. Eles incluem a amicacina, arbecacina, gentamicina, canamicina, neomicina, netilmicina, paromomicina, rodostreptomicina[1], estreptomicina, tobramicina e apramicina.
As antraciclinas são outro grupo de aminoglicosídeos, que são utilizadas na quimioterapia.
A excreção dos aminoglicosídeos se dá pelos rins, com uma pequena meia vida de excreção de cerca de duas horas.
Contudo, ao acumularem-se no córtex renal, os aminoglicosídeos induzem necrose tubular aguda.
História[editar | editar código-fonte]
O primeiro aminoglicosídeo – a estreptomicina – foi isolado em 1944 por Waksman e seus colaboradores a partir de culturas de Streptomyces griseus e foi o segundo antibiótico usado na terapêutica, logo após o aparecimento da penicilina, nomeadamente para o tratamento da tuberculose.[2]
A estreptomicina, a neomicina e a tobramicina são derivados de Streptomyces spp., enquanto a gentamicina é obtida de Micromonospora spp. Por outro lado, eles também podem ser obtidos, in vitro, por síntese química, à custa de produtos naturais, como é o caso da netilmicina, amicacina, arbecacina e isepamicina.[2]
Indicações[editar | editar código-fonte]
- Sepse com Gram-negativos.
- Infecções com bactérias Gram-negativas aeróbias, como Pseudomonas, Acinetobacter e Enterobacter.
- Contra Streptococcus e Listeria concomitantemente com penicilina.
- Usadas secundariamente em infecções por Mycobacterium, como na Tuberculose.
Mecanismo de ação[editar | editar código-fonte]
São caracterizados por um efeito pós-antibiótico, isto é, a atividade bactericida permanece mesmo com a diminuição da concentração sérica abaixo da concentração mínima inibitória (CIM). Estes antibióticos penetram no interior das bactérias Gram negativas, por difusão facilitada nas porinas presentes na membrana externa. O local de ação é a subunidade 30s dos ribossomo, que é composto por vinte e uma proteínas e uma molécula 16s de ARN. O antibiótico aminoglicosídeo liga-se à proteína 12s na subunidade 30s ribossômica, o que leva a um erro de leitura do código genético. A síntese proteica pode ser inibida de duas formas diferentes, por interferência sobre o complexo de iniciação ou a leitura errônea do ARNm, que leva à incorporação de diferentes aminoácidos, resultando numa proteína não funcional.[3]
Efeitos adversos[editar | editar código-fonte]
São reversíveis se detectados prematuramente e a administração cessada. Contraindicados se há patologia renal.
- Ototoxicidade: danos progressivos nas células sensoriais do sentido da audição e do equilibrio no ouvido interno: pode resultar em ataxia (andar desequilibrado), vertigens; surdez.
- Nefrotoxicidade: danos nos túbulos do rim. É aconselhável o controle dos níveis plasmáticos.
- Bloqueio neuromuscular e paralisia: raramente observado. A miastenia grave é uma contraindicação absoluta para o uso dos aminoglicosídeos.
Formas de administração[editar | editar código-fonte]
Como não são absorvidos por via oral, são geralmente administrados por via intravenosa, intramuscular ou na forma de cremes tópicos para tratamento de feridas.
Pode ser utilizado por via oral para descontaminação do estômago (como em encefalopatia hepática).
Pode ser inalado, para tratamento de fibrose cística
Intra-arterial para tratamento do coração, e seus batimentos.
Membros do grupo[editar | editar código-fonte]
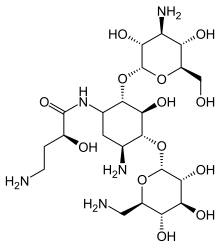
- Amicacina: mais eficaz contra estirpes parcialmente resistentes.
- Apramicina
- Arbecacina
- Canamicina
- Estreptomicina: muito usado na guerra do ultramar, muito ototóxico.
- Gentamicina
- Isepamicina: o mais recente.
- Netilmicina: o menos tóxico.
- Neomicina: comum em pomadas tópicas para tratamento de feridas
- Tobramicina: o mais eficaz com o Streptococuos.
- Paromomicina
Referências
- ↑ Massachusetts Institute of Technology. "Bacterial 'Battle For Survival' Leads To New Antibiotic." ScienceDaily 27 February 2008. 28 February 2008 <http://www.sciencedaily.com /releases/2008/02/080226115618.htm>.
- ↑ a b RIBEIRO, A. M. F. Farmacologia dos Antibióticos Aminoglicosídeos. 2017. 72 f. Dissertação (Mestrado) - Curso de Ciências Farmacêuticas, Universidade Fernando Pessoa, Porto, 2017. Disponível em: <https://bdigital.ufp.pt/bitstream/10284/6570/1/PPG_31032.pdf>. Acesso em: 21 nov. 2019.
- ↑ BAPTISTA, M. G. F. M. Mecanismos de Resistência aos Antibióticos. 2013. 51 f. Tese (Doutorado) - Curso de Ciências Farmacêuticas, Universidade Lusófona de Humanidades e Tecnologia, Lisboa, 2013. Disponível em: <http://recil.grupolusofona.pt/bitstream/handle/10437/3264/Mecanismos%20de%20Resist%C3%AAncia%20aos%20Antibi%C3%B3ticos%20%20Maria%20Galv%C3%A3o%20Ba.pdf?sequence=1>. Acesso em: 21 nov. 2019.
