Penicilina

As penicilinas são antibióticos do grupo dos betalactâmicos profusamente utilizados no tratamento de infecções causadas por bactérias sensíveis. A maioria das penicilinas são derivadas do ácido 6-aminopenicilânico, diferenciando-se umas das outras conforme a substituição na cadeia lateral do seu grupo amino. A benzilpenicilina, ou penicilina G, foi o primeiro antibiótico amplamente utilizado na medicina; a sua descoberta foi atribuída ao médico e bacteriologista escocês Alexander Fleming em 1928, que juntamente com os cientistas Ernst Boris Chain e Howard Walter Florey — que criaram um método para produzir em massa o medicamento — ganhou o Prêmio Nobel de Medicina em 1945. O fármaco está disponível desde 1941, sendo o primeiro antibiótico a ser utilizado com sucesso.[1][2]
O mecanismo de ação das penicilinas não é totalmente conhecido, embora sua analogia com a D-alanil-D-alanina terminal, localizada na cadeia lateral peptídica da subunidade do peptidoglicano (o principal constituinte da parede bacteriana) sugere que o seu carácter bactericida deriva da sua intervenção como inibidor enzimático do processo de transpeptidação durante a sua síntese. Desta forma, a penicilina actua debilitando a parede bacteriana e favorecendo a lise osmótica da bactéria durante o processo de multiplicação.[3]
Existe uma grande diversidade de penicilinas. Algumas espécies de fungos do género Penicillium sintetizam naturalmente penicilinas, como o primeiro tipo isolado, a penicilina G. Porém, devido ao aparecimento de resistências, outras famílias foram desenvolvidas seguindo basicamente duas estratégias: a adição de precursores da cadeia lateral ao meio de cultura do fungo produtor, o que se traduz na produção de penicilinas biossintéticas; e a modificação química da penicilina obtida pela fermentação biotecnológica, dando lugar às penicilinas semissintéticas.[4]
As penicilinas diferenciam-se entre si de acordo com o seu espectro de ação. Por exemplo, a benzilpenicilina é eficaz contra bactérias gram-positivas como estreptococos e estafilococos, assim como gonococos e meningococos, porém deve administrar-se por via parenteral (por injeção) devido à sua sensibilidade ao pH ácido do estômago. A fenoximetilpenicilina é, no entanto, resistente a este pH e pode ser administrada por via oral. A ampicilina, além de apresentar resistência ao pH, é efetiva contra bactérias gram-negativas como Haemophilus, Salmonella e Shigella.[3]
Embora as penicilinas sejam antibióticos menos tóxicos, é comum que produzam alergias. Cerca de 10% dos pacientes que recebem tratamentos de betalactâmicos desenvolvem-nas.[5] Uma vez que um choque anafiláctico pode provocar a morte do paciente, é necessário interrogá-lo antes de se dar início ao tratamento.
Além das suas propriedades antibacterianas, a penicilina é um antídoto eficaz contra os efeitos de envenenamento por α-amanitina, um dos aminoácidos tóxicos dos fungos do género Amanita.[6]
História[editar | editar código-fonte]
Tem-se dito que muitas descobertas científicas são feitas ao acaso. O acaso, já dizia Pasteur, só favorece aos espíritos preparados e não prescinde da observação. A descoberta da penicilina constitui um exemplo típico. Alexander Fleming, bacteriologista do St. Mary's Hospital, de Londres, vinha já há algum tempo pesquisando substâncias capazes de matar ou impedir o crescimento de bactérias nas feridas infectadas. Essa preocupação se justificava pela experiência adquirida na Primeira Grande Guerra (1914-1918), na qual muitos combatentes morreram em consequência da infecção em ferimentos profundos. Em 1922 Fleming descobrira uma substância antibacteriana na lágrima e na saliva, a qual dera o nome de lisozima. Em 1929 Fleming desenvolvia pesquisas sobre estafilococos, quando descobriu a penicilina. A descoberta da penicilina deu-se em condições peculiaríssimas, graças a uma sequência de acontecimentos imprevistos e surpreendentes.
O fungo foi identificado como pertencente ao gênero Penicilium, donde deriva o nome de penicilina dado à substância por ele produzida. Fleming passou a empregá-la em seu laboratório para selecionar determinadas bactérias, eliminando das culturas as espécies sensíveis à sua ação.
O surgimento dos antibióticos ocorreram no final dos anos 20, ou seja, a penicilina como conhecemos foi descoberta em 1928 por Alexander Fleming quando saiu de férias e esqueceu algumas placas com culturas de micro-organismos em seu laboratório no Hospital St. Mary em Londres.[7] Quando voltou, reparou que uma das suas culturas de Staphylococcus tinha sido contaminada por um bolor, e em volta das colônias deste não havia mais bactérias. Então, Fleming e seu colega, Dr. Pryce, descobriram um fungo do gênero Penicillium, e demonstraram que o fungo produzia uma substância responsável pelo efeito bactericida: a penicilina. Esta foi obtida em forma purificada por Howard Florey, Ernst Chain e Norman Heatley, da Universidade de Oxford, muitos anos depois, em 1940. Eles comprovaram as suas qualidades antibióticas em ratos infectados, assim como a sua não-toxicidade. Em 1941, os seus efeitos foram demonstrados em humanos. O primeiro homem a ser tratado com penicilina foi um agente da polícia que sofria de septicémia com abcessos disseminados, uma condição geralmente fatal na época. Ele melhorou bastante após a administração do fármaco, mas morreu quando as reservas iniciais de penicilina se esgotaram. Em 1945, Fleming, Florey e Chain receberam o Prémio Nobel de Fisiologia ou Medicina por este trabalho. A penicilina salvou milhares de vidas de soldados dos aliados na Segunda Guerra Mundial.[8][9]
A descoberta de Fleming não despertou inicialmente maior interesse e não houve a preocupação em utilizá-la para fins terapêuticos em casos de infecção humana até a eclosão da Segunda Guerra Mundial, em 1939. Em 1940, Sir Howard Florey e Ernst Chain, de Oxford, retomaram as pesquisas de Fleming e conseguiram produzir penicilina com fins terapêuticos em escala industrial, inaugurando uma nova era para a medicina — a era dos antibióticos. Alguns anos mais tarde, Ronald Hare, colega de trabalho de Fleming, tentou, sem êxito, "redescobrir" a penicilina em condições semelhantes às que envolveram a descoberta de Fleming. Após um grande número de experiências verificou que a descoberta da penicilina só se tornou possível graças a uma série inacreditável de coincidências, quais sejam: O fungo que contaminou a placa, como se demonstrou posteriormente, é um dos três melhores produtores de penicilina dentre todas as espécies do gênero Penicilium; O fungo contaminante teria vindo pela escada do andar inferior, onde se realizavam pesquisas sobre fungos;[7] O crescimento do fungo e dos estafilococos se fez lentamente, condição necessária para se evidenciar a lise bacteriana; No mês de agosto daquele ano, em pleno verão, sobreveio uma inesperada onda de frio em Londres, que proporcionou a temperatura ideal ao crescimento lento da cultura; A providencial entrada do Dr. Pryce no Laboratório permitiu que Fleming reexaminasse as placas contaminadas e observasse o halo transparente em torno do fungo, antes de sua inutilização. Apesar de todas essas felizes coincidências, se Fleming não tivesse a mente preparada não teria valorizado o halo transparente em torno do fungo e descoberto a penicilina.
Em Portugal[editar | editar código-fonte]
A primeira pessoa a ser tratada com penicilina em Portugal, foi tenente Fernando Ramôa em outubro de 1944, depois de ter sofrido um grave acidente nas Lajes, nos Açores, onde estava a cumprir serviço militar. Nessa altura, estavam no arquipélago elementos das tropas Aliadas, envolvidas na Segunda Guerra Mundial, e na posse do que era, então, um quase milagroso segredo: a penicilina. Foi graças a ela que o tenente conseguiu recuperar da grave infecção decorrente do acidente e a cura pareceu tão extraordinária que a família do portuense preservou, durante décadas, o frasquinho que continha a substância salvadora. O frasco portador da primeira penicilina administrada a um português ficou, assim, guardado, até ser oferecida ao Museu da Farmácia.[10]
Estrutura química[editar | editar código-fonte]
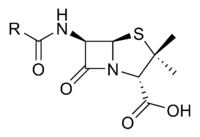
As penicilinas contêm um anel activo, o anel beta-lactâmico, que partilham com as cefalosporinas. As penicilinas contêm um núcleo comum a todas elas e uma região que varia conforme o subtipo. Todas penicilinas têm a mesma estrutura básica: ácido 6 aminopenicilanico, um anel tiazolidina unido a um anel beta lactâmico que leva um grupo amino livre.[11]
Mecanismo de ação[editar | editar código-fonte]
Todos os antibióticos beta-lactâmicos (penicilinas e cefalosporinas) interferem na síntese de parede celular bacteriana, através de sua ligação com as enzimas PBP. A penicilina acopla num receptor presente na membrana interna bacteriana (PBP) e interfere com a transpeptidação que ancora o peptidoglicano estrutural de forma rígida em volta da bactéria. Como o interior desta é hiperosmótico, sem uma parede rígida há afluxo de água do exterior e a bactéria lisa (explode).
O principal mecanismo de resistência de bactérias à penicilina baseia-se na produção de Beta-lactamases, enzimas que degradam a penicilina impedindo sua ação. Outro mecanismo de ação da penicilina é a inativação do inibidor das enzimas autolíticas na parede celular. Isto dá, como resultado, a lise celular.[12][13][14]
Propriedades farmacológicas[editar | editar código-fonte]
Em relação à farmacocinética, as penicilinas apresentam várias diferenças, as quais definem seu uso clínico:
- Benzilpenicilinas ou penicilinas naturais;
- Penicilinas resistentes às penicilinases;
- Penicilinas de amplo espectro, obtidas por associação com inibidores de ß-lactamase.
Benzilpenicilinas[editar | editar código-fonte]
Entre as benzilpenicilinas, a associação da penicilina com determinadas substâncias determina sua farmacocinética e farmacodinâmica.[15]
Penicilina cristalina ou aquosa[editar | editar código-fonte]
Restrita ao uso endovenoso. Apresenta meia-vida curta (30 a 40 minutos), é eliminada do organismo rapidamente (cerca de 4 horas). Distribuí-se amplamente pelo organismo, alcançando concentrações terapêuticas em praticamente todos os tecidos. É a única benzilpenicilina que ultrapassa a barreira hemato-encefálica em concentrações terapêuticas, e mesmo assim, somente quando há inflamação.[15]
Penicilina G procaína[editar | editar código-fonte]
Apenas para uso intramuscular. A associação com procaína retarda o pico máximo e aumenta os níveis séricos e teciduais por um período de 12 horas.
Penicilina G benzatina[editar | editar código-fonte]
Foi a primeira descoberta, geralmente injetável (intra-muscular) ainda que existam formas bucais para tratamento dental. Ela é mal absorvida a partir do intestino por isso a via oral não é utilizada.
É uma penicilina de depósito, pouco hidrossolúvel, e seu uso é exclusivamente intramuscular. Os níveis séricos permanecem por 15 a 30 dias, dependendo da dose utilizada.
Penicilina V[editar | editar código-fonte]
É geralmente administrada por via oral e é absorvida para o sangue ao nível intestinal. Os níveis séricos atingidos por esta preparação são 2 a 5 vezes maiores do que os obtidos com as penicilinas G administradas por via intramuscular e com distribuição tecidual similar a esta. Pode ser utilizada como terapêutica sequencial oral na substituição das penicilinas parenterais, exceto contra Neisseria spp e Haemophilus spp.[15]
Aminopenicilinas[editar | editar código-fonte]
As aminopenicilinas são penicilinas semi-sintéticas, disponíveis desde 1960, após a adição de um grupo amino na cadeia lateral, e de espectro de ação mais amplo, em relação às benzilpenicilinas. Apresentam boa absorção, tanto oral como parenteral.[15]
As aminopenicilinas disponíveis para uso clínico no Brasil são: Ampicilina e Amoxacilina.
Ampicilina[editar | editar código-fonte]
Apresenta meia-vida de 1,2 horas, não devendo ser utilizada com intervalos maiores que 6 horas. Tem boa distribuição em todos os compartimentos orgânicos e atinge concentrações terapêuticas no LCR, líquido pleural, articulações e fluidos peritoneais na presença de inflamação e após administração parenteral.
Amoxicilina[editar | editar código-fonte]
Difere da ampicilina pela presença do grupo hidroxil na cadeia benzênica. A absorção por via oral é melhor do que a da ampicilina. Utilizada com intervalos de 8 horas. Alcança níveis no LCR inferiores a ampicilina, não havendo vantagem do seu uso para terapêutica de pacientes com meningoencefalites bacterianas.
Penicilinas resistentes às penicilinases[editar | editar código-fonte]
Após o advento da penicilina G, houve uma rápida disseminação de resistência a esta droga, por produção de ß-lactamases, pelos estafilococos. Assim, foram desenvolvidas as penicilinas resistentes às penicilinases.[15]
No Brasil, atualmente, o único representante disponível é a oxacilina.
Oxacilina[editar | editar código-fonte]
Disponível apenas para uso endovenoso. Apresenta metabolização hepática, excreção renal. Atinge concentrações liquóricas satisfatórias quando na presença de processos inflamatórios.
Posteriormente, para ampliar a cobertura contra os bacilos gram-negativos, foram desenvolvidas as penicilinas chamadas de penicilinas de amplo espectro. Dividem-se em dois grupos:
- Carboxipenicilinas (representadas por carbenicilina e ticarcilina); e
- Ureído-penicilinas (representadas por mezlocilina, piperacilina e azlocilina).
Penicilinas de amplo espectro, obtidas por associação com inibidores de ß-lactamase[editar | editar código-fonte]
Apesar do desenvolvimento de toda essa variedade de penicilinas, a produção das ß-lactamases continuou sendo o meio mais eficiente e comum das bactérias se tornarem resistentes aos antimicrobianos ß–lactâmicos.[15]
Novas estratégias foram desenvolvidas para recuperar o espectro destes antimicrobianos.
Os inibidores de ß–lactamases, quando em associação com antimicrobianos ß-lactâmicos, ligam-se às ß-lactamases. Dessa forma, evitam a hidrólise do anel ß–lactâmico e potencializam sua atividade.
Identifique cada um deles:[15]
Amoxicilina - ácido clavulânico[editar | editar código-fonte]
Tanto a amoxacilina quanto o ácido clavulânico são absorvidos rapidamente pelo trato digestivo. Tem meia-vida de aproximadamente uma hora. Ligação proteica baixa (18 e 25%), com rápida penetração na maioria dos tecidos e líquidos extravasculares, incluindo líquidos pleural, peritoneal e secreções pulmonares. Apresenta excelente atividade contra S. aureus e anaeróbios produtores da ß-lactamases. Ativo contra H. influenzae e Moraxella catarrhalis produtoras de ß-lactamases.
Ticarcilina – ácido clavulânico[editar | editar código-fonte]
Ambas apresentam meia-vida de uma hora. Atingem bom nível sérico em ossos, líquidos biliares e articulares. Embora atravesse a barreira hematoliquórica na presença de inflamação, esta combinação não deve ser utilizada para tratamento de infecções neste sítio. Esta associação está indicada em infecções graves causadas por E. coli, Klebsiella spp., Proteus spp., Enterobacter spp., Pseudomonas aeruginosa, Serratia spp., Providencia spp., S. aureus oxacilina sensível, e Bacteroides fragilis.
Ampicilina – sulbactam[editar | editar código-fonte]
A relação é de 2:1 e a dose total de sulbactam não deve ultrapassar a 4g por dia. Meia-vida de uma hora para ambas as drogas. Mais de 75% desta associação é eliminada por via renal. Ambos penetram bem tanto nos tecidos como nos líquidos extravasculares. No líquido peritoneal atinge 90% da concentração sérica. Na presença de meninges inflamadas atinge bom nível liquórico, porém a correlação clínica precisa ser melhor avaliada. A ampicilina quando em associação com sulbactam é ativa contra cepas produtoras de ß-lactamases incluindo S. aureus, H. influenzae, M. catarrhalis, E. coli, Proteus spp., Providencia spp., Klebsiella spp. e anaeróbios. Não tem atividade contra P. aeruginosa ou cepas de enterobacteriaceas indutoras de ß-lactamases. Já existem relatos de cepas de E. coli resistentes a esta associação.
Piperacilina – tazobactam[editar | editar código-fonte]
A proporção da associação é de 8:1. Após 30 minutos da infusão a meia-vida é de 0,7 a 1,2 horas. Apresentam boa distribuição tecidual e em líquidos orgânicos, incluindo pulmões, pele, mucosa intestinal, vesícula e líquidos biliares. Atinge baixos níveis no LCR na ausência de inflamação. Ativa contra todas as cepas de S. aureus oxacilina sensível, estreptococos e enterococos. O tazobactam aumenta a atividade da piperacilina contra enterobacteriaceas produtoras de ß-lactamases, H. influenzae, N. gonorrhoeae, e M. catarrhalis. A maioria das P. aeruginosa é resistente a essa associação. “In vitro” e “in vivo” todos os anaeróbios gram-positivos e negativos são suscetíveis à combinação de piperacilina e tazobactam, mas essa associação não apresenta vantagem em relação às outras associações com inibidores de ß-lactamases para os anaeróbios.
Usos terapêuticos[editar | editar código-fonte]
É a primeira escolha para infecções bacterianas causadas por organismos Gram-positivos e outros que não sejam suspeitos de resistência.
É geralmente eficaz contra espécies Gram+ ou de Streptococcus, Clostridium, Neisseria, e anaérobiose excluindo Bacteroides. Usa-se em casos de meningite bacteriana, bacterémia, endocardite, infecções do tracto respiratório (pneumonia), faringite, escarlatina, sífilis, gonorreia, otite média e infecções da pele causadas pelos organismos referidos.
A Penicilina já não é a primeira escolha em infecções por Staphylococcus devido a resistência disseminada nesse género.
Pneumonias[editar | editar código-fonte]
Agente mais frequente: S. pneumoniae é o agente mais frequente das pneumonias adquiridas na comunidade.[15] Droga de escolha: as penicilinas permanecem como opção para tratar estas infecções, porém as penicilinas não têm atividade contra agentes intracelulares (atípicos) e devem ser avaliadas com cuidado em regiões com alta resistência à penicilina. Outros agentes frequentes: Haemophilus influenzae é um dos agentes mais frequentes de pneumonia em idosos e crianças menores de 4 anos. A resistência deste microrganismo às penicilinas varia entre 5 a 30%, conforme a localidade.
As penicilinas anti-pseudomonas (piperacilina/tazobactam), entre outras, são opções para o tratamento:
- Pneumonias de repetição dos portadores de fibrose cística (geralmente causado por Pseudomonas spp.);
- Tratamento das pneumonias em pacientes internados em instituições para idosos, alcoólatras ou desnutridos (geralmente causadas por bacilos gram-negativos);
- Pneumonia associada à assistência à saúde.
Otites e sinusites[editar | editar código-fonte]
- Agentes usuais: Nas crianças menores de cinco anos, os agentes usuais são H. influenzae e S. pneumoniae.[15]
Opção: aminopenicilinas geralmente em combinação com ácido clavulânico.
- Em processos crônicos: a cultura de secreções é importante, podendo estar presentes os estafilococos, bacilos gram-negativos e anaeróbios. Neste caso, devem ser usadas penicilinas com atividade anti-estafilocócica e anti-pseudomonas.
- Em pacientes diabéticos: com a cronificação dos processos infecciosos, surge a Pseudomonasspp, como agente frequente, sendo necessário o uso de penicilinas anti-pseudomonas.
Faringites e epiglotites[editar | editar código-fonte]
- Agente mais frequente: em pacientes não neutropênicos, o agente mais frequente deste tipo de infecção é o S. pyogenes (Streptococcus ß-hemolítico, do grupo A).[15]
- Drogas de escolha: as penicilinas G e V ou aminopenicilinas. O uso de ampicilina com inibidor de beta-lactamase ou cefalosporina de terceira geração está indicado.
- H. influenzae: nas epiglotites, em crianças e às vezes nos adultos jovens, o H. influenzae é o microrganismo envolvido e pode desencadear bacteremia, sendo neste caso tratadas como infecções potencialmente graves, com terapêutica parenteral.
Infecções cutâneas[editar | editar código-fonte]
- Estreptococo: a maioria destas infecções é causada por estreptococos, em particular as infecções superficiais.
- Estafilococo: algumas infecções cutâneas, as mais profundas, que surgem em pacientes diabéticos e as da região da face.
- Pós-trauma, são devidas ao estafilococo. Neste caso, deve-se utilizar penicilinas resistentes às penicilinases: oxacilina é a terapêutica mais recomendada.
Meningites bacterianas[editar | editar código-fonte]
- Agentes causadores mais frequentes*: N. meningitides, S pneumoniae e H. influenzae.
- Drogas de escolha*: penicilina cristalina em altas doses é uma boa opção terapêutica de germes sensíveis.
Efeitos indesejados[editar | editar código-fonte]
Reações de hipersensibilidade[editar | editar código-fonte]
A penicilina não tem efeitos secundários significativos, mas pode raramente causar reações alérgicas e até choque anafilático nos indivíduos susceptíveis.[15]
Sintomas iniciais nesses casos podem incluir eritemas cutâneos disseminados, febre e edema da laringe, com risco de asfixia. A sua introdução por injeção no organismo também é conhecida por ser dolorosa.
- Toxicidade: Geralmente as penicilinas apresentam pouca toxicidade, mas suas reações de hipersensibilidade são frequentes, ocorrendo em até 8% dos pacientes.
- Variações: podem variar desde uma simples reação urticariforme até choque anafilático.
- Agentes: É mais comum com as benzilpenicilinas, entretanto, pode ocorrer com qualquer penicilina.
Manifestações cutâneas[editar | editar código-fonte]
São bastante variáveis, desde eritema difuso, “rash” cutâneo, placas urticariformes, até raramente a síndrome de Stevens-Johnson. Estas reações geralmente são tardias e ocorrem em 1 a 10% dos pacientes. Podem ser acompanhadas por eosinofilia e febre. As aminopenicilinas são as mais associadas com estas reações dermatológicas.[15]
Toxicidade Renal[editar | editar código-fonte]
A nefrite intersticial alérgica pode ocorrer, sendo mais frequente com a oxacilina. Acompanha–se de febre, “rash”, eosinofilia e hematúria.[15]
Toxicidade hematológica[editar | editar código-fonte]
São incomuns, mas anemia hemolítica e trombocitopenia devem ser lembradas. A leucopenia é dose e tempo-dependente. Desordens hemorrágicas podem surgir por efeito similar às aspirinas, por alteração da agregação plaquetária.[15]
Neurotoxicidade[editar | editar código-fonte]
Convulsões e abalos musculares podem ocorrer com altas doses de penicilinas quando na presença de insuficiência renal.[15]
- Atenção: As convulsões são refratárias aos anticonvulsivantes e cessam apenas com a retirada do antimicrobiano.
Outros[editar | editar código-fonte]
Além disso uso prolongado ou em altas doses pode causar deplecção da flora normal no intestino e suprainfecção com espécie patogénica.[16]
Fármacos derivados[editar | editar código-fonte]
Existem muitos antibióticos derivados por métodos químicos industriais da penicilina, constituindo as penicilinas semi-sintéticas:
- Amoxicilina, Ampicilina e Pivampicilina têm maior espectro de ação, e são eficazes contra mais tipos de organismos.
- Flucloxacilina é mais resistente à beta-lactamase (uma penicilinase).
- Carbenicilina, Aziocilina, Ticarcilina são eficazes contra espécies de Pseudomonas, especialmente a P.aeruginosa, que são importantes patogénios do meio hospitalar.[17]
Fleming e Churchill[editar | editar código-fonte]
Não passa de um boato a história de que a família de Alexander Fleming teria salvo a vida de Winston Churchill duas vezes: a primeira vez, quando o menino Winston teria sido salvo de afogamento (por Alexander ou seu pai), o que teria feito com que o pai de Winston, como agradecimento, tivesse pago os estudos do jovem Alexander, e, na segunda vez, quando a penicilina (descoberta por Fleming) foi usada para curar Churchill de pneumonia. A história foi inventada por Arthur Gladstone Keeney: nem o quase afogamento pode ser confirmado, nem Churchill foi tratado por penicilina, e sim por sulfadiazina.[18]
Excreção[editar | editar código-fonte]
As penicilinas são eliminadas por secreção tubular nos rins.
Produção industrial por processos fermentativos[editar | editar código-fonte]
Como é possível observar, a penicilina é um antibiótico de extrema importância para a indústria farmacêutica, visto que é amplamente utilizado no tratamento de diversas doenças. Para realizar a comercialização dessa droga, deve-se, primeiramente, produzi-la em grande escala e, para isso, utiliza-se do processo de produção via fermentação aeróbia do microrganismo produtor. Para a produção da penicilina, é necessário realizar um inóculo do microrganismo utilizado para que as vias metabólicas do mesmo sintetizem o composto, sendo os microrganismos mais utilizados nesse caso, os fungos das espécies Penicillium chrysogenum e Aspergillus nidulans. É interessante destacar que, no caso da produção de antibióticos em geral, os meios de cultivo utilizados na fermentação podem ser oriundos de matérias primas derivadas de resíduos agroindustriais. No caso da penicilina, é comum o uso de água de milho, arroz ou trigo como fontes de nitrogênio, como também melaço como fonte de carbono.[19]
Para produção dos antibióticos em geral utiliza-se do processo fermentação submersa com agitação, uma vez que dessa forma facilita-se a manipulação de maiores volumes de meio, além de que a absorção de nutrientes e excreção de metabólitos ocorre de maneira mais rápida e simples, aumentando então a produtividade do sistema. Dessa forma, inicia-se a produção da penicilina por meio da fermentação submersa inoculando esporos liofilizados com alta concentração de células, para ocorrer a formação de agregados celulares, denominados pellets. O inóculo passa por uma sequência de etapas para potencializar o crescimento das células de forma que possa ser iniciado a produção em grande escala no fermentador. A Figura a seguir representa esquematicamente o processo de produção da penicilina em escala industrial.[19]

De acordo com estudos, alguns parâmetros para a fermentação foram determinados a fim de otimizar a produção da penicilina, sendo esses o crescimento aeróbio com absorção de oxigênio a taxas de 0,4- 0,8 mM/L.min, a temperatura ótima entre 25-27 ⁰C, e o pH constante de 6,5, sendo o tempo total de reação de 120 a 160 horas em reatores de aço inox com volumes entre 40 m³ e 200 m³, para que a areação ao longo do reator seja a adequada.[19]
Purificação de Penicilina[editar | editar código-fonte]
Após todo o processo de fermentação, faz-se necessária a separação do antibiótico produzido e excretado pelo microrganismo do meio de cultivo retirado do reator.[19] A Figura a seguir indica as fases que devem ser executadas para a posterior purificação da penicilina.

Como é possível perceber, o primeiro passo a ser seguido é a filtração, para retirada do micélio, do caldo fermentado, seguida por duas extrações líquido-líquido contínuas em contracorrente com acetato de amila, butila ou metilisobutilcetona, em condições de pH e temperatura de 2,5 a 3,0 e 0 a 3 ⁰C respectivamente. Logo após, o produto obtido após essas etapas segue para uma fase de adsorção e subsequente filtração. Realizados esses procedimentos, necessita-se precipitar a penicilina desse produto obtido anteriormente e, para isso, realiza-se uma reação do composto com acetona, permitindo que ocorra a precipitação. Com isso, deve-se apenas filtrar a penicilina precipitada para separá-la da fração líquida e subsequente cristalização, usando isopropanol, e centrifugação e secagem, obtendo assim o produto final.[19]
Ver também[editar | editar código-fonte]
Referências
- ↑ Nossa capa: Alexander Fleming e a descoberta da penicilina. J. Bras. Patol. Med. Lab., Rio de Janeiro , v. 45, n. 5, Oct. 2009
- ↑ A Penicilina. Superinteressante, fevereiro de 1988
- ↑ a b Prescott, L.M. (1999). McGraw-Hill Interamericana de España, S.A.U., ed. Microbiologia. [S.l.: s.n.] ISBN 84-486-0261-7
- ↑ Crueger, Wulf; Crueger, Anneliese (1989). Sinauer Associates, ed. A texbook of industrial microbiology 2 ed. Sunderland: [s.n.] ISBN 0878931317
- ↑ Solensky R (2003). Clinical reviews in allergy & immunology, ed. Hypersensitivity reactions to beta-lactam antibiotics. 24. [S.l.: s.n.] pp. 201–20. PMID 12721392. doi:10.1385/CRIAI:24:3:201
- ↑ Enjalbert F, Rapior S, Nouguier-Soulé J, Guillon S, Amouroux N, Cabot C (2002). Treatment of amatoxin poisoning: 20-year retrospective analysis. 40. [S.l.]: J Toxicol Clin Toxicol. PMID 12475187
- ↑ a b «FLEMING, O ACASO E A OBSERVAÇÃO». Cultura.com. Consultado em 15 de setembro de 2012
- ↑ Bettelheim, Frederick; Brown, William; Campbell, Mary; Farrell, Shawn; Torres, Omar. Introduction to Organic and Biochemistry. 8ª edi. Cengage Learning, 2012. pp. 243. ISBN 1133109764
- ↑ W. Hudler, George. Magical Mushrooms, Mischievous Molds. Edi. ilustrada. Princeton University Press, 2000. pp. 119. ISBN 0691070164
- ↑ «Água medicinal "poderosamente radioactiva"? Sim, já foi recomendada por cá»
- ↑ CALIXTO, Carolina Maria Fioramonti; CAVALHEIRO, Éder Tadeu Gomes. Penicilina: Efeito do Acaso e Momento Histórico no Desenvolvimento Científico. Química Niva Interativa - Sociedade Brasileira de Química
- ↑ Behera, D.. Textbook of Pulmonary Medicine, Volume 1. Edi. ilustrada: Jaypee Brothers Publishers, 2010. pp. 248. ISBN 8184487495
- ↑ Hacker, Miles; S. Messer II, William; A. Bachmann, Kenneth. Pharmacology: Principles and Practice. Academic Press, 2009. pp. 380. ISBN 0080919227
- ↑ Garg, Nisha; Garg, Amit. Textbook of Endodontics. Col: Anil Chandra. Edi. ilustrada. JP Medical Ltd, 2013. pp. 142. ISBN 9350909529
- ↑ a b c d e f g h i j k l m n o http://www.anvisa.gov.br/servicosaude/controle/rede_rm/cursos/rm_controle/opas_web/modulo1/propriedades4.htm ANTIMICROBIANOS - BASES TEÓRICAS E USO CLÍNICO - Anvisa
- ↑ «Penicilina (Benzetacil)». Tua Saúde. Consultado em 15 de setembro de 2012
- ↑ Strateva, Tanya; Yordanov, Daniel (2009). «Pseudomonas aeruginosa – a phenomenon of bacterial resistance» (PDF). Journal of Medical Microbiology (em inglês). 58: 1133–1148. doi:10.1099/jmm.0.009142-0. Consultado em 17 de maio de 2014
- ↑ Sir Alexander Fleming Twice Saved Churchill's Life. The Churchill Centre
- ↑ a b c d e PEREIRA, Erlon Lopes; OLIVEIRA, Ana Flávia Alves (2016). «A PRODUÇÃO DE ANTIBIÓTICOS POR PROCESSOS FERMENTATIVOS AERÓBIOS». REVISTA DA UNIVERSIDADE VALE DO RIO VERDE. 14 (2): 1058–1078. ISSN 1517-0276. doi:10.5892/ruvrd.v14i2.3157
- ↑ Borzani, Walter; Aquarone, Eugenio (agosto de 1957). «Molasses Fermentation, Continuous Fermentation, Alcoholic Fermentation of Blackstrap Molasses. Penicillin as Contamination Control Agent». Journal of Agricultural and Food Chemistry. 5 (8): 610–616. ISSN 0021-8561. doi:10.1021/jf60078a010
- ↑ Hook, Derek J. «Production of antibiotics by fermentation». Cambridge: Cambridge University Press: 433–456. ISBN 9780511802409
Ligações externas[editar | editar código-fonte]
