Clorofórmio
| Clorofórmio Alerta sobre risco à saúde | |
|---|---|

|
|

| |
| Nome IUPAC | Triclorometano |
| Outros nomes | Clorofórmio, Freon 20, R-20, UN 1888 |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| KEGG | |
| ChEBI | |
| Número RTECS | FS9100000 |
| SMILES |
|
| InChI | 1/CHCl3/c2-1(3)4/h1H
|
| Propriedades | |
| Fórmula molecular | CHCl3 |
| Massa molar | 119,38 g/mol |
| Aparência | líquido incolor |
| Densidade | 1,48 g/cm³, líquido |
| Ponto de fusão |
-63,5 °C |
| Ponto de ebulição |
61,2 °C |
| Solubilidade em água | 0,8 g/100 ml a 20 °C |
| Estrutura | |
| Forma molecular | Tetraedro |
| Riscos associados | |
| Principais riscos associados |
Nocivo (Xn), Irritante (Xi), |
| NFPA 704 | |
| Frases R | R22, R38, R40, R48/R20/R22 |
| Frases S | S2, S36/37 |
| Ponto de fulgor | Non-flammable |
| EUA Limite de exposição permissível (PEL) |
50 ppm (240 mg/m3) (OSHA) |
| Compostos relacionados | |
| Outros aniões/ânions | Trifluorometano, Bromofórmio, Iodofórmio |
| Outros catiões/cátions | Triclorossilano |
| Halometanos relacionados | Clorometano, Diclorometano, Tetracloreto de carbono |
| Compostos relacionados | Metano |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Clorofórmio ou triclorometano, é um composto químico de fórmula CHCl3, no estado líquido em temperatura ambiente, incolor e volátil. Ele é um anestésico externo, sendo muito tóxico se ingerido ou seus vapores aspirados. Pertence ao grupo dos trialometanos.
Estrutura[editar | editar código-fonte]
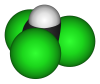
A molécula apresenta uma geometria molecular tetraédrica, em razão de o átomo de carbono central possuir hibridização sp3.
Ocorrência natural[editar | editar código-fonte]
Cerca de 660 000 toneladas de clorofórmio são emitidas no meio ambiente todos os anos,[1] e aproximadamente 90% dessas emissões tem origem natural.
A substância se volatiliza facilmente no solo e na superfície da água e se degrada no ar, produzindo fosgênio, diclorometano, cloreto de acila, monóxido de carbono e cloreto de hidrogênio. Sua meia-vida no ar varia entre 55 e 620 dias, e a degradação no solo e na água é lenta. Esse trialometano não se acumula de forma significativa em organismos aquáticos.[2]
História[editar | editar código-fonte]
O clorofórmio foi sintetizado de forma independente por vários pesquisadores por volta de 1831.
Moldenhawer, um farmacêutico alemão, parece ter produzido clorofórmio em 1830 ao misturar cal clorada com etanol. No entanto, ele pensou erroneamente tratar-se de 1,2-dicloroetano. Samuel Guthrie, físico norte-americano, também parece ter produzido clorofórmio com os mesmos reagentes em 1831 e notado suas propriedades anestésicas, mas também acreditou ter produzido o 1,2-dicloroetano.
Em 1850, o clorofórmio era sintetizado usando o procedimento de Liebig, importante até 1960, quando, passou a ser preparado em escala industrial pela cloração do clorometano.[3]
Usos[editar | editar código-fonte]
A reação mais importante do clorofórmio em termos de escala é a mistura com fluoreto de hidrogênio, produzindo CFC-22, um precursor na produção de Teflon.
Sua ação anestésica ocorre devido ao fato deste ser muito volátil, desta forma ele absorve calor da pele, a qual tem temperatura diminuída, então os nervos sensitivos que mandam as informações ao cérebro ficam inativos e a sensação de dor é diminuída. Atualmente, sua principal aplicação é como solvente. Também é usado como matéria-prima para a produção de outros compostos.
O clorofórmio é um trialometano, sua presença na água é um grande fator de poluição, mesmo que em pequenas quantidades. A legislação brasileira permite a presença de trialometanos de até 0,1 mg/L, acima disso a água é considerada como não potável.
Pela sua característica de causar várias desordens coronárias, foi paulatinamente abandonado pelos médicos, substituindo-o por outros analgésicos mais eficazes e com menos efeitos colaterais.
Pode ser fatal se for aspirado ou inalado. Causa irritação à pele, olhos e trato respiratório. Afeta o sistema nervoso central, rins, sistema cardiovascular e fígado. Pode causar câncer dependendo do nível e duração de exposição. Segundo a Agência de Proteção Ambiental Americana (EPA) o clorofórmio está classificado no Grupo B2, como provável carcinogênico humano. A exposição prolongada pode causar hepatite e icterícia[4].
Referências
- ↑ Gribble, Gordon W. (2004). «Natural Organohalogens: A New Frontier for Medicinal Agents?». Journal of Chemical Education. 81 (10). 1441 páginas. doi:10.1021/ed081p1441
- ↑ «Chloroform» (PDF). World Health Organization. 2004
- ↑ Rossberg, M. «Chlorinated Hydrocarbons». doi:10.1002/14356007.a06_233.pub2
- ↑ EPA - Agência Americana de Proteção Ambiental. «Air Toxics Web Site - Chloroform». EPA - Agência Americana de Proteção Ambiental. Consultado em 20 de abril de 2015

