Cânfora: diferenças entre revisões
| Linha 146: | Linha 146: | ||
== {{Links}} == |
== {{Links}} == |
||
{{Commons|Camphor}} |
{{Commons|Camphor}} |
||
*[http://books.google.fr/books?id=LpAUAAAAYAAJ&pg=PA117&lpg=PA117&dq=camphre&source=bl&ots=1QdPLJuUdc&sig=Nr9U-iCV6mYqJNndjiE9SIz5YKc&hl=fr&ei=ASvnSvikDOG8jAeh76S8CA&sa=X&oi=book_result&ct=result&resnum=2&ved=0CA4Q6AEwATgK#v=onepage&q=&f=false ''Histoire pharmacologique du camphre'' Par D. B. J. L. Millot] |
|||
*[http://www.infoescola.com/compostos-quimicos/canfora/ Infoescola: Cânfora] |
|||
*[https://www.infopedia.pt/dicionarios/termos-medicos/c%C3%A2nfora Infopédia:Cânfora] |
|||
{{Portal3|Química}} |
{{Portal3|Química}} |
||
Revisão das 01h04min de 16 de abril de 2017
| Cânfora Alerta sobre risco à saúde[1][2] | |
|---|---|

| |
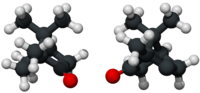
| |
| Nome IUPAC | 1,7,7-Trimethylbicyclo[2.2.1]heptan-2-one |
| Nome sistemático | 1,7,7-Trimethylbicyclo[2.2.1]heptan-2-one |
| Outros nomes | 2-Bornanone; Bornan-2-one; 2-Camphanone; Formosa |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| DrugBank | DB01744 |
| ChemSpider | |
| KEGG | |
| MeSH | |
| ChEBI | |
| Número RTECS | EX1225000 |
| SMILES |
|
| InChI | 1/C10H16O/c1-9(2)7-4-5-10(9,3)8(11)6-7/h7H,4-6H2,1-3H3
|
| Referência Beilstein | 1907611 |
| Referência Gmelin | 83275 |
| 3DMet | |
| Propriedades | |
| Fórmula química | C10H16O |
| Massa molar | 152.23 g mol-1 |
| Aparência | Branco, com cristais translucentes |
| Odor | fragrante e penetrante |
| Densidade | 0.992 g cm−3 |
| Ponto de fusão |
175-177 °C, 271 K, -112 °F |
| Ponto de ebulição |
209 °C, 482 K, 408 °F |
| Solubilidade em água | 1.2 g dm−3 |
| Solubilidade em acetona | ~2500 g dm−3 |
| Solubilidade em ácido acético | ~2000 g dm−3 |
| Solubilidade em dietil éter | ~2000 g dm−3 |
| Solubilidade em clorofórmio | ~1000 g dm−3 |
| Solubilidade em etanol | ~1000 g dm−3 |
| log P | 2.089 |
| Pressão de vapor | 4 mmHg (a 70 °C) |
| Rotação quiral [α]D | +44.1° |
| Susceptibilidade magnética | -103·10−6 cm3/mol |
| Farmacologia | |
| Código ATC | C01 |
| Riscos associados | |
| Classificação UE | |
| NFPA 704 | |
| Frases R | R11 R22 R36/37/38 |
| Frases S | S16 S26 |
| Limites de explosividade | 0.6%-3.5%[3] |
| EUA Limite de exposição permissível (PEL) |
TWA 2 mg/m3[3] |
| LD50 | 1310 mg/kg (oral, rato)[4] |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Cânfora é uma substância semi-sólida cristalina e cerosa, com um forte e penetrante odor acre. É um terpenoide com a fórmula química C10H16O, inicialmente extraído da árvore Cinnamomum camphora, mas presentemente em boa parte obtido por síntese química.
Descrição
A cânfora é uma substância é cerosa, branca ou transparente, com um odor forte e aromático,[5] presente em diversas plantas, com destaque para as pertencentes à ordem Laurales. A sua fonte inicial foi a madeira da canforeira, Cinnamomum camphora, uma árvore perene originária do Sueste Asiático. O composto é industrialmente sintetizado a partir do óleo de terebintina e é usado como bálsamo e com outros propósitos medicinais.
História
O vocábulo «cânfora» provavelmente deriva da latinização da palavra árabe al-kafur, que por sua vez deriva do malaio kapur Barus que significa "giz de Barus". Naquele tempo era aos comerciantes malaios que os comerciantes indianos compravam a cânfora, os quais a designavam por kapur, "giz", devido à sua coloração esbranquiçada. Barus era um porto situado na costa oeste da ilha de Samatra, de donde os comerciantes o traziam. Em sânscrito a palavra karpūram é usada para designar a cânfora.
O moderno estudo químico da cânfora foi iniciado por Nicolas-Théodore de Saussure, continuado posteriormente por Justus von Liebig, Jean-Baptiste Dumas e Théophile-Jules Pelouze. Foi Pelouze quem obteve pela primeira vez a cânfora sintética, obtida em 1840 oxidando a cânfora do Bornéu. Marcellin Berthelot conseguiu a síntese pela oxidação do canfeno em 1859, determinando a sua composição química.
A primeira síntese integral da cânfora, a partir de compostos simples, foi conseguida por Gustav Komppa em 1903. Previamente alguns compostos orgânicos (como a ureia) tinham sido sintetizados em laboratório como prova conceptual, mas a cânfora era um produto natural escasso e com uma grande procura em todo o mundo, pelo que Komppa iniciou a sua produção industrial em Tainionkoski (Finlândia) em 1907, sendo a primeira síntese totalmente industrial de um produto vegetal.
O produto conhecido por noralcanfor é um derivado da cânfora por substituição dos três grupos metilo por hidrogénio.
Usos
Os usos modernos da cânfora são múltiplos: para além dos usos farmacológicos, é utilizada como plastificante do nitrato de celulose, como repelente de traças, como substância antimicrobiana, como bálsamo e em pirotecnia. Os cristais de cânfora são usados para prevenir os danos provocado por insectos nas colecções de insectos e em herbários. Uma forma de gel anti-comichão comum utiliza cânfora como princípio activo.
A cânfora é rapidamente absorvida pela pele, produzindo uma sensação de resfriamento similar à do mentol e actua como um anestésico local leve e como antimicrobiano. Pode ser administrado em pequenas quantidades (50 mg) para sintomas de fatiga e sintomas cardíacos menores.
É usado como saborizante de doces na Índia e na Europa.
No ritual pūja de origem hindu, é utilizada para acender o fogo que finaliza a cerimónia.
É utilizado em forma de pastilhas ou geles como repelente de animais, geralmente domésticos, como cães e gatos, que costumam marcar o seu território, já que cânfora nas zonas de marcação do território, se favorece o seu afastamento da zona.
A cânfora possui acção rubefaciente, antipruriginosa, antisséptica e ligeiramente analgésica. O produto é em geram empregue sob a forma de linimentos, soluções alcoólicas (sob o nome de álcool canforado) e unguentos e pomadas, como revulsivo em dores articulares, musculares, neuralgias e outras afecções similares.
Administrado por via sistémica apresenta propriedades irritantes e carminativas, utilizando-se como um expectorante suave. A cânfora é muito utilizada em fórmulas para descongestão nasal, ainda que a sua eficácia seja duvidosa.
O uso de óleos canforados está desaconselhado, por ser potencialmente tóxico (aumenta a absorção da cânfora). Foi também utilizado como estimulante e como sedante, por via interna. Segundo o Comité para la Revisión de Medicamentos (Espanha), a cânfora não deve ser incluída na composição de preparados destinados ao tratamento de transtornos hepáticos e biliares, cálculos biliares, cólicas, alterações renais, infecções do tracto urinário ou cálculos uretrais. O seu emprego por via parenteral ou em irrigação não é aconselhável, devido aos efeitos adversos.[6]
Referências
- ↑ The Merck Index, 7th edition, Merck & Co., Rahway, New Jersey, USA, 1960
- ↑ Handbook of Chemistry and Physics, CRC Press, Ann Arbor, Michigan, USA
- ↑ a b Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as refs de nomePGCH - ↑ «Camphor (synthetic)». National Institute for Occupational Safety and Health (NIOSH). 4 December 2014. Consultado em 19 February 2015 Verifique data em:
|acessodata=, |data=(ajuda) - ↑ Mann JC, Hobbs JB, Banthorpe DV, Harborne JB (1994). Natural products: their chemistry and biological significance. Harlow, Essex, England: Longman Scientific & Technical. pp. 309–11. ISBN 0-582-06009-5
- ↑ Ficha Técnica: Alcanfor - Cristal Sintético.


