Peroxissoma
| Biologia celular |
|---|
| Célula animal |
|
Organelos da célula animal |
| Célula vegetal |
|
Organelos da célula vegetal 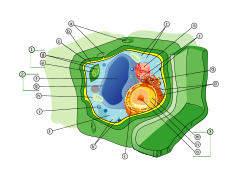
1. Cloroplasto
2. Vacúolo
3. Núcleo
|
|
Portal Biologia celular Portal Biologia |
Peroxissoma (português de Portugal), Peroxissomo (português do Brasil) é um organelo envolvido por uma membrana (conhecido antigamente como microcorpo) e presente no citoplasma de quase todas as células eucarióticas.[1][2] São organelos com atividade de síntese e decomposição de peróxido de hidrogénio, tendo esta caraterística dado o nome a estes organelos. Frequentemente, o oxigénio molecular é necessário para a atividade catalítica de muitas enzimas do organelo, a partir do qual, o peróxido de hidrogénio (H2O2) é formado (substância altamente tóxica para a célula). Nos peroxissomas, por meio da enzima catalase, o H2O2 é convertido em oxigénio molecular (O2) e água (H2O).[3][4][5] Os peroxissomas desempenham papéis-chave no metabolismo lípidico e na conversão de espécies reativas de oxigénio. Os peroxissomas estão envolvidos no catabolismo de ácidos gordos de cadeia muito longa (VLCFA, pelo ingês Very Long Chain Fatty Acids, isto é, ácidos gordos com 24 ou mais átomos de carbono), ácidos gordos de cadeia ramificada, intermediários de ácidos biliares (no fígado), D-aminoácidos, e poliaminas;[6] na redução de espécies reativas de oxigénio - especificamente peróxido de hidrogénio[3] - e na biossíntese de plasmogénios, isto é, fosfolípidos éter necessários para o normal funcionamento do cérebro e pulmões dos mamíferos.[7] Os peroxissomas também contêm aproximadamente 10% da atividade total de duas enzimas (Glicose-6-fosfato dehidrogenase e 6-fosfogliconato dehidrogenase) na via pentose-fosfato,[7][8] que é importante para o metabolismo energético. Se os peroxissomas estão envolvidos na síntese de isoprenóides e colesterol em animais ainda é assunto em debate.[7]
Outras funções conhecidas incluem o ciclo do glioxilato no germinar de sementes ("glioxissomas")[carece de fontes], na fotorespiração de folhas,[9] glicólise em trypanosomas ("glicossomas") e na oxidação de metanol e/ou aminas e na assimilação de algumas leveduras.
As investigações neste campo tem sido intensas nas últimas duas décadas.
História[editar | editar código-fonte]
Os peroxissomas foram descritos, pela primeira vez, por um estudante de doutoramento sueco, J. Rhodin (1954),[10] em células de rato, sendo então designados por microcorpos (microbodies). Contudo, a sua caraterização bioquímica ficou a dever-se ao citologista belga Christian De Duve e colaboradores.[11] Em 1966, De Duve propôs a designação de peroxissoma em substituição de microbodies, salientando a existência simultânea de duas classes de enzimas: oxidases produtoras de peróxido de hidrogénio e catalase. Posteriormente, os peroxissomas foram identificados em diversas células animais e vegetais.
Mais tarde, foi descrito que a enzima luciferase firefly localiza-se nos peroxissomas em células de mamífero, permitindo a descoberta de um sinal de importe para peroxissomas, o que contribui para avanços na área da biogénese dos peroxissomas.[12][13]
Origem Evolucionária[editar | editar código-fonte]
Ainda é um tópico muito debatido e várias hipóteses são levantadas para explicar o surgimento dos peroxissomas, alguns pesquisadores afirmam que eles surgiram de forma similar aos cloroplastos e às mitocôndrias, por meio de endossimbiose com um organismo procariótico que perdeu seu material genético e independência com o tempo.[14] Um dos possíveis seres que originou o peroxissoma poderia ser do grupo das actinobactérias.[15] Já outros pesquisadores acreditam na hipótese da formação espontânea dos peroxissomas a partir do retículo endoplasmático[16][17] com o possível recrutamento de enzimas que eram originalmente mitocondriais.[17]
É muito provável que os peroxissomas atuais sejam somente vestígios de um organelo ancestral que realizava o metabolismo completo do oxigénio nas células eucarióticas primitivas, mas com a endossimbiose da célula com a mitocôndria, que não só lidava com o oxigénio como também acoplava a produção de energia a estes processos, as funções do peroxissoma primitivo se tornaram obsoletas e só se mantiveram aquelas que eram exclusivas do organelo (não competiam com a mitocôndria).[5]
Caraterização[editar | editar código-fonte]
Os peroxissomas são pequenos (0.1-1µm) compartimentos subcelulares (organelos), geralmente geralmente menores que as mitocôndrias, rodeados por uma única membrana, localizadas no citoplasma da célula.[18][19] A sua matriz apresenta-se, habitualmente, com uma textura finamente granular e contendo um corpo denso no qual se reconhece uma estrutura cristalina, designado por cristalóide ou core. O cristalóide resultaria da cristalização progressiva da catalase ou das oxidases existentes na matriz. A compartimentalização cria um ambiente ótimo para promover diversas reações metabólicas peroxissomais necessárias para manter as funções celulares e a viabilidade do organismo.
O número, tamanho e composição proteica dos peroxissomas são variáveis e dependentes do tipo de célula e das condições ambientais. Por exemplo, na S. Cerevisae foi observado que com um bom suplemento de glucose, apenas poucos e pequenos peroxissomas estavam presentes, Pelo contrário, quando às leveduras foi adicionado um suplemento com ácidos gordos de cadeia longa como fonte de carbono foram formados cerca de 20-25 grandes peroxissomas.[4][20]
Controlo da abundância na célula[21][editar | editar código-fonte]
As células são equipadas com mecanismos que coordenam a formação e a degradação de novos organelos, caso estejam presentes em excesso ou disfuncionais.
Formação:
- Formação de novo:
- pelo retículo endoplasmático sob determinadas condições
- pela fusão de vesículas derivadas de mitocôndria e pré-peroxissomas derivados do retículo endoplasmático.
- Divisão de organelos preexistentes.
As proteínas da matriz dos peroxissomas são traduzidas no citoplasma antes do seu importe. Sequências específicas de aminoácidos - Ser-Lys-Leu-COO - (PTS, peroxisomal targeting signal) no C-terminal (PTS1) ou no N-terminal (PTS2) sinalizam as proteínas da matriz para que estas sejam importadas para a matriz através de um fator alvo.[22] Existem atualmente 36 proteínas conhecidas que estão envolvidas na formação e manutenção dos peroxissomas, as chamadas peroxinas,[23] que participam no processo de formação dos peroxissomas em diferentes organismos. Em células de mamíferos existem 13 peroxinas caraterizadas. Em contraste ao importe de proteínas para o retículo endoplasmático ou mitocôndria, as proteínas não precisam de ser unfolded para serem importadas para o lumen peroxissomal. Os recetores de importe das proteínas da matriz, as peroxinas PEX5 e PEX7, acompanham as cargas (que contêm as sequências de aminácidos PTS1 e PTS2, respetivamente) até aos peroxissomas, mais precisamente para a matriz. Depois, PEX5 e PEX7 regressam para o citosol - um processo chamado de reciclagem.[24]
O modelo que descreve o ciclo de importe é referido como um "mecanismo de shuttle extensivo". Existem evidências que a hidrólise de ATP é necessária para a reciclagem dos recetores para o citosol. Além disso, a ubiquitinação é crucial para a exportação da PEX5 para o citosol a partir dos peroxissomas. A biogénese da membrana peroxissomal e a inserção de proteínas da membrana dos peroxissomas requerem as peroxinas PEX19, PEX3 e PEX16. PEX19 é um recetor e chaperona das proteínas da membrana, que leva as proteínas até à membrana peroxissomal, onde interage com a PEX3, uma proteína integral da membrana dos peroxissomas.
Degradação:
- Pela via da autofagia lisossómica, a chamada pexofagia.[25]
Controlo transcricional[21][editar | editar código-fonte]
Os peroxissomas possuem mecanismos transcricionais que coordenam sua abundância e as suas enzimas.
A expressão de genes envolvidos com a beta-oxidação de ácidos gordos e com a proliferação dos peroxissomas é realizada por fatores de transcrição da família PPAR.
- PPAR (peroxisome proliferator-activated receptor): receptores nucleares que agem em conjunto com RXRs (retinoid X receptors) para regular funções fisiológicas (metabolismo de lipídos e carbohidratos, diferenciação celular e formação de tumores.)
- Agonistas de PPARs: lipídos alimentares e seus metabolitos, fibratos.
- Cada subtipo de PPAR possui um padrão de expressão tecidual, especificidade a um substrato e é responsável por regular a expressão de diferentes genes.
- PPARs são modulados por proteínas co-ativadoras (PGC-1alfa) e co-repressoras (NCOR).
- PGC-1alfa: grande indutor da biogénese mitocondrial e da sua funcionalidade.
- Esse co-ativador contribui para uma variedade de outros recetores nucleares diferentes do PPAR, como por exemplo, NRFs (nuclear respiratory factor) para promover uma melhor expressão de genes que atuam na biogénese mitocondrial, em enzimas antioxidantes, etc.
- PGC-1alfa também atua na regulação positiva da biogénese de peroxissomas em vários tecidos, como no fígado e músculos esqueléticos. Esse processo não precisa do PPARalfa para ser realizado.
Logo, a abundância e a atividade peroxissomal são reguladas a nível transcricional, num mecanismo dependente de PPAR e de PGC-1alfa.
Funções[editar | editar código-fonte]
A maior função dos peroxissomas é a degradação de ácidos gordos de cadeia longa através da beta-oxidação. Em células animais, os ácidos gordos de cadeia longa através da beta-oxidação. Em células animais, os ácidos gordos de cadeia longa são convertidos em ácidos gordos de cadeia média, que são subsequentemente transportados para a mitocôndria, onde são eventualmente degradados em dióxido de carbono e água. Em leveduras e plantas, este processo é realizado apenas pelos peroxissomas.[26][27]
O peroxissoma também atua na síntese de substâncias para a célula, sendo um dos possíveis sítios para a formação de colesterol (o retículo endoplasmático é o outro), de plasmogénios (estruturas de função debatida encontrados na bainha de mielina e tecido cardíaco e respiratório),[26] de açúcares a partir de ácidos gordos (ocorre em plantas pelo ciclo do glioxilato e é de vital importância para a semente) e de subprodutos da fotossíntese, aproveitando-se do CO2 libertado na reação (esse processo ocorre pelo ciclo de Calvin).[4]
As vias metabólicas específicas que ocorrem exclusivamente nos peroxissomas de mamíferos são[7]:
- alfa-oxidação de ácido fitânico
- beta-oxidação dos ácidos gordos de cadeia longa/muita longa e polinsaturados
- biossíntese de plasmogénios
- conjugação de ácido cólico como parte da síntese de ácido biliar
A sua função de oxidação é realizada de enzimas, tais como as de D-aminoácido e urato oxidase[28] que são usadas para oxidar certas moléculas dentro do organelo, levando à produção de peróxido de hidrogénio (H2O2) (primeira equação). Já que H2O2 pode causar danos à célula ele precisa de ser degradado ou ser utilizado para oxidar alguma outra substância e esse processo é realizado pela enzima catalase, que usa H2O2 para oxidar outros substratos, como fenóis, ácido fórmico, formaldeído e álcool (segunda equação). Exemplos de compostos quebrados no peroxissomas são aminoácidos, ácido úrico e ácidos gordos.
Em certas plantas, os peroxissomas contêm também um complexo de enzimas antioxidantes como a superóxido dismutase, componentes do ciclo de ascobarto-glutationa e a NADP-dehidrogenase da via de pentose-fosfato. Foi demonstrado que os peroxissomas geram radicais de superóxido e óxido nítrico.[29][30] Também em plantas, os peroxissomas participam na fotorrespiração e promovem a conversão de lípidos em glícidos, aquando da germinação de sementes e oleaginosas.
Existem evidências que as espécies reativas de oxigénio incluindo o H2O2 peroxissomal são importantes moléculas sinalizadoras em plantas e animais e contribuem para o envelhecimento e doenças relacionadas com a idade em humanos[31].
Os peroxissomas em mamíferos e humanos também contribuem para a defesa antiviral[32] e para o combate de patogénios[33].
Interação e Comunicação com outros organelos[editar | editar código-fonte]
As diversas funções dos peroxissomas requerem interações dinâmicas e cooperação com muitos organelos envolvidos no metabolismo lipídico tais como o retículo endoplasmático, a mitocôndria, lisossomas.[34]
Os peroxissomas interagem com a mitocôndria em diversas vias metabólicas, incluindo a beta-oxidação de ácidos gordos e no metabolismo de espécies reativas de oxigénio.[7] Ambos os organelos estão em proximidade com o retículo endoplasmático e partilham algumas proteínas, incluindo fatores de divisão dos organelos.[35] Os peroxissomas também interagem com o retículo endoplasmático e cooperam na síntese de éter lípidos (plasmogénios) que são importantes para as células nervosas. O contacto físico entre organelos é muitas vezes mediado por locais de contacto de membranas, onde as membranas de dois organelos estão fisicamente ligados para permitir a transferência rápida de pequenas moléculas, havendo comunicação de organelos e são cruciais para a coordinação de funções celulares e consequentemente a saúde humana.[36] Alterações netes contactos são observados em diversas doenças.
Peroxissoma - mitocôndria[21][editar | editar código-fonte]
- β oxidação de ácidos gordos;
- Síntese de ácidos biliares;
- Detoxificação de glioxilato;
- Manutenção da homeostase de espécies reativas de oxigénio.
β-oxidação de ácidos gordos[editar | editar código-fonte]
Especificidade de substratos: ácidos gordos de cadeia longa são preferencialmente oxidados no peroxissoma.
- Primeira etapa da reação:
Para manter a beta oxidação no peroxissoma, é crucial a reoxidação de NADH em NAD+ na mitocôndria, para que possa continuar a servir como aceitador de eletrões nessa via metabólica celular.
Metabolismo de espécies reativas de oxigénio[editar | editar código-fonte]
Importante papel do peroxissoma no catabolismo de H2O2: como por exemplo a catalase.
Várias vias metabólicas do organelo produzem naturalmente o peróxido de hidrogénio (H2O2), e, em certos tecidos, também superóxido e ácido nítrico.
Para evitar danos oxidativos pelo acúmulo dessas espécies reativas, os peroxissomas possuem, além da catalase, outros sistemas antioxidantes enzimáticos (como a peroxiredoxina-5 e superoxidodesmutase 1) e não enzimáticos (como a vitamina C e glutationa).
A quantidade de espécies reativas de oxigénio liberadas pelo peroxissoma depende do estado fisiológico e do ambiente de crescimento da célula, podendo o organelo atuar tanto como fonte ou escoamento desses compostos.
Interação com a mitocôndria[editar | editar código-fonte]
Ambos possuem grande sensibilidade à variação oxidativa da célula e defeitos no peroxissoma podem causar grande stress oxidativo na mitocôndria. Uma maior atividade da catalase, por outro lado, protege a mitocôndria e melhora o desempenho das suas funções.
Comunicação[21][editar | editar código-fonte]
A comunicação existente entre esses dois organelos pode ocorrer de três maneiras: contato físico, transporte de vesículas e mensageiros biológicos. O contato físico é estabelecido pela aproximação das membranas, e a maneira e frequência com que é estabelecido depende do tipo celular e das condições fisiológicas em que a célula está inserida. Evidências recentes da existência desse contato foram obtidas por meio de estudos com microscopia confocal e da densidade analítica do gradiente de centrifugação obtido a partir de frações de fígado de rato.
Em hepatócitos humanos, foi identificado que a interação entre peroxissomas e mitocôndrias foi acentuada pela ativação da via da proteína 1 do gene RIG, o que configura uma descoberta em potencial e que necessita de pesquisas mais aprofundadas. Recentemente, foi identificado em mamíferos um complexo proteico denominado enoilCoA isomerase 2 (ECI2), a qual apresenta um domínio de acetilCoA cuja extremidade N-terminal é voltada para a mitocôndria e a extremidade C-terminal é voltada para o peroxissoma. A expressão desse complexo proteico em células tumorais de Leydig tem sido reportada como responsável por promover a aposição e contato físico entre as membranas desses dois organelos.
Além disso, essa comunicação pode ser feita mediante transporte de vesículas, as quais são originadas a partir de mitocôndrias (por isso denominadas mitochondria-derived vesicles, as MDVs) e endereçadas a uma subpopulação de peroxissomas. Essas MDVs, por sua vez, ao se fundirem com vesículas derivadas do Retículo Endoplasmático, formam estruturas intracelulares que se maturam em peroxissomas funcionais. Por fim, essa comunicação também pode ser feita por meio de mensageiros biológicos, os quais carregam informação de um organelo a outra usando moléculas como: lípidos, espécies reativas de oxigénio (ROS) e metabolitos.
Sinalização[21][editar | editar código-fonte]
As atividades metabólicas peroxissómicas e mitocondriais são estreitamente interligadas, reforçando a ideia de que esses organelos desenvolveram estratégias para comunicar os seus níveis de atividade metabólica entre si.
De maneira análoga a outras vias de sinalização mitocondriais, essas estratégias de comunicação podem incluir: (i) a libertação de biomoléculas (proteínas, ROS/RNS ou metabolitos) que direta ou indiretamente modulam a função do outra organelo; ou (ii) a ativação de complexos de membrana associados que coordenam a atividade de ambos.
O H2O2 (peróxido de hidrogénio) atua como molécula de sinalização por meio da oxidação de resíduos desprotonados de cisteína que são altamente conservados em várias proteínas de sinalização, como: reguladores transcricionais, cinases, fosfatases, proteínas estruturais. Após a oxidação, ocorre uma instável formação de pontes dissulfeto. Essa formação reversível regula a atividade proteica, localização e / ou interação com outras biomoléculas. Logo, mudanças no fluxo de H2O2 podem afetar vários processos celulares, considerando que essa molécula atravessa rapidamente as membranas dos dois organelos.
Tanto os peroxissomas quanto as mitocôndrias desempenham um papel central no metabolismo dos lípidos celulares. Dessa forma, as mudanças no metabolismo lipídico de um organelo influenciam a função da outra. Níveis elevados de oxidação de ácidos gordos peroxissomais podem induzir défice multifacetados nas mitocôndrias. Além disso, a oxidação prejudicada de ácido gordo mitocondrial leva a um aumento compensatório na oxidação de ácidos gordos peroxissomais.
O equilíbrio redox mitocondrial, por sua vez, é rapidamente perturbado pela geração de excesso de ROS dentro dos peroxissomas. Por outro lado, os peroxissomas resistem amplamente ao stress oxidativo quando a carga se origina dentro das mitocôndrias. A comunicação redox entre peroxissomas e mitocôndrias, no entanto, envolve sinalização complexa a ser esclarecida.
Importância Fisiológica[21][editar | editar código-fonte]
Deficiência funcional: Devido à ligação entre a mitocôndria e o peroxissoma, um defeito na função de um organelo facilmente impacta a outra. Por exemplo, na Esteatohepatite microvesicular, ocorre inativação da Acil-CoA oxidase 1 (ACOX 1) no peroxissoma, o que gera um acúmulo dos lípidos não metabolizados por essa enzima. Esse acúmulo na célula leva a uma ativação sustentada da PPAR α (fator de transcrição), que, por sua vez, induz a expressão de enzimas oxidantes do citocromo, responsáveis pela transformação de ácidos gordos de cadeia longa em ácidos dicarboxílicos. Entretanto, esses compostos são normalmente degradados no peroxissoma, que está com a sua função comprometida, ocasionando uma acumulação desses ácidos gordos a concentrações suficientes para desacoplar a fosforilação oxidativa na mitocôndria.
Deficiência na maquinaria de fissão: Levam a um decréscimo do número de mitocôndrias e peroxissomas por comprometer a divisão e formação de novos organelos, o que pode gerar diversas doenças neurodegenerativas.
Infecções virais: O peroxissoma, juntamente com a mitocôndria, é capaz de auxiliar no combate a infecções virais por meio da via RLM-MAVS (receptores de reconhecimento de RNA estrangeiro e proteínas adaptadoras a eles, presentes na membrana de ambos os organelos).
A proteína X do vírus da hepatite B, por exemplo, que causa hepatocarcinoma, liga-se à MAVS e desencadeia respostas de defesa em mitocôndrias e peroxissomas, como a produção de radicais oxigenados e ativação de NF-kB, um fator de transcrição responsável por promover a regulação da resposta imune. Esse mecanismo é tão importante que diversos vírus possuem mecanismos para silenciar esse sistema, como o vírus da dengue, que prejudica a biogénese peroxissomal para evitar a indução de INF III (proteína de resposta imune).
Envelhecimento: Disfunções nos dois organelos podem levar a envelhecimento e doenças associadas.
Investigadores propõem que os peroxissomas atuam como "guardiões" da capacidade mitocondrial durante o envelhecimento celular, por meio de homeostase, principalmente, de radicais oxigenados. Pesquisas demonstraram que a restauração da catalase em fibroblastos envelhecidos reverte a despolarização mitocondrial e atrasa o aparecimento de marcadores de células senescentes, como a β galactosidase.
Além disso, foi demonstrado que a proliferação de peroxissomas e alta atividade antioxidante protegem núcleos hipocampais do peptídeo β amilóide, responsável pela Doença de Alzheimer, ao causar disfunções mitocondriais, neurotoxicidade e morte celular.
Doenças peroxissomais: conjunto de condições médicas que tipicamente afetam o sistema nervoso humano bem como muitos outros órgãos. Dois exemplos comuns são adrenoleucodistrofia associada ao cromossoma X (ALD-X) e desordens na biogénese dos peroxissomas, por exemplo Síndrome de Zellweger.[37][38] Esta última é uma doença congénita, descrita clinicamente pela primeira vez em 1964, que afeta o cérebro, fígado, glândula adrenal, ossos e rins. Já a ALD é devido a defeitos nas enzimas peroxissomais que levam a falhas metabólicas onde a presença de enzimas não-funcionais leva à acumulação de ácidos gordos de cadeia longa nos tecidos, causando complicações patológicas, principalmente para o sistema nervoso.[39]
Genes[carece de fontes][editar | editar código-fonte]
Os genes PEX codificam a maquinaria da proteína (peroxinas) necessárias para a formação correta dos peroxissomas, como descrito anteriormente. A formação da membrana e a manutenção requerem três destes (peroxinas 3, 16 e 19) e podem ocurrer sem o importe das enzimas da matriz (lumen). A proliferação do organelo é regulada pela Pex11.
Os genes que codificam peroxinas incluem: PEX1, PEX2 (PXMP3), PEX3, PEX5, PEX6, PEX7, PEX9, PEX10, PEX11A, PEX11B, PEX11G, PEX12, PEX13, PEX14, PEX16, PEX19, PEX26, PEX28, PEX30 e PEX31. Entre organismos, o número e a função dos PEX podem mudar.
Referências
- ↑ Gabaldón, Toni (12 de março de 2010). «Peroxisome diversity and evolution». Philosophical Transactions of the Royal Society B: Biological Sciences. 365 (1541): 765–773. ISSN 0962-8436. PMID 20124343. doi:10.1098/rstb.2009.0240
- ↑ Islinger, Markus; Voelkl, Alfred; Fahimi, H. Dariush; Schrader, Michael (novembro de 2018). «The peroxisome: an update on mysteries 2.0». Histochemistry and Cell Biology (em inglês). 150 (5): 443–471. ISSN 0948-6143. PMC 6182659
 . PMID 30219925. doi:10.1007/s00418-018-1722-5
. PMID 30219925. doi:10.1007/s00418-018-1722-5
- ↑ a b Bonekamp, Nina A.; Völkl, Alfred; Fahimi, H. Dariush; Schrader, Michael (julho de 2009). «Reactive oxygen species and peroxisomes: Struggling for balance». BioFactors (em inglês). 35 (4): 346–355. doi:10.1002/biof.48
- ↑ a b c Cooper, Geoffrey M. (1 de janeiro de 2000). «Peroxisomes» (em inglês)
- ↑ a b Molecular biology of the cell. [S.l.]: Garland Science. 1 de janeiro de 2008
- ↑ Manuela Martinez et al Am J Clin Nutr 2000;71(suppl):376-385
- ↑ a b c d e Wanders, Ronald J. A.; Hans R. (1 de janeiro de 2006). «Biochemistry of mammalian peroxisomes revisited». Annual Review of Biochemistry. 75: 295–332. ISSN 0066-4154. PMID 16756494. doi:10.1146/annurev.biochem.74.082803.133329
- ↑ Antonenkov, Vasily D. (julho de 1989). «Dehydrogenases of the pentose phosphate pathway in rat liver peroxisomes». European Journal of Biochemistry (em inglês). 183 (1): 75–82. ISSN 0014-2956. doi:10.1111/j.1432-1033.1989.tb14898.x
- ↑ Evert, Ray Franklin.; Esau, Katherine. (2006). Esau's Plant anatomy : meristems, cells, and tissues of the plant body : their structure, function, and development 3 ed. Hoboken, N.J.: Wiley-Interscience. ISBN 0-471-73843-3. OCLC 70265585
- ↑ "Correlation of ultrastructural organization and function in normal and experimentally changed proximal tubule cells of the mouse kidney". Doctorate Thesis. Karolinska Institutet, Stockholm.
- ↑ de Duve, C. (15 de abril de 1969). «The peroxisome: a new cytoplasmic organelle». Proceedings of the Royal Society of London. Series B, Biological Sciences. 173 (1030): 71–83. ISSN 0950-1193. PMID 4389648
- ↑ Keller, G. A.; Gould, S.; Deluca, M.; Subramani, S. (1 de maio de 1987). «Firefly luciferase is targeted to peroxisomes in mammalian cells.». Proceedings of the National Academy of Sciences (em inglês). 84 (10): 3264–3268. ISSN 0027-8424. PMC 304849
 . PMID 3554235. doi:10.1073/pnas.84.10.3264
. PMID 3554235. doi:10.1073/pnas.84.10.3264
- ↑ Gould, S. J. (1 de setembro de 1988). «Identification of peroxisomal targeting signals located at the carboxy terminus of four peroxisomal proteins». The Journal of Cell Biology (em inglês). 107 (3): 897–905. ISSN 0021-9525. PMC 2115268
 . PMID 2901422. doi:10.1083/jcb.107.3.897
. PMID 2901422. doi:10.1083/jcb.107.3.897
- ↑ Lazarow, P. B.; Y. (1 de janeiro de 1985). «Biogenesis of peroxisomes». Annual Review of Cell Biology. 1: 489–530. ISSN 0743-4634. PMID 3916321. doi:10.1146/annurev.cb.01.110185.002421
- ↑ Duhita, Narendra; Huyen Ai Thuy (15 de janeiro de 2010). «The origin of peroxisomes: The possibility of an actinobacterial symbiosis». Gene. 450 (1-2): 18–24. ISSN 1879-0038. PMID 19818387. doi:10.1016/j.gene.2009.09.014
- ↑ Schlüter, Agatha; Stéphane (1 de abril de 2006). «The evolutionary origin of peroxisomes: an ER-peroxisome connection». Molecular Biology and Evolution. 23 (4): 838–845. ISSN 0737-4038. PMID 16452116. doi:10.1093/molbev/msj103
- ↑ a b Gabaldón, Toni; Berend (23 de março de 2006). «Origin and evolution of the peroxisomal proteome». Biology Direct. 1. 8 páginas. ISSN 1745-6150. PMID 16556314. doi:10.1186/1745-6150-1-8
- ↑ Karlson, Peter. (2005). Karlsons Biochemie und Pathobiochemie. 15., komplett überarb. und neugestaltete Aufl ed. Stuttgart: Thieme. ISBN 3-13-357815-4. OCLC 181474420
- ↑ Raven, Peter H.; Eichhorn, Susan E. (2006). Biologie der Pflanzen 4. Aufl ed. Berlin: De Gruyter. ISBN 978-3-11-018531-7. OCLC 180904366
- ↑ Feldmann, Horst (Cytologist) (2010). Yeast : molecular and cell biology. Weinheim: Wiley-VCH. ISBN 978-3-527-32609-9. OCLC 489629727
- ↑ a b c d e f Fransen M, Lismont C, Walton P. The Peroxisome-Mitochondria Connection: How and Why? Renard P, ed. International Journal of Molecular Sciences. 2017;18(6):1126. doi:10.3390/ijms18061126.
- ↑ Gregory J. Gatto, Jr., Brian V. Geisbrecht, Stephen J. Gould and Jeremy M. Berg. Department of Biophysics and Biophysical Chemistry and Department of Biological Chemistry, The Johns Hopkins University School of Medicine, Baltimore, Maryland 21205, USA.
- ↑ Saleem, R.A.; Smith, J.J.; Aitchison, J.D. (dezembro de 2006). «Proteomics of the peroxisome». Biochimica et Biophysica Acta (BBA) - Molecular Cell Research (em inglês). 1763 (12): 1541–1551. PMC 1858641
 . PMID 17050007. doi:10.1016/j.bbamcr.2006.09.005
. PMID 17050007. doi:10.1016/j.bbamcr.2006.09.005
- ↑ Thoms, Sven (novembro de 2015). «Import of proteins into peroxisomes: piggybacking to a new home away from home». Open Biology (em inglês). 5 (11). 150148 páginas. ISSN 2046-2441. PMC 4680570
 . PMID 26581572. doi:10.1098/rsob.150148
. PMID 26581572. doi:10.1098/rsob.150148
- ↑ Eberhart, Tanja; Kovacs, Werner J. (novembro de 2018). «Pexophagy in yeast and mammals: an update on mysteries». Histochemistry and Cell Biology (em inglês). 150 (5): 473–488. ISSN 0948-6143. doi:10.1007/s00418-018-1724-3
- ↑ a b Alberts, Bruce; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002). Molecular biology of the cell 4 ed. New York: Garland Science. ISBN 0-8153-3218-1. OCLC 48122761
- ↑ Schrader, Michael; Kamoshita, Maki; Islinger, Markus (16 de abril de 2019). «Organelle interplay-peroxisome interactions in health and disease». Journal of Inherited Metabolic Disease (em inglês). doi:10.1002/jimd.12083
- ↑ del Río, Luis A.; Sandalio, Luisa M.; Palma, JoséM.; Bueno, Pablo; Corpas, Francisco J. (novembro de 1992). «Metabolism of oxygen radicals in peroxisomes and cellular implications». Free Radical Biology and Medicine (em inglês). 13 (5): 557–580. doi:10.1016/0891-5849(92)90150-F
- ↑ Corpas, Francisco J; Barroso, Juan B; del Rı́o, Luis A (abril de 2001). «Peroxisomes as a source of reactive oxygen species and nitric oxide signal molecules in plant cells». Trends in Plant Science (em inglês). 6 (4): 145–150. doi:10.1016/S1360-1385(01)01898-2
- ↑ Corpas, Francisco J.; Barroso, Juan B.; Carreras, Alfonso; Quirós, Miguel; León, Ana M.; Romero-Puertas, María C.; Esteban, Francisco J.; Valderrama, Raquel; Palma, José M. (setembro de 2004). «Cellular and Subcellular Localization of Endogenous Nitric Oxide in Young and Senescent Pea Plants». Plant Physiology (em inglês). 136 (1): 2722–2733. ISSN 0032-0889. PMC 523336
 . PMID 15347796. doi:10.1104/pp.104.042812
. PMID 15347796. doi:10.1104/pp.104.042812
- ↑ Lismont C, Revenco I, Fransen M (July 2019). "Peroxisomal Hydrogen Peroxide Metabolism and Signaling in Health and Disease". International Journal of Molecular Sciences. 20 (15): 3673. doi:10.3390/ijms20153673. PMC 6695606. PMID 31357514.
- ↑ Dixit E, Boulant S, Zhang Y, Lee AS, Odendall C, Shum B, et al. (May 2010). "Peroxisomes are signaling platforms for antiviral innate immunity". Cell. 141 (4): 668–81. doi:10.1016/j.cell.2010.04.018. PMC 3670185. PMID 20451243.
- ↑ Di Cara F, Bülow MH, Simmonds AJ, Rachubinski RA (November 2018). "Dysfunctional peroxisomes compromise gut structure and host defense by increased cell death and Tor-dependent autophagy". Molecular Biology of the Cell. 29 (22): 2766–2783. doi:10.1091/mbc.E18-07-0434. PMC 6249834. PMID 30188767.
- ↑ Shai, Nadav; Schuldiner, Maya; Zalckvar, Einat (maio de 2016). «No peroxisome is an island — Peroxisome contact sites». Biochimica et Biophysica Acta (BBA) - Molecular Cell Research (em inglês). 1863 (5): 1061–1069. PMC 4869879
 . PMID 26384874. doi:10.1016/j.bbamcr.2015.09.016
. PMID 26384874. doi:10.1016/j.bbamcr.2015.09.016
- ↑ Costello, Joseph L.; Passmore, Josiah B.; Islinger, Markus; Schrader, Michael (2018). del Río, Luis A.; Schrader, Michael, eds. «Multi-localized Proteins: The Peroxisome-Mitochondria Connection». Singapore: Springer Singapore. 89: 383–415. ISBN 978-981-13-2232-7. doi:10.1007/978-981-13-2233-4_17
- ↑ Castro, Inês Gomes; Schuldiner, Maya; Zalckvar, Einat (março de 2018). «Mind the Organelle Gap – Peroxisome Contact Sites in Disease». Trends in Biochemical Sciences (em inglês). 43 (3): 199–210. PMC 6252078
 . PMID 29395653. doi:10.1016/j.tibs.2018.01.001
. PMID 29395653. doi:10.1016/j.tibs.2018.01.001
- ↑ Depreter, Marianne; Espeel, Marc; Roels, Frank (1 de junho de 2003). «Human peroxisomal disorders». Microscopy Research and Technique (em inglês). 61 (2): 203–223. ISSN 1059-910X. doi:10.1002/jemt.10330
- ↑ Islinger, Markus; Grille, Sandra; Fahimi, H. Dariush; Schrader, Michael (maio de 2012). «The peroxisome: an update on mysteries». Histochemistry and Cell Biology (em inglês). 137 (5): 547–574. ISSN 0948-6143. doi:10.1007/s00418-012-0941-4
- ↑ Santos, Antonio Carlos dos (dezembro de 2014). «Adrenoleucodistrofia ligada ao X: diagnóstico e quantificação da progressão». Radiologia Brasileira. 47 (6): VII–VIII. ISSN 0100-3984. PMC 4341375
 . PMID 25741127. doi:10.1590/0100-3984.2014.47.6e2
. PMID 25741127. doi:10.1590/0100-3984.2014.47.6e2





