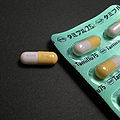
Oseltamivir
| Oseltamivir Alerta sobre risco à saúde | |
|---|---|

|

|
| |
| Nome IUPAC | ethyl (3R,4R,5S)-5-amino-4-acetamido-3-(pentan-3-yloxy)cyclohex-1-ene-1-carboxylate |
| Outros nomes | GS-4104; HSDB 7433; 1-Cyclohexene-1-carboxylic acid, 4-(acetylamino)-5-amino-3-(1-ethylpropoxy)-, ethyl ester, (3R-(3α,4β,5α))-. |
| Identificadores | |
| Número CAS | |
| PubChem | |
| DrugBank | DB00198 |
| ChemSpider | |
| MeSH | |
| ChEBI | |
| Código ATC | J05 |
| SMILES |
|
| DCB n° | 06650 |
| Primeiro nome comercial ou de referência | Tamiflu |
| Propriedades | |
| Fórmula química | C16H28N2O4 |
| Massa molar | 312.38 g mol-1 |
| Densidade | 1,08 g/cm3 |
| Ponto de fusão |
240 °C |
| Ponto de ebulição |
473.3 °C |
| Farmacologia | |
| Biodisponibilidade | 79 ± 12 (carboxilato) |
| Via(s) de administração | per os |
| Metabolismo | hepático |
| Meia-vida biológica | 6 a 10 horas (carboxilato) 1 a 3 horas (fosfato) |
| Excreção | Renal 93 ± 12 (carboxilato) e pequena parte nas fezes |
| Classificação legal | |
| Riscos associados | |
| Frases R | 36-43-52/53 |
| Frases S | 22-24-37-61 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Fosfato de oseltamivir é um pró-fármaco ester etil que possui atividade antiviral, onde após metabolização pelo fígado e trato gastrintestinal é transformado em carboxilato de oseltamivir (RO-64-0802) e assim torna-se seletivo contra o vírus influenza dos tipos A e B [1]. É produzido pelos laboratórios Roche sob o nome comercial Tamiflu®. O medicamento feito a partir deste princípio ativo foi o primeiro a ser usado na pandemia de gripe A que se iniciou em 2009 no México.[2] Foi classificado na lista C1 das outras substâncias sujeitas a controle especial da ANVISA, sujeita a receita de controle especial em duas vias, mas em 2012 a restrição foi removida pela RDC 30/2012 e o medicamento é vendido sem retenção de receita.[3]
Recebeu aprovação do FDA em dezembro de 2012, para o tratamento da gripe em crianças com no mínimo 2 semanas de idade. O estudo para a aprovação do medicamento envolveu 136 crianças e possui restrição na administração que é permitida por apenas dois dias.[4]
Rumor
Devido a pandemia, uma série de e-mails com informações duvidosas e falsas começaram a circular na Internet, prática conhecida como hoax. Algumas delas, diziam que o medicamento era fabricado a partir da planta anis estrelado e que o consumo desta poderia originar os mesmos efeitos do medicamento. De fato, o oseltamivir é produzido a partir do anis estrelado de quatro províncias chinesas, porém, é produzido através de um processo químico complexo, que envolve uma série de etapas, fora as outras substâncias que entram em sua composição.[5]
Versão em xarope
Em agosto de 2009 o Hospital Universitário de Brasília conseguiu produzir uma versão sob a forma farmacêutica xarope do oseltamivir, especialmente para crianças, que tem por via de regra dificuldades em ingerir comprimidos. Tem indicação para crianças menores de 12 anos com suspeita da doença. (lembrando que o medicamento é vendido no Brasil apenas sob prescrição médica, tendo em vista a escassa quantidade dos medicamentos).[6]
Propriedades
O fosfato de oseltamivir é considerado uma pró-droga, ou seja, ela é biotransformada dentro do organismo humano em carboxilato de oseltamivir. A principal característica de seu modo de ação é inibição seletiva de neuraminidases, glicoproteínas de liberação dos vírions, ou seja, ele impede a saída dos vírus de uma célula para outra.[7][8][9] O medicamento não impede a contaminação com o vírus e é usado no tratamento da infecção. Possui ligação plasmática < 3% e volume de distribuição de 0,32 +-0,09 l/kg e não é substrato para P450.[nota 1] Além disto, a ingestão de alimentos não impede sua absorção.
Precauções
O metabólito é eliminado pela via renal. Desta forma, deve-se observar pacientes com insuficiência renal, com ajuste de dose. Em pacientes idosos, a dose não necessita ser ajustada. Em grávidas, o medicamento não foi testado e seu uso deve ser feito a critério médico[8] Segundo a Anvisa, as pacientes grávidas devem ser observadas pelos médicos de 30 a 48 horas após a administração do medicamento e depois de 30 dias após o nascimento da criança e crianças menores de um ano devem ser observadas de 30 a 48 horas.[10]
Efeitos adversos
Efeitos colaterais associados com a terapia com oseltamivir incluem: náuseas, vômitos, diarréia, dor abdominal e cefaléia. Raramente incluem: hepatite e enzimas hepáticas elevadas, erupções cutâneas, reacções alérgicas incluindo anafilaxia e síndrome de Stevens-Johnson. Vários outros efeitos colaterais foram relatados na vigilância: necrólise epidérmica tóxica, arritmia cardíaca, convulsão, confusão, agravamento de diabetes, e colite hemorrágica.
Resumo
- Enjoo
- Náusea
- Cefaleia
- Insônia
- Dores de garganta
- Congestão nasal
- Diarreia
- Fadiga
- Alergia
Efeitos neurológicos
Existem preocupações de que o oseltamivir pode causar perigosos efeitos colaterais psicológicos, neuropsiquiátricos, incluindo automutilação em alguns usuários.[11] Essas preocupações se confirmaram em 2014, quando a GSK, empresa reponsável pela fabricação do medicamento, foi obrigada a pagar uma indenização de 60 milhões de Libras para vítimas da vacinação.[12]
Interações medicamentosas
Devido às propriedades do metabólito de mínima ligação com proteínas plasmáticas, as interações medicamentosas para este medicamento são improváveis de acontecer. A cimetidina não interfere em sua biodisponibilidade.[8][13] Contudo, segundo o Infarmed, a administração de probenecida poderá aumentar as concentrações do metabolito activo do oseltamivir.[14]
Síntese

A síntese é uma reação complexa, que compreende uma série de etapas até a obtenção do produto final, o fosfato de oseltamivir.
Outras imagens
Notas
- ↑ Em indivíduos normais, após dose oral única. Dados referêntes ao carboxilato de oseltamivir
Referências
- ↑ Laurence L Brunton; Almir Lourenço Fonseca; Carlos Henrique de Araújo Cosendey; Goodman & Gilman as bases farmacológicas da terapêutica [tradução da 10. ed. original, Carla de Melo Vorsatz. et al] Rio de Janeiro: McGraw-Hill, 2005. Livro ISBN 857-726-001-1 OCLC 77543277 e-Livro OCLC 882498497
- ↑ Gazeta Web. «Suspeitas da gripe suína no Brasil já são 20». Consultado em 29 de abril de 2009
- ↑ Anvisa. «Resolução - RDC nº 40, de 28 de abril de 2000». Consultado em 30 de janeiro de 2010
- ↑ PT Jornal. «Tamiflu é o primeiro medicamento para a gripe autorizado nos EUA em crianças de duas semanas». Consultado em 6 January 2013 Verifique data em:
|acessodata=(ajuda) - ↑ Estadão. «Gripe vira alvo de informação falsa». Consultado em 20 de agosto de 2009
- ↑ Agência Brasil. «Versão em xarope do Tamiflu para crianças já está sendo distribuída no DF». Consultado em 21 de agosto de 2009
- ↑ G1. «Empresa farmacêutica informa primeiro caso de resistência do H1N1 a remédio». Consultado em 30 de junho de 2009
- ↑ a b c P.R. Vade-mécum ABIMIP 2006/2007
- ↑ P. R Vade-mécum de Medicamentos - 2009-2010 - 15ª Ed. Soriak. ISBN 978-858-640-929-5 OCLC 53857630
- ↑ Anvisa. «Médico deve acompanhar bebês e grávidas que utilizam o Tamiflu». Consultado em 14 de agosto de 2009
- ↑ FDA, Yael (2006). «Tamiflu May Be Linked to Risk for Self-Injury and Delirium». Medscape. Consultado em 17 May 2008
|last=e|author=redundantes (ajuda); Verifique data em:|acessodata=(ajuda) - ↑ Brain-Damaged UK Victims of Swine Flu Vaccine to Get £60 Million Compensation International Business Times, Tom Porter, 2 de março de 2014
- ↑ Bulas Med. «(FOSFATO DE OSELTAMIVIR)». Consultado em 29 de abril de 2009
- ↑ Infarmed. «(Oseltamivir no Prontuário Terapêutico)». Consultado em 26 de fevereiro de 2013