Glicina: diferenças entre revisões
m clean up, Replaced: [[image: → [[Imagem: (2) |
|||
| Linha 1: | Linha 1: | ||
{{chembox new |
|||
| Reference=<ref>''[[Merck Index]]'', 11th Edition, '''4386'''.</ref> |
|||
| ImageFileL1 = Glycin - Glycine.svg |
|||
| ImageSizeL1 = 73px |
|||
| ImageFileR1 = Glycine-zwitterion-2D-skeletal.png |
|||
| ImageSizeR1 = 120px |
|||
| ImageFileL2 = Glycine-from-xtal-2008-3D-balls.png |
|||
| ImageSizeL2 = 120px |
|||
| ImageFileR2 = Glycine-from-xtal-2008-3D-vdW.png |
|||
| ImageSizeR2 = 120px |
|||
| IUPACName = Glycine<br/>2-Aminoacetic acid |
|||
| OtherNames = Aminoethanoic acid |
|||
| Section1 = {{Chembox Identifiers |
|||
| Abbreviations = '''Gly''', '''G''' |
|||
| CASNo = 56-40-6 |
|||
| CASNo_Ref = {{cascite}} |
|||
| ChemSpiderID = 730 |
|||
| PubChem = 750 |
|||
| SMILES = NCC(O)=O |
|||
}} |
|||
| Section2 = {{Chembox Properties |
|||
| C=2 | H=5 | N=1 | O=2 |
|||
| MolarMass = |
|||
| Appearance = |
|||
| Density = 1.1607 g/cm<sup>3</sup> |
|||
| MeltingPt = 233 °C (decomposition) |
|||
| BoilingPt = |
|||
| Solubility = 25 g/100 mL |
|||
}} |
|||
| Section3 = {{Chembox Hazards |
|||
| MainHazards = |
|||
| FlashPt = |
|||
| Autoignition = |
|||
}} |
|||
| ⚫ | |||
A '''glicina''' (do [[Língua grega antiga|grego]] ''glykos'', "doce", nome devido ao seu sabor adocicado<ref name="Lehninger">NELSON, David L.; COX, Michael M., '''Lehninger Principles of Biochemistry''', 4th ed., W.H.Freeman, 2004, ISBN 978-0716743392</ref>) é um dos [[aminoácido]]s codificados pelo [[código genético]], sendo portanto um dos componentes das [[proteína]]s dos seres vivos. É codificado pelos [[codões]] GGU, GGC, GGA e GGG<ref>{{cite web | author=IUPAC-IUBMB Joint Commission on Biochemical Nomenclature | title=Nomenclature and Symbolism for Amino Acids and Peptides | work=Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc | url=http://www.chem.qmul.ac.uk/iupac/AminoAcid/ | accessdate=2007-05-17}}</ref>. |
A '''glicina''' (do [[Língua grega antiga|grego]] ''glykos'', "doce", nome devido ao seu sabor adocicado<ref name="Lehninger">NELSON, David L.; COX, Michael M., '''Lehninger Principles of Biochemistry''', 4th ed., W.H.Freeman, 2004, ISBN 978-0716743392</ref>) é um dos [[aminoácido]]s codificados pelo [[código genético]], sendo portanto um dos componentes das [[proteína]]s dos seres vivos. É codificado pelos [[codões]] GGU, GGC, GGA e GGG<ref>{{cite web | author=IUPAC-IUBMB Joint Commission on Biochemical Nomenclature | title=Nomenclature and Symbolism for Amino Acids and Peptides | work=Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc | url=http://www.chem.qmul.ac.uk/iupac/AminoAcid/ | accessdate=2007-05-17}}</ref>. |
||
| Linha 4: | Linha 39: | ||
Apesar de ser um aminoácido apolar, a sua cadeia lateral (um [[átomo]] de [[hidrogénio]]) é demasiado curta para participar em [[Hidrofobia|interacções hidrofóbicas]]<ref name="Lehninger"/>. No entanto, a glicina pode, em determinadas [[enzima]]s como a piruvato:formato liase, ser convertida a [[radical livre|radical]] glicilo através da retirada desse átomo de hidrogénio, sendo este radical importante para a [[catálise enzimática]], embora instável e destruído na presença de [[oxigénio|O<sub>2</sub>]]<ref>WAGNER, A.F.; FREY, M.; NEUGEBAUER, F.A.; SCHÄFER, W.; KNAPPE J, "The free radical in pyruvate formate-lyase is located on glycine-734", '''Proc. Natl. Acad. Sci. U.S.A.''', '''89'''(3):996-1000 (1992).</ref>. |
Apesar de ser um aminoácido apolar, a sua cadeia lateral (um [[átomo]] de [[hidrogénio]]) é demasiado curta para participar em [[Hidrofobia|interacções hidrofóbicas]]<ref name="Lehninger"/>. No entanto, a glicina pode, em determinadas [[enzima]]s como a piruvato:formato liase, ser convertida a [[radical livre|radical]] glicilo através da retirada desse átomo de hidrogénio, sendo este radical importante para a [[catálise enzimática]], embora instável e destruído na presença de [[oxigénio|O<sub>2</sub>]]<ref>WAGNER, A.F.; FREY, M.; NEUGEBAUER, F.A.; SCHÄFER, W.; KNAPPE J, "The free radical in pyruvate formate-lyase is located on glycine-734", '''Proc. Natl. Acad. Sci. U.S.A.''', '''89'''(3):996-1000 (1992).</ref>. |
||
{| border=1 |
|||
|Nomenclatura |
|||
|Glicina ou Glicocola |
|||
|- |
|||
|Símbolo |
|||
|Gly, Gli ou G |
|||
|- |
|||
|Nome químico |
|||
|Ácido 2-aminoacético ou ácido 2-amino-etanóico |
|||
|- |
|||
|Classificação |
|||
|Aminoácido apolar |
|||
|- |
|||
|Estrutura linear |
|||
|[[Imagem:Glycine2.png|100px|center]] |
|||
|- |
|||
|Estrutura Tridimensional |
|||
|[[Imagem:Image-Glycine3d.png|100px|center]] |
|||
| ⚫ | |||
==Biossíntese== |
==Biossíntese== |
||
Revisão das 22h56min de 3 de junho de 2009
| Glicina Alerta sobre risco à saúde[1] | |
|---|---|
|
|
|
|
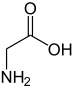
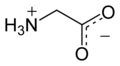
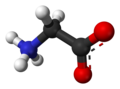
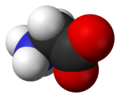
| Nome IUPAC | Glycine 2-Aminoacetic acid |
| Outros nomes | Aminoethanoic acid |
| Identificadores | |
| Abreviação | Gly, G |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| SMILES |
|
| Propriedades | |
| Fórmula química | C2H5NO2 |
| Massa molar | 75.06 g mol-1 |
| Densidade | 1.1607 g/cm3 |
| Ponto de fusão |
233 °C (decomposition) |
| Solubilidade em água | 25 g/100 mL |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A glicina (do grego glykos, "doce", nome devido ao seu sabor adocicado[2]) é um dos aminoácidos codificados pelo código genético, sendo portanto um dos componentes das proteínas dos seres vivos. É codificado pelos codões GGU, GGC, GGA e GGG[3].
Devido à sua simplicidade estrutural, este aminoácido tende a ser conservado evolucionariamente em proteínas como o citocromo c, a mioglobina e a hemoglobina. A glicina é o único aminoácido que não apresenta actividade óptica. A maioria das proteínas possui pequenas quantidades de glicina; o colagénio é uma excepção de nota, constituindo a glicina cerca de um terço da sua estrutura primária. A presença de glicina inibe a formação de hélices alfa mas facilita a formação de voltas beta na estrutura secundária de proteínas, por ser um aminoácido que apresenta um alto grau de flexibilidade quando integrado numa cadeia polipeptídica[2].
Apesar de ser um aminoácido apolar, a sua cadeia lateral (um átomo de hidrogénio) é demasiado curta para participar em interacções hidrofóbicas[2]. No entanto, a glicina pode, em determinadas enzimas como a piruvato:formato liase, ser convertida a radical glicilo através da retirada desse átomo de hidrogénio, sendo este radical importante para a catálise enzimática, embora instável e destruído na presença de O2[4].
Biossíntese
A glicina não é um aminoácido essencial na dieta humana, já que é sintetizado pelo organismo a partir do aminoácido serina numa reacção catalizada pela enzima serina hidroximetiltransferase[2]:
- HO2CCH(NH2)CH2OH + H2-folato → HO2CCH2NH2 + CH2-folato + H2O
Função fisiológica
Como intermediário biossintético
A glicina serve de precursor a diversas espécies químicas. O ácido aminolevulínico, precursor chave das porfirinas, é sintetizado in vivo a partir de glicina e succinil-coenzima A. A glicina fornece também o bloco C2N central a todas as purinas. Uma das vias de degradação do aminoácido treonina passa pela sua conversão a glicina, embora esta via metabólica seja relativamente pouco importante no metabolismo humano. É ainda precursor na via biossintética da fosfocreatina.
A degradação da glicina segue três vias principais:
- Pode ser degradada a piruvato, seguindo a reacção inversa da sua biossíntese (ou seja, conversão a serina e então conversão desta a piruvato).
- Especialmente em animais, a glicina pode ser oxidada a CO2, NH4+ e um grupo metileno pela enzima glicina sintase.
- Pode ser oxidada e desaminada a glioxilato pela enzima D-aminoácido oxidase, sendo o glioxilato posteriormente reduzido a oxalato.
Como neurotransmissor
A glicina é um neurotransmissor inibitório no sistema nervoso central, especialmente a nível da medula espinal, tronco cerebral e retina. Quando receptores de glicina são activados, o anião cloreto entra no neurónio através de receptores ionotrópicos, causando um potencial pós-sináptico inibitório. A estricnina actua como antagonista nos receptores ionotrópicos de glicina. A glicina é, junto com o glutamato, um co-agonista de receptores NMDA; esta acção facilita a actividade excitatória dos receptores glutaminérgicos, em contraste com a actividade inibitória da glicina.
A dose letal de glicina administrada oralmente, em ratos, é de 7930 mg/kg[5], causando morte usualmente por hiperexcitabilidade.
Como elemento estrutural
Além de ser um aminoácido importante na formação de colagénio, é essencial na formação da camada de peptidoglicano na parede celular de bactérias Gram-positivas, ao formar um pentapéptido (pentaglicina) que ajuda na ligação entre resíduos de ácido N-acetilmurâmico. A pentaglicina está ausente nas bactérias Gram-negativas.
A glutationa, tripéptido essencial na manutenção do equilíbrio redox intracelular, tem na sua constituição glicina.
Na fotorrespiração
As mitocôndrias de plantas apresentam uma via alternativa de respiração, a fotorrespiração, em que a glicina é convertida a serina através da seguinte reacção, catalizada pela enzima glicina descarboxilase:
- 2 Gly + NAD+ → Ser + CO2 + NH3 +� NADH +� H+,
tornando-se esta a principal fonte de NADH mitocondrial� para posterior produção de ATP. Esta reacção faz parte do ciclo do glicolato.
Referências
- ↑ Merck Index, 11th Edition, 4386.
- ↑ a b c d NELSON, David L.; COX, Michael M., Lehninger Principles of Biochemistry, 4th ed., W.H.Freeman, 2004, ISBN 978-0716743392 Erro de citação: Código
<ref>inválido; o nome "Lehninger" é definido mais de uma vez com conteúdos diferentes - ↑ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature. «Nomenclature and Symbolism for Amino Acids and Peptides». Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. Consultado em 17 de maio de 2007
- ↑ WAGNER, A.F.; FREY, M.; NEUGEBAUER, F.A.; SCHÄFER, W.; KNAPPE J, "The free radical in pyruvate formate-lyase is located on glycine-734", Proc. Natl. Acad. Sci. U.S.A., 89(3):996-1000 (1992).
- ↑ «Safety (MSDS) data for glycine». The Physical and Theoretical Chemistry Laboratory Oxford University. 2005. Consultado em 1 de novembro de 2006
- DAWSON, R.M.C.; ELLIOTT, D.C.; ELLIOTT, W.H.; JONES, K.M., Data for Biochemical Research, 3rd ed., pp. 1-31 (1986)
Ligações externas
Predefinição:Portal-bioquímica
- «Glicina» (em inglês)
- «Computational Chemistry Wiki» (em inglês)
- «Sistema de clivagem da glicina» (em inglês)
