Prolina
| Prolina Alerta sobre risco à saúde | |
|---|---|

|
|
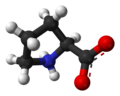
| Nome IUPAC | (S)-Pyrrolidine-2-carboxylic acid |
| Outros nomes | L-Prolina (S)-Prolina D-Prolina (R)-Prolina Ácido (2S)-Pirrolidino-2-carboxílico Ácido (2S)-1,3,4,5-tetraidro-2H-pirrol-2-carboxílico Ácido (2S)-azaciclopentano-2-carboxílico Ácido (2S)-azolidino-2-carboxilíco Pro, P (abreviaturas) |
| Identificadores | |
| Número CAS | ,(L-Prolina) 344-25-2 (D-Prolina) 609-36-9 {Racêmico; sinônimos: DL-Prolina e (RS)-Prolina} |
| PubChem | |
| DrugBank | NUTR00047 |
| Código ATC | ATC |
| SMILES |
|
| Propriedades | |
| Fórmula química | C5H9NO2 |
| Massa molar | 115.12 g mol-1 |
| Densidade | 1,35–1,38 g·cm 3 (25 °C), |
| Ponto de fusão |
decompõe-se a 220–222 °C (D- e L-Prolina) |
| Solubilidade em água | muito solúvel (1500 g·l-1 a 20 °C) |
| Acidez (pKa) | pKCOOH: 1,95 pKNH2: 10,64 (a 25 °C) |
| Riscos associados | |
| Frases R | - |
| Frases S | - |
| LD50 | > 5110 mg·kg-1 (rato, oral) |
| Compostos relacionados | |
| Aminoácidos relacionados | Norvalina (ácido 2-aminopentanoico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A prolina (símbolo Pro ou P) é um aminoácido proteinogênico utilizado na biossíntese de proteínas.
Definição
[editar | editar código-fonte]A prolina faz parte do grupo dos 20 aminoácidos que participam da composição de proteínas, desse modo, chamados de aminoácidos proteicos ou α-aminoácidos, visto que possuem um grupo amino primário e um grupo carboxila ligados ao mesmo átomo de carbono. Contudo, a estrutura da prolina difere dos demais aminoácidos, pois ela possui um grupo amino secundário e não primário. Sua cadeia lateral é considerada apolar, pois não participa de ligações iônicas ou de hidrogênio, desse modo participando de interações hidrofóbicas. Estruturalmente, a cadeia lateral da prolina e seu N α-amínico formam uma estrutura rígida em anel, com 5 átomos. A geometria da molécula permite, por exemplo, a formação da estrutura fibrosa do colágeno e de proteínas globulares.[1] As propriedades físico-químicas da prolina podem ser observadas no quadro ao lado.[2][3]
Síntese de prolina
[editar | editar código-fonte]É considerado um aminoácido não essencial, visto que sua síntese ocorre endogenamente a partir do aminoácido glutamato. Inicialmente, o glutamato sintetizado é convertido em γ-glutamil fosfato através da enzima glutamato quinase. A seguir a enzima glutamato desidrogenase o converte em glutamato γ-semialdeído, que é então reduzido pelo NADPH a ∆¹-pirrolina-5-carboxilato de forma espontânea. Por fim, o último passo necessário para a síntese de prolina é a conversão da ∆¹-pirrolina-5-carboxilato em prolina, catalisado pela enzima pirrolina carboxilato redutase.[4]
Propriedades em proteínas
[editar | editar código-fonte]A estrutura cíclica da cadeia lateral da prolina confere à molécula uma rigidez considerável em relação a outros aminoácidos, no entanto afetando a taxa de formação de ligações peptídicas. Comparado com outros tRNAs, a formação de ligação peptídica do Pro-tRNA é lenta, um fenômeno característico dos N-alquil-aminoácidos.[5] A formação da ligação também é lenta entre moléculas de tRNA e cadeias que terminam em prolina, sendo a interação prolina-prolina a mais lenta de todas.[6]
Quando a região amida da prolina realiza ligação peptídica, seu nitrogênio não interage com hidrogênio, ou seja, não atua como doador (apenas como receptor) na ligação de hidrogênio.[7]
A rigidez conformacional da prolina afeta a estrutura secundária da proteína em que está inserida, o que poderia explicar sua maior prevalência em organismos termofílicos. A prolina pode alterar elementos da estrutura secundaria como a alfa-hélice e a folha-beta. Contudo, a prolina é frequentemente encontrada nas primeiras posições da N-terminal, onde a perda do hidrogênio da ponte de hidrogênio da amida não produz uma alteração significativa. Em análises de estrutura, foi encontrado que grande parte das prolinas ocorrem no primeiro giro.[8]
Uma sequência de múltiplas prolinas forma uma hélice de poliprolina, a estrutura secundária predominante em colágeno. A hidroxilação da prolina pela prolil hidroxilase aumenta de modo significativo a estabilidade conformacional do colágeno. Por causa disso, a hidroxilação da prolina é um fator bioquímico essencial para conservar o tecido conectivo.
Usos
[editar | editar código-fonte]A prolina e seus derivados são regularmente utilizados como catalisadores assimétricos em reações que usam catalisadores orgânicos. A redução Corey–Bakshi–Shibata (CBS) e a condensação aldólica são exemplos disso.
Na preparação de cerveja, proteínas ricas em prolina são utilizadas para obter turbidez.[9]
A L-prolina serve como osmoprotetor, sendo assim usado em aplicações farmacológicas e biotecnológicas.
Meios de cultura de tecido vegetal podem ser suplementado com prolina. É sabido que a acumulação de prolina em plantas está relacionado com estresse, porém sua função específica continua em debate.[10][11]
Referências
- ↑ Francis A. Carey. Química Orgânica. 7. Ed. São Paulo: editora AMGH Ltda, 2011
- ↑ Catálogo da Merck Prolina acessado em 19. Januar 2008
- ↑ Hans Beyer und Wolfgang Walter: Lehrbuch der Organischen Chemie, Hirzel Verlag, Stuttgart 1991, ISBN 3-7776-0485-2, S. 823.
- ↑ Richard A. Harvey, Denise R. Ferrier. Bioquímica Ilustrada.5.ed. Editora Artmed. 2012
- ↑ Pavlov, Michael Y.; Watts, Richard E.; Tan, Zhongping; Cornish, Virginia W.; Ehrenberg, Måns; Forster, Anthony C. (6 de janeiro de 2009). «Slow peptide bond formation by proline and other N-alkylamino acids in translation». Proceedings of the National Academy of Sciences (em inglês). 106 (1): 50–54. ISSN 0027-8424. PMID 19104062. doi:10.1073/pnas.0809211106
- ↑ Buskirk, Allen R.; Green, Rachel (4 de janeiro de 2013). «Getting Past Polyproline Pauses». Science (em inglês). 339 (6115): 38–39. ISSN 0036-8075. PMID 23288527. doi:10.1126/science.1233338
- ↑ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). «Primary Structure: Amino Acids Are Linked by Peptide Bonds to Form Polypeptide Chains». Biochemistry. 5th edition (em inglês)
- ↑ Kim, M. K.; Kang, Y. K. (julho de 1999). «Positional preference of proline in alpha-helices.». Protein Science : A Publication of the Protein Society. 8 (7): 1492–1499. ISSN 0961-8368. PMC 2144370
 . PMID 10422838
. PMID 10422838
- ↑ «Haze & Foam». 11 de julho de 2010. Consultado em 3 de junho de 2018
- ↑ Verbruggen, Nathalie; Hermans, Christian (novembro de 2008). «Proline accumulation in plants: a review». Amino Acids. 35 (4): 753–759. ISSN 1438-2199. PMID 18379856. doi:10.1007/s00726-008-0061-6
- ↑ Mattioli, Roberto; Costantino, Paolo; Trovato, Maurizio (novembro de 2009). «Proline accumulation in plants: not only stress». Plant Signaling & Behavior. 4 (11): 1016–1018. ISSN 1559-2324. PMC 2819507
 . PMID 20009553
. PMID 20009553
