Vitamina B6
Esta página ou seção foi marcada para revisão devido a incoerências ou dados de confiabilidade duvidosa. |
| Vitamina B6 Alerta sobre risco à saúde[1] | |
|---|---|
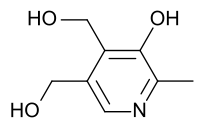
| |
| Nome IUPAC | 4,5-Bis(hydroxymethyl)- 2-methylpyridin- 3-ol |
| Identificadores | |
| Número CAS | , 58-56-0 (hydrochloride) |
| PubChem | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C8H11NO3 |
| Massa molar | 169.18 g/mol |
| Ponto de fusão |
159-162 °C |
| Compostos relacionados | |
| Outros aniões/ânions | Piridoxamina |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Vitamina B6 é o grupo de compostos quimicamente semelhantes que podem ser interconvertidos em sistemas biológicos. A vitamina B6 é parte do grupo da vitamina B de nutrientes essenciais. Sua forma ativa, piridoxal-5-fosfato, serve como uma coenzima em aproximadamente 100 reações enzimáticas em aminoácidos, glicose, e metabolismo de lipídios.[2][3]
Formas[editar | editar código-fonte]
A piridoxamina é convertida em piridoxamina-5’-fosfato pela cinase piridoxal e depois é convertida em piridoxal-5’-fosfato pela transaminase piridoxamina-fosfato ou pela oxidase piridoxina-5’-fosfato que também catalisa a conversão de piridoxina-5’-fosfato em piridoxal-5’-fosfato.[4] A oxidase piridoxina-5’-fosfato é dependente do mononucleótido de flavina como um cofator produzido a partir de riboflavina (vitamina b2).
- Piridoxina, a forma mais utilizada em suplementos de vitamina B6
- Piridoxina-5’-fosfato
- Piridoxal
- Piridoxal-5’-fosfato, a forma metabolicamente ativa
- Piridoxamina
- Piridoxamina-5’-fosfato
- Ácido 4-piridoxico
- Piritinol
Todas as formas, com a exceção do ácido piridoxico e do piritinol, podem ser interconvertidos.[5] Piritinol é um derivado semi-sintético da piridoxina, onde duas metades de piridoxina são ligadas por uma ponte de dissulfeto.
Funções[editar | editar código-fonte]
O Piridoxal-5’-fosfato, a forma metabolicamente ativa da vitamina B6, é envolvido em muitos aspectos do metabolismo de macronutrientes, síntese de neurotransmissores, síntese de histamina, síntese e função de hemoglobina e expressão genética. O Piridoxal-5’-fosfato geralmente serve como uma coenzima (cofator) para muitas reações incluindo descarboxilação, transaminação, racemização, eliminação, substituição e interconversão do grupo beta.[2][3][6]
Metabolismo de aminoácidos[editar | editar código-fonte]
- O piridoxal-5’-fosfato é um cofator na biosíntese de cinco neurotransmissores importantes: serotonina, dopamina, epinefrina, norepinefrina e ácido gama-aminobutírico (GABA). O piridoxal-5’-fosfato também é envolvido na síntese de histamina.
- Transaminases quebram aminoácidos com o piridoxal-5’-fosfato como um cofator. A atividade adequada dessas enzimas é crucial para o processo de mover grupos amino de um aminoácido para outro.
- A serina racemasa que sintetiza o neuromodulador D-serina a partir de seu enantiômero é uma enzima dependente do piridoxal-5’-fosfato.
- O piridoxal-5’-fosfato é uma coenzima necessária para a função adequada das enzimas cistationina sintase e cistationase. Essas enzimas catalisam reações no catabolismo de metionina. Parte desse caminho (a reação catalisada pela cistationase) também produz cisteína.
- A selenometionina é a forma dietética primária de selênio. O piridoxal-5’-fosfato é necessário como um cofator para as enzimas que permitem que o selênio seja usado a partir da forma dietética. O piridoxal-5’-fosfato também serve como cofator para liberar selênio da selenohomocisteína para produzir seleneto de hidrogênio, que pode então ser usado para incorporar selênio em selenoproteínas.
- O piridoxal-5’-fosfato é requerido para a conversão de triptofano em niacina, assim baixa vitamina B6 prejudica essa conversão.[6][7]
Metabolismo de glicose[editar | editar código-fonte]
O piridoxal-5’-fosfato é uma coenzima essencial da glicogênio fosforilase, a enzima necessária para a glicogenólise acontecer.[6] Piridoxal-5’-fosfato pode catalisar reações de transaminação que são essenciais para fornecer aminoácidos como um substrato para a gliconeogênese.
Metabolismo de lipídios[editar | editar código-fonte]
O piridoxal-5’-fosfato é um componente essencial de enzimas que facilitam a biossíntese de esfingolipídios.[6] Em particular, a síntese de ceramida requer piridoxal-5’-fosfato. Nessa reação, a serina é descarboxilada e combinada com palmitoyl-CoA para formar esfinganina, que é combinada com um Acil-CoA gorduroso para formar dihidroceramida. A dihidroceramida continua sendo dessaturada para formar ceramida. Além disso, a quebra de esfingolipídios também depende da vitamina B6 porque a esfingosina-1-fosfato liase, enzima responsável por quebrar esfingosina-1-fosfato, também é dependente de piridoxal-5’-fosfato.
Síntese e função de hemoglobina[editar | editar código-fonte]
O piridoxal-5’-fosfato ajuda na síntese de hemoglobina, servindo como uma coenzima para a enzima ácido aminolevulínico sintetase.[8] Ele também se liga a dois sítios na hemoglobina para aumentar a aderência da hemoglobina ao oxigênio.
Expressão gênica[editar | editar código-fonte]
O piridoxal-5’-fosfato tem sido relacionado com o aumento ou a diminuição da expressão de certos genes. Níveis intracelulares aumentados da vitamina levam à diminuição da transcrição de glicocorticóides. Deficiência de vitamina B também leva ao aumento da expressão gênica do mRNA de albumina. O piridoxal-5’-fosfato também influencia na expressão de glicoproteína IIb, através da interação com vários fatores de transcrição. O resultado é a inibição de agregação de plaquetas.[6]
Nutrição[editar | editar código-fonte]
Fontes dietéticas[editar | editar código-fonte]
A vitamina B6 é amplamente distribuída em comidas, tanto em forma livre como ligada. Perdas durante cozinhamento, armazenamento e processamento variam e em alguns alimentos pode ser maior do que 50%,[3] dependendo da forma da vitamina presente na comida. Vegetais são os que menos perdem vitamina B6 durante o processamento, porque eles contêm piridoxina, que é muito mais estável do que piridoxal e piridoxamina, encontrados em alimentos de origem animal. Por exemplo, o leite pode perder de 30 a 70% da sua vitamina B6 quando secado.[6] A vitamina B6 é encontrada na camada de germe e aleurona dos grãos e processamento resulta na redução dessa vitamina na farinha branca. O aquecimento que ocorre antes dos processos de congelamento e enlatamento também pode resultar em perda de vitamina B6.[9]
Alimentos que contêm grandes quantidades de vitamina B6 incluem:[2][10]
- Bananas[11]
- Grão-de-bico[12]
- Chocolate amargo[13]
- Batata[14]
- Pistache[15]
- Cereais matinais fortificados[2]
- Carne bovina[16]
- Carne suína[17]
- Peru[18]
Recomendações dietéticas[editar | editar código-fonte]
O Instituto de Medicina dos Estados Unidos (renomeado como Academia Nacional de Medicina em 2015) atualizou os Requisitos Médios Estimados (RMEs) e as Tolerâncias Dietéticas Recomendadas (TDRs) para a vitamina B6 em 1998. Os RMEs de vitamina B6 para mulheres e homens que tenham 14 anos ou mais aumentam com a idade de 1 para 1,3 mg/dia e de 1,1 para 1,4 mg/dia, respectivamente; Os TDRs aumentam com a idade de 1,2 para 1,5 mg/dia e de 1,3 para 1,7 mg/dia, respectivamente. TDRs são maiores do que RMEs para incluir pessoas com necessidades médias maiores. TDR para mulheres grávidas é 1,9 mg/dia. TDR para mulheres amamentando é 2 mg/dia. Para bebês de até 12 meses o Consumo Adequado (CA) é de 0,1 a 0,3 mg/dia e para crianças que tenham de 1 a 13 anos o TDR aumenta com a idade de 0,5 para 1 mg/dia. Por segurança, Limites Máximos (LMs) para vitaminas e minerais são determinados quando as evidências são suficientes. No caso da vitamina B6 o LM está estabelecido como 100 mg/dia. Coletivamente os RMEs, TDRs, CMs e LMs são chamados de Referência de Consumo Dietético (RCDs).[19]
A Autoridade Europeia de Segurança da Comida (AESC) se refere às informações coletivas como Valores de Referência Dietéticos, com Consumo de Referência da População (CRP) em vez de TDR, e Requerimento Médio em vez de RME. CA e LM são definidos como a mesma coisa nos Estados Unidos. Para mulheres e homens com 15 anos ou mais, o CRP é 1,6 e 1,7 mg/dia, respectivamente. O CA para mulheres grávidas é de 1,8 mg/dia, para mulheres amamentando é de 1,7 mg/dia. Para crianças de 1 a 14 anos os CRPs aumentam com a idade de 0,6 para 1,4 mg/dia. Esses CRPs são um pouco maiores do que os TDRs dos Estados Unidos.[20] O AESC também reviu a questão de segurança e estabeleceu seu LM 25 mg/dia.[21]
Para alimentos e suplementos dietéticos nos Estados Unidos, a quantidade em uma servida é representada como uma porcentagem do valor diário. Para a vitamina B6, 100% do valor diário era 2 mg, mas em 27 de maio de 2016 foi ajustado para 1,7 mg para ficar em acordo com o TDR.[22][23] Conformidade com o regulamento atualizado foi requerido a partir de 1º de janeiro de 2020 para produtores com faturamento de 10 milhões de dólares ou mais em vendas de alimentos, e a partir de 1º de janeiro de 2021 para produtores com menor volume de vendas.[24][25] Uma tabela com os valores diários velhos e novos é fornecida pelo Consumo Diário de Referência.
Absorção e excreção[editar | editar código-fonte]
A vitamina B6 é absorvida no jejuno e íleo por difusão passiva. Como a capacidade de absorção é muito grande, os animais são capazes de absorver quantidades muito maiores do que o necessário para as demandas fisiológicas. A absorção de piridoxal fosfato e piridoxamina fosfato envolve a desfosforilação dos mesmos, catalisada por uma fosfatase alcalina ligada à membrana. Esses produtos e formas não fosforiladas no trato digestivo são absorvidos por difusão, que é conduzida pelo aprisionamento da vitamina como 5′-fosfatos por meio da ação da fosforilação (por uma cinase piridoxal) na mucosa jejunal. A piridoxina e a piridoxamina presas são oxidadas a piridoxal fosfato no tecido.[6]
Os produtos do metabolismo da vitamina B6 são excretados na urina, cujo principal produto é o ácido 4-piridóxico. Estima-se que 40–60% da vitamina B6 ingerida é oxidada em ácido 4-piridoxico. Vários estudos mostraram que o ácido 4-piridóxico é indetectável na urina de indivíduos com deficiência de vitamina B6, tornando-o um marcador clínico útil para avaliar o nível de vitamina B6 de um indivíduo.[6] Outros produtos do metabolismo da vitamina B6 excretados na urina quando altas doses da vitamina são administradas incluem piridoxal, piridoxamina e piridoxina e seus fosfatos. Uma pequena quantidade de vitamina B6 também é excretada nas fezes.
Deficiência[editar | editar código-fonte]
Sinais e sintomas[editar | editar código-fonte]
A síndrome clínica clássica para deficiência de vitamina B6 é uma erupção semelhante à dermatite seborreica, glossite atrófica com ulceração, queilite angular, conjuntivite, intertrigo e sintomas neurológicos de sonolência, confusão e neuropatia[26] (devido à síntese prejudicada de esfingosina) e anemia sideroblástica (devido à síntese prejudicada do heme).
Os casos menos graves apresentam doença metabólica associada à atividade insuficiente da coenzima piridoxal-5-fosfato. A mais proeminente das lesões é devido à conversão prejudicada de triptofano-niacina. Isso pode ser detectado com base na excreção urinária de ácido xanturênico após uma dose oral de triptofano. A deficiência de vitamina B6 também pode resultar em transulfuração prejudicada de metionina em cisteína. As transaminases dependentes de piridoxal-5’-fosfato e a glicogênio fosforilase fornecem à vitamina seu papel na gliconeogênese, portanto, a privação de vitamina B6 resulta em tolerância à glicose prejudicada.[6]
Diagnóstico[editar | editar código-fonte]
A avaliação do nível de vitamina B6 é essencial, pois os sinais e sintomas clínicos em casos menos graves não são específicos.[27] Os três testes bioquímicos mais amplamente usados são o coeficiente de ativação da enzima aspartato aminotransferase eritrocitária, as concentrações plasmáticas de piridoxal-5’-fosfato e a excreção urinária de produtos de degradação da vitamina B6, especificamente o PA urinário. Destes, o piridoxal-5’-fosfato plasmático é provavelmente a melhor medida individual, porque reflete as reservas de tecido. Piridoxal-5’-fosfato plasmático inferior a 10 nmol/l é indicativo de deficiência de vitamina B6.[28] Uma concentração de piridoxal-5’-fosfato superior a 20 nmol/l foi escolhida como um nível de adequação para estabelecer os Requisitos Médios Estimados e as Tolerâncias Dietéticas Recomendadas nos EUA.[19] PA urinária também é um indicador de deficiência de vitamina B6; níveis inferiores a 3,0 mmol/dia são sugestivos de deficiência de vitamina B6.[29]
A síndrome clássica de deficiência de vitamina B6 é rara, mesmo em países em desenvolvimento. Alguns casos foram observados entre 1952 e 1953, principalmente nos Estados Unidos, e ocorreram em uma pequena porcentagem de bebês que foram alimentados com uma fórmula sem piridoxina.[30]
Causas[editar | editar código-fonte]
A deficiência de vitamina B6 isolada é relativamente incomum e frequentemente ocorre em associação com outras vitaminas do complexo B. Idosos e alcoólatras têm um risco aumentado de deficiência de vitamina B6, bem como de outras deficiências de micronutrientes.[3] Existem evidências de níveis reduzidos de vitamina B6 em mulheres com diabetes tipo 1 e em pacientes com inflamação sistêmica, doença hepática, artrite reumatoide e pessoas infectadas com HIV.[31][32][33] O uso de contraceptivos orais e o tratamento com certos anticonvulsivantes, isoniazida ,cicloserina, penicilamina e hidrocortisona impactam negativamente o estado da vitamina B6.[34][35][36] A hemodiálise reduz os níveis plasmáticos de vitamina B6.[37] O consumo excessivo de sementes de Ginkgo Biloba pode esgotar a vitamina B6.[38][39]
Toxicidade[editar | editar código-fonte]
Efeitos adversos foram documentados em suplementos de vitamina B6, mas nunca em fontes alimentares. Danos aos gânglios da raiz dorsal são documentados em casos humanos de overdose de piridoxina.[40] Embora seja uma vitamina solúvel em água e excretada na urina, doses de piridoxina que excedem ao Limite Máximo (LM) por longos períodos causam problemas neurológicos dolorosos e irreversíveis.[19] Os principais sintomas são dor e dormência nas extremidades. Em casos graves, a neuropatia motora pode ocorrer com "desaceleração das velocidades de condução motora, latências da onda F prolongadas e latências sensoriais prolongadas em ambas as extremidades inferiores", causando dificuldade para andar.[41] A neuropatia sensorial geralmente se desenvolve em doses de piridoxina superiores a 1.000 mg por dia, mas os efeitos adversos podem ocorrer com muito menos; portanto, doses acima de 200 mg não são consideradas seguras.[42] Foram relatados sintomas entre mulheres que tomam doses mais baixas.[43]
As autorizações e avaliações existentes variam consideravelmente em todo o mundo. Conforme observado, o Instituto de Medicina dos EUA definiu um LM adulto para 100 mg/dia.[19] O Comitê Científico da Comunidade Europeia de Alimentos definiu a ingestão de 50 mg de vitamina B6 por dia como prejudicial e estabeleceu um LM de 25 mg/dia.[44] Os valores de referência dos nutrientes na Austrália e Nova Zelândia recomendam um LM de 50 mg/dia para adultos. “O mesmo valor foi estabelecido para gravidez e lactação, pois não há evidência de teratogenicidade neste nível. O LM foi estabelecido com base no tamanho do corpo metabólico e considerações de crescimento para todas as outras idades e fases da vida, exceto a infância. Não foi possível definir um LM para bebês, então a ingestão é recomendada na forma de alimento, leite ou fórmula." Os LMs foram definidos usando resultados de estudos envolvendo a administração oral de piridoxina em longo prazo em doses inferiores a 1 g/dia.[19][43] "Um nível de efeito adverso não observado (NEANO) de 200 mg/dia foi identificado a partir dos estudos de Bernstein & Lobitz (1988) e Del Tredici et al (1985). Esses estudos envolveram indivíduos que geralmente tomavam suplementos por cinco a seis meses ou menos. O estudo de Dalton e Dalton (1987), entretanto, sugeriu que os sintomas podem demorar substancialmente mais do que isso para aparecer. Nesta última pesquisa retrospectiva, os indivíduos que relataram sintomas tomaram suplementos por 2,9 anos, em média. Aqueles que não relataram nenhum sintoma, tomaram suplementos por 1,9 anos."[45]
História[editar | editar código-fonte]
Em 1934, o médico húngaro Paul György descobriu uma substância capaz de curar uma doença de pele em ratos (dermatite acrodínia). Ele chamou essa substância de vitamina B6.[46][47] Em 1938, Samuel Lepkovsky isolou a vitamina B6 do farelo de arroz. Em 1939, Harris e Folkers determinaram a estrutura da piridoxina e em 1945, Snell foi capaz de mostrar as duas formas de vitamina B6, piridoxal e piridoxamina. A vitamina B6 foi nomeada piridoxina para indicar sua homologia estrutural com a piridina.[carece de fontes]
Principais antagonistas[editar | editar código-fonte]
Existem mais de 40 medicamentos que interferem com a vitamina B6, os quais podem causar uma disponibilidade diminuída e mau estado da vitamina B6. Os principais antagonistas incluem:
- Desoxipiridoxina, um antimetabólito eficaz;
- Isoniazida, uma droga tuberculostática;
- Hidralazina, um medicamento anti-hipertensivo;
- Ciclosserina, um antibiótico;
- Penicilamina, utilizada no tratamento da doença de Wilson.
A vitamina B6, por outro lado, pode atuar em si mesma como um antagonista nos pacientes com doença de Parkinson e que estejam sob tratamento com L-dopa. Em tais casos, pode contrariar o efeito da L-dopa.
Principais sinergistas[editar | editar código-fonte]
Certas vitaminas do complexo B (niacina, riboflavina, biotina) podem atuar em sinergia com a piridoxina. A niacina e a riboflavina são necessárias para a interconversão das diferentes formas de vitamina B6.
Referências
- ↑ Pyridoxine at Sigma-Aldrich
- ↑ a b c d «Vitamin B6». Micronutrient Information Center, Linus Pauling Institute, Oregon State University, Corvallis, OR. Maio de 2014. Consultado em 7 de março de 2017. Cópia arquivada em 14 de março de 2018
- ↑ a b c d Da Silva VR, Gregory III JF (2020). «Vitamin B6». In: BP Marriott, DF Birt, VA Stallings, AA Yates. Present Knowledge in Nutrition, Eleventh Edition. London, United Kingdom: Academic Press (Elsevier). pp. 225–38. ISBN 978-0-323-66162-1
- ↑ Ink SL, Henderson LM (1984). «Vitamin B6 metabolism». Annual Review of Nutrition. 4: 455–70. PMID 6380540. doi:10.1146/annurev.nu.04.070184.002323
- ↑ Johansson S, Lindstedt S, Tiselius HG (outubro de 1974). «Metabolic interconversions of different forms of vitamin B6». The Journal of Biological Chemistry. 249 (19): 6040–6. PMID 4418204
- ↑ a b c d e f g h i Combs GF (2007). The Vitamins: Fundamental Aspects in Nutrition and Health 3rd ed. San Diego: Elsevier Academic Press. pp. 320–324. ISBN 978-0-8121-0661-9. LCCN 2007026776. OCLC 150255807
- ↑ Lichtstein HC, Gunsalus IC, Umbreit WW (1945). «Function of the vitamin B6 group; pyridoxal phosphate (codecarboxylase) in transamination» (PDF). The Journal of Biological Chemistry. 161 (1): 311–20. PMID 21005738
- ↑ Erskine PT, Coates L, Butler D, Youell JH, Brindley AA, Wood SP, et al. (agosto de 2003). «X-ray structure of a putative reaction intermediate of 5-aminolaevulinic acid dehydratase». The Biochemical Journal. 373 (Pt 3): 733–8. PMC 1223560
 . PMID 12777167. doi:10.1042/bj20030513
. PMID 12777167. doi:10.1042/bj20030513
- ↑ Sauberlich HE (1987). «Vitamins – how much is for keeps?». Nutrition Today. 22: 20–28. doi:10.1097/00017285-198701000-00004
- ↑ «B vitamins and folic acid». nhs.uk (em inglês). Consultado em 23 de outubro de 2018
- ↑ «09040, Bananas, raw». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «16360, Chickpeas (garbanzo beans, bengal gram), mature seeds, canned, solids and liquids, low sodium». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «, FoodData Central Search Results»
- ↑ «11356, Potatoes, Russet, flesh and skin, baked». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «12151, Nuts, pistachio nuts, raw». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «23040, Beef, chuck, shoulder clod, shoulder top and center steaks, separable lean and fat, trimmed to 0" fat, select, cooked, grilled». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «10973, Pork, ground, 96% lean / 4% fat, raw». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ «05305, Ground turkey, raw». National Nutrient Database for Standard Reference, Release 27. United States Department of Agriculture, Agricultural Research Service. Consultado em 27 de junho de 2015
- ↑ a b c d e Institute of Medicine (1998). «Vitamin B6». Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, DC: The National Academies Press. pp. 150–195. ISBN 978-0-309-06554-2. LCCN 00028380. OCLC 475527045. PMID 23193625. doi:10.17226/6015
- ↑ «Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies» (PDF). 2017. Cópia arquivada (PDF) em 28 de agosto de 2017
- ↑ «Tolerable Upper Intake Levels For Vitamins And Minerals» (PDF). European Food Safety Authority. 2006. Cópia arquivada (PDF) em 19 de setembro de 2017
- ↑ «Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels» (PDF). Cópia arquivada (PDF) em 22 de setembro de 2017
- ↑ «Daily Value Reference of the Dietary Supplement Label Database (DSLD)». Dietary Supplement Label Database (DSLD). Consultado em 16 de maio de 2020
- ↑ «Changes to the Nutrition Facts Label». U.S. Food and Drug Administration (FDA). 27 de maio de 2016. Consultado em 16 de maio de 2020
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ «Industry Resources on the Changes to the Nutrition Facts Label». U.S. Food and Drug Administration (FDA). 21 de dezembro de 2018. Consultado em 16 de maio de 2020
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ Andrews' Diseases of the Skin 10th ed. [S.l.]: Elsevier
- ↑ Gibson RS (2005). «Assessment of vitamin B6 status». Principles of Nutritional Assessment 2nd ed. New York: Oxford University Press. pp. 575–594. ISBN 978-0-19-517169-3. LCCN 2004054778. OCLC 884490740
- ↑ Lui A, Lumeng L, Aronoff GR, Li TK (novembro de 1985). «Relationship between body store of vitamin B6 and plasma pyridoxal-P clearance: metabolic balance studies in humans». The Journal of Laboratory and Clinical Medicine. 106 (5): 491–7. PMID 4056565
- ↑ Leklem JE (novembro de 1990). «Vitamin B-6: a status report». The Journal of Nutrition. 120 Suppl 11 (4): 1503–7. PMID 2243296. doi:10.1093/jn/120.suppl_11.1503
- ↑ Menkes JH (1980). Textbook of Child Neurology 2nd ed. Philadelphia: Henry Kimpton Publishers. p. 486. ISBN 978-0-8121-0661-9. LCCN 79010975. OCLC 925196268
- ↑ Massé PG, Boudreau J, Tranchant CC, Ouellette R, Ericson KL (fevereiro de 2012). «Type 1 diabetes impairs vitamin B(6) metabolism at an early stage of women's adulthood». Applied Physiology, Nutrition, and Metabolism. 37 (1): 167–75. PMID 22288928. doi:10.1139/h11-146
- ↑ Ulvik A, Midttun Ø, Pedersen ER, Eussen SJ, Nygård O, Ueland PM (julho de 2014). «Evidence for increased catabolism of vitamin B-6 during systemic inflammation». The American Journal of Clinical Nutrition. 100 (1): 250–5. PMID 24808485. doi:10.3945/ajcn.114.083196

- ↑ Rall LC, Meydani SN (agosto de 1993). «Vitamin B6 and immune competence». Nutrition Reviews. 51 (8): 217–25. PMID 8302491. doi:10.1111/j.1753-4887.1993.tb03109.x
- ↑ Bhagavan HN (1985). «Interaction between vitamin B6 and drugs». In: Reynolds RD, Leklem JE. Vitamin B6: Its Role in Health and Disease. New York: Liss. pp. 401–415
- ↑ Wilson SM, Bivins BN, Russell KA, Bailey LB (outubro de 2011). «Oral contraceptive use: impact on folate, vitamin B₆, and vitamin B₁₂ status». Nutrition Reviews. 69 (10): 572–83. PMID 21967158. doi:10.1111/j.1753-4887.2011.00419.x
- ↑ Schwaninger M, Ringleb P, Winter R, Kohl B, Fiehn W, Rieser PA, Walter-Sack I (março de 1999). «Elevated plasma concentrations of homocysteine in antiepileptic drug treatment». Epilepsia. 40 (3): 345–50. PMID 10080517. doi:10.1111/j.1528-1157.1999.tb00716.x

- ↑ Corken M, Porter J (setembro de 2011). «Is vitamin B(6) deficiency an under-recognized risk in patients receiving haemodialysis? A systematic review: 2000-2010». Nephrology. 16 (7): 619–25. PMID 21609363. doi:10.1111/j.1440-1797.2011.01479.x
- ↑ Kobayashi, Daisuke (2019). «Food poisoning by Ginkgo seeds through vitamin B6 depletion (article in Japanese)». Yakugaku Zasshi. 139 (1): 1–6. ISSN 0031-6903. PMID 30606915. doi:10.1248/yakushi.18-00136

- ↑ Wada, Keiji; Ishigaki, Seikou; Ueda, Kaori; Sakata, Masakatsu; Haga, Masanobu (1985). «An antivitamin B6, 4'-methoxypyridoxine, from the seed of Ginkgo biloba L.». Chemical & Pharmaceutical Bulletin. 33 (8): 3555–3557. ISSN 0009-2363. PMID 4085085. doi:10.1248/cpb.33.3555

- ↑ Schaumburg H, Kaplan J, Windebank A, Vick N, Rasmus S, Pleasure D, Brown MJ (agosto de 1983). «Sensory neuropathy from pyridoxine abuse. A new megavitamin syndrome». The New England Journal of Medicine. 309 (8): 445–8. PMID 6308447. doi:10.1056/NEJM198308253090801
- ↑ Foca FJ (setembro de 1985). «Motor and sensory neuropathy secondary to excessive pyridoxine ingestion». Archives of Physical Medicine and Rehabilitation. 66 (9): 634–6. PMID 2994596
- ↑ Katan MB (novembro de 2005). «[How much vitamin B6 is toxic?]». Nederlands Tijdschrift voor Geneeskunde. 149 (46): 2545–6. PMID 16320662
- ↑ a b Dalton K, Dalton MJ (julho de 1987). «Characteristics of pyridoxine overdose neuropathy syndrome». Acta Neurologica Scandinavica. 76 (1): 8–11. PMID 3630649. doi:10.1111/j.1600-0404.1987.tb03536.x
- ↑ Scientific Panel on Food Additives, Flavourings, Processing Aids and Materials in Contact with Food (2008). «Opinion on Pyridoxal 5′-phosphate as a source for vitamin B6 added for nutritional purposes in food supplements». The EFSA Journal. 760: 1–13. doi:10.2903/j.efsa.2008.760

- ↑ «Vitamin B6». www.nrv.gov.au (em inglês). 17 de março de 2014. Consultado em 20 de abril de 2018. Cópia arquivada em 13 de março de 2018
- ↑ György P (1934). «Vitamin B2 and the Pellagra-like Dermatitis in Rats». Nature. 133 (3361): 498–9. doi:10.1038/133498a0
- ↑ György P, Eckardt RE (setembro de 1940). «Further investigations on vitamin B(6) and related factors of the vitamin B(2) complex in rats. Parts I and II». The Biochemical Journal. 34 (8–9): 1143–54. PMC 1265394
 . PMID 16747297. doi:10.1042/bj0341143
. PMID 16747297. doi:10.1042/bj0341143


