Cromo: diferenças entre revisões
bot : reversão de 201.35.230.200 (vandalismo : -10), revertendo para a versão 15949338" parentid="15949300 de 213.22.205.111 |
|||
| Linha 155: | Linha 155: | ||
==Características principais== |
==Características principais== |
||
O crômio é um [[metal de transição]], [[dureza|duro]], frágil, de coloração cinza semelhante ao [[aço]]. É muito resistente à [[corrosão]]. |
O crômio é um [[metal de transição]], [[dureza|bem duro]], frágil, de coloração cinza cinzado semelhante ao [[aço durão]]. É muito resistente à [[corrosão]]. |
||
Seu maior [[estado de oxidação]] é +6, ainda que estes compostos sejam muito [[redução|oxidantes]]. Os estados de oxidação +4 e +5 são pouco frequentes, enquanto que os estados mais estáveis são +2 e +3. Também é possível obter-se compostos nos quais o crômio apresenta estados de oxidação mais baixos, porém são bastantes raros. |
Seu maior [[estado de oxidação]] é +6, ainda que estes compostos sejam muito [[redução|oxidantes]]. Os estados de oxidação +4 e +5 são pouco frequentes, enquanto que os estados mais estáveis são +2 e +3. Também é possível obter-se compostos nos quais o crômio apresenta estados de oxidação mais baixos, porém são bastantes raros. |
||
Revisão das 12h06min de 19 de agosto de 2009
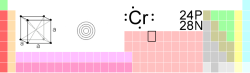
O crômio/cromo (formas aceitas com predileção por crômio[1])PB ou crómioPE, do grego χρώμα, pronunciado como "chrõma", significando cor, é um elemento químico de símbolo Cr, número atômico 24 ( 24 prótons e 24 elétrons ) e massa atômica 52 u, Sólido em temperatura ambiente.
É um metal encontrado no grupo 6 ( 6B ) da Classificação Periódica dos Elementos, empregado especialmente em metalurgia em processos denominados eletrodeposição. Alguns de seus óxidos e cromatos são usados como corantes.
Foi descoberto em 1797 por Louis Nicolas Vauquelin no mineral crocoíta encontrado na Rússia.
Características principais
O crômio é um metal de transição, bem duro, frágil, de coloração cinza cinzado semelhante ao aço durão. É muito resistente à corrosão.
Seu maior estado de oxidação é +6, ainda que estes compostos sejam muito oxidantes. Os estados de oxidação +4 e +5 são pouco frequentes, enquanto que os estados mais estáveis são +2 e +3. Também é possível obter-se compostos nos quais o crômio apresenta estados de oxidação mais baixos, porém são bastantes raros.
Aplicações
- O crômio é empregado principalmente em metalurgia para aumentar a resistência à corrosão e dar um acabamento brilhante.
- Em ligas metálicas. O aço inoxidável, por exemplo, apresenta aproximadamente 8% de crômio.
- Em processos de cromagem que é depositar sobre uma peça uma capa protetora de crômio através da eletrodeposição. Também é utilizado em anodizado de alumínio.
- Seus cromatos e óxidos são empregados em corantes e pinturas. Em geral, seus sais são empregados, devido às suas cores variadas, como mordentes.
- O dicromato de potássio ( K2Cr2O7 ) é um reativo químico usado para a limpeza de materiais de vidro de laboratório e em análises volumétricas.
- É comum o uso do crômio e de alguns de seus óxidos como catalisadores, por exemplo, na síntese do amoníaco ( NH3 ).
- O mineral cromita ( Cr2O3·FeO ) é empregado em moldes para a fabricação de ladrilhos, geralmente materiais refratários. Entretanto, uma grande parte de cromita é empregada para obter o crômio ou em ligas metálicas.
- No curtimento de couros é comum empregar o denominado "curtido ao crômio", sendo este o produto de maior consumo na curtição de couros e peles, consistindo em utilizar o hidroxisulfato de crômio(III) ( Cr)(OH)( SO4 ) .
- Para preservar a madeira costuma-se utilizar substâncias químicas que se fixam a ela, protegendo-a. Entre essas substâncias, aquela usada para proteger a madeira é o óxido de crômio(VI) ( CrO3 ).
- Quando no coríndon ( α-Al2O3 ) se substituem alguns íons de alumínio por íons de crômio, obtém-se o rubi. O rubi pode ser empregado, por exemplo, em laseres.
- O dióxido de crômio ( CrO2 ) é usado para a produção do material magnético empregado em fitas-cassetes para gravação de som, produzindo melhores resultados do que aquelas com óxido de ferro ( Fe2O3 ), devido a sua maior coercitividade.
História
Em 1761, Johann Gottlob Lehmann encontrou nos Urais (Rússia) um mineral de cor laranja avermelhada que denominou de "chumbo vermelho da Sibéria". Esse mineral era a crocoíta ( PbCrO4 ), e acreditou-se, na época, que era um composto de chumbo com selênio e ferro.
Em 1770, Peter Simon Pallas escavou no mesmo lugar e encontrou o mineral, verificando ser muito útil, devido às suas propriedades, como pigmento, em pinturas. Essa aplicação como pigmento difundiu-se rapidamente.
Em 1797, Louis Nicolas Vauquelin recebeu amostras desse material. Foi capaz de, a partir dele, produzir o óxido de crômio (CrO3) misturando crocoíta com ácido clorídrico ( HCl ).
Em 1798, descobriu que se podia isolar o crômio aquecendo o óxido em um forno de carvão. Também pôde detectar traços de crômio em pedras preciosas, como por exemplo, em rubis e esmeraldas. Denominou o elemento de crômio (do grego "chroma", que significa "cor"). devido às diferentes colorações que apresentam os compostos desse elemento.
O crômio foi empregado principalmente como corante em pinturas. No final do século XIX começou a ser utilizado como aditivo em aço. Atualmente, em torno de 85% do crômio consumido é utilizado em ligas metálicas.
Compostos
O dicromato de potássio, K2Cr2O7, é um oxidante enérgico utilizado para limpeza de materiais de vidro de laboratório, eliminando qualquer tipo de resto orgânico que possa conter.
O "verde de crômio" ( óxido de crômio(III) , Cr2O3 ) é um pigmento empregado em pinturas esmaltadas e na coloração de vidros. O "amarelo de crômio" ( cromato de chumbo, PbCrO4 ) também é usado como pigmento.
Não é encontrado na natureza o ácido crômico e nem o dicrômico, porém seus ânions são encontrados numa ampla variedade de compostos. O trióxido de crômio, CrO3, que deveria ser o anidrido do ácido crômico, é vendido comercialmente como "ácido crômico".
O dicromato de amônio, (NH4)2Cr2O7 é o principal material que é expelido dos vulcões em erupção. É um sólido alaranjado.
Papel biológico
Em princípio, se considera o crômio (em seu estado de oxidação +3) um elemento químico essencial, ainda que não se conheça com exatidão suas funções. Parece participar do metabolismo dos lipídios e dos hidratos de carbono, assim como em outras funções biológicas.
Tem-se observado que alguns dos complexos do crômio parecem participar da potencialização da ação da insulina, sendo, por isso, denominado de "fator de tolerância à glicose", devido à relação com a atuação da insulina. A ausência de crômio provoca intolerância à glicose e, como consequência, o aparecimento de diversos distúrbios.
Até hoje não foi encontrada nenhuma metaloproteína com atividade biológica que contenha crômio, por isso ainda não se pode explicar como atua.
Sua carência nos seres humanos pode causar ansiedade, fadiga e problemas de crescimento. Em contraposição, seu excesso (em nível de nutriente) pode causar dermatites, úlcera, problemas renais e hepáticos. [2][3]
Por outro lado, os compostos de crômio no estado de oxidação +6 são muito oxidantes e são cancerígenos.
Abundância e obtenção
Obtém-se crômio a partir da cromita (FeCr2O4). O crômio é obtido comercialmente aquecendo a cromita em presença de alumínio ou silício mediante o processo de redução. Aproximadamente metade da produção mundial de cromita é extraída na África do Sul. Também obtém-se em grandes quantidades no Casaquistão, Índia e Turquia.
Os depósitos ainda não explorados são abundantes, porém estão concentrados no Casaquistão e no sul da África.
Em 2000 foram produzidas aproximadamente 15 milhões de toneladas de cromita, da qual a maior parte destina-se ao uso em ligas metálicas (cerca de 70%) como, por exemplo, para a obtenção do ferrocromo, que é uma liga metálica de crômio e ferro, com um pouco de carbono. Outra parte (cerca de 15% aproximadamente) emprega-se diretamente como material refratário e o restante, na indústria química para a obtenção de diferentes compostos de crômio.
Foram descobertos alguns depósitos de crômio metálico, embora de pequenas quantidades. Numa mina russa (Udachnaya) produzem-se amostras do metal, devido ao ambiente redutor, que facilita a produção de diamantes e crômio elementar.
Isótopos
São encontrados três isótopos estáveis na natureza: crômio-52, crômio-53 e crômio-54. O mais abundante é o crômio-52 (83,789%). Estão caracterizados 19 radioisótopos, sendo o mais estável o crômio-50 com meia-vida superior a 1,8 x 1017 anos, seguido do crômio-51 com meia-vida de 27,7025 dias. Os demais têm meia-vida de menos de 24 horas, e, dentre esses, a maioria com menos de um minuto. Esse elemento também tem dois meta-estados.
O crômio-53 é um produto do decaimento radioativo do manganês-53. Os conteúdos isotópicos no crômio estão relacionados com os do manganês, o que se aplica em geologia. As relações isotópicas de Mn-Cr reforçam a evidência de alumínio-26 e paládio-107 na origem do sistema solar. As variações nas relações de crômio-53/crômio-52 e Mn/Cr em alguns meteoritos indicam uma relação inicial de 53Mn/55Mn, sugerindo que as relações isotópicas Mn-Cr resultam do decaimento in situ de 53Mn em corpos planetários diferenciados. Portanto, o 53Cr fornece evidência adicional de processos nucleossintéticos anteriores à formação do sistema solar.
O peso atómico dos isótopos do crômio varia de 43 u (crômio-43) até 67 u (crômio-67). O principal modo de decaimento antes do isótopo estável mais abundante, o crômio-52, é a captura eletrônica, enquanto que, nos posteriores a aquele, é a desintegração beta.
Precauções
Geralmente, não se considera que o crômio metálico e os compostos de crômio(III) sejam, especialmente, um risco para a saúde. Trata-se de um elemento essencial para o ser humano, porém em altas concentrações é toxico.
Os compostos de crômio(VI) são tóxicos quando ingeridos, sendo a dose letal de alguns gramas. Em níveis não letais, o crômio(VI) (crômio hexavalente) é altamente carcinógeno. A maioria dos compostos de crômio(VI) irritam os olhos, a pele e as mucosas. A exposição crônica a compostos de crômio(VI) pode provocar danos permanentes nos olhos.
A Organização Mundial da Saùde ( OMS ) recomenda desde 1958 uma concentração máxima de 0.05 mg/litro de crômio(VI) na água de consumo. Este valor está sendo revisado, havendo novos estudos sobre os seus efeitos a saúde.
Ligações externas
- WebElements.com - Chromium
- EnvironmentalChemistry.com - Chromium
- International Chromium Development Association
- It's Elemental - The Element Chromium
- Native Chromium
- The Merck Manual - Mineral Deficiency and Toxicity
Referências
- ↑ ROCHA-FILHO, R. C.; CHAGAS, A. P. Sobre os nomes dos elementos químicos, inclusive dos transférmios. Quím. Nova, São Paulo, v. 22, n. 5, 1999. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0100-40421999000500022&lng=pt&nrm=iso>. Acesso em: 10 set. 2007. doi:10.1590/S0100-40421999000500022
- ↑ ANDERSON, R. A. Chromium metabolism and its role in disease processes in man. Clin. Physiol. Biochem., Basel, v. 4, n. 1, p. 31-41, 1986.
- ↑ MERTZ, W. Chromium in human nutrition: a review. J. Nutr., Philadelphia, v. 123, n. 4, p.626-633, Apr. 1993. Disponível em: <http://jn.nutrition.org/cgi/reprint/123/4/626.pdf>. Acesso em: 5 jul. 2009.