Usuário(a):Lucas Sassi/Síntese de Materiais Nanoestruturados
A síntese de materiais nanoestruturados é de suma importância para o desenvolvimento da nanotecnologia, sendo o processo de partida para a construção dos mais distintos dispositivos e produtos em escalas nanométricas. Pode-se dividir os materiais nanoestruturados em três grande grupos: os blocos básicos de construção, os dispositivos de 2ª geração e os dispositivos de 3ª geração.
Os blocos básicos de construção consistem das unidades básicas que vão, por sua vez, compor os sistemas de 2ª e 3ª geração. Enquadram-se na condição de blocos básicos de construção os sistemas 0D como nanopartículas e nanoclusters, os sitemas 1D, como nanotubos e nanofios, os sistemas 2D, como o grafeno e os sistemas porosos, como as zeólitas.
Os dispositivos de 2ª geração consistem em nanoestruturas formadas a partir da aplicação dos princípios da química supramolecular nos blocos básicos de construção. A escolha de subunidades segue uma lógica que considera sua geometria e capacidade de formação de ligações intermoleculares (como ligação de hidrogênio, complexo de coordenação, interação pi-pi) reversíveis, de modo que a estrutura desejada seja termodinamicamente a mais favorável, e se forme espontaneamente por automontagem(self assembly).[1] Destacam-se, dentre os dispositivos de 2ª geração, aqueles formados por arquiteturas moleculares mecanicamente ligados, como catenanos, pseudorotaxanos e rotaxanos, macrociclos com cavidades com capacidade de reconhecimento molecular, como ciclodextrinas e calixarenos, e origamis de DNA, que usam ácidos nucleicos para a formação de estruturas específicas. Podem ser aplicados na síntese de interruptores moleculares, motores moleculares, portas lógicas moleculares, propulsores moleculares, entre outros.
Os dispositivos de 3ª geração, por fim, são o uso das nanoestruturas tanto de 1ª quanto de 2ª geração em aplicações específicas, de modo a criar materiais com as propriedades controladas em escala nanométrica. Suas aplicações incluem, por exemplo, o uso de deposição de nanofios (1ª geração) para formação de circuitos eletrônicos, o uso de portas lógicas moleculares (2ª geração) para a formação de um computador químico, uso de complexos com ciclodextrinas (2ª geração) para sistemas de drug delivery, entre outros.
Blocos Básicos de Construção[editar | editar código-fonte]
Sistemas 0D[editar | editar código-fonte]
Para a fabricação de nanopartículas, em caso de qualquer aplicação prática, não devemos nos preocupar apenas com o tamanho, mas também com o controle das condições de processamento de forma que as nanopartículas venham a ter as seguintes características:[2]

- Uniformidade do tamanho de todas as partículas.[2]
- Uniformidade da forma e morfologia.[2]
- A composição química e a estrutura cristalina idênticas que são desejadas entre diferentes partículas e dentro de partículas individuais, como o núcleo e a composição superficial devem ser as mesmas.[2]
- Dispersão individual ou mono-dispersão, ou seja, supressão da aglomeração. Caso isto aconteça, as nanopartículas devem ser facilmente redispersas.[2]
- Crescimento monodisperso, isto é, crescimento por difusão controlada/Ostwald ripening.[3]
- Formação de alto grau de supersaturação com um tempo ou espaço estreito.[3]
A preparação de nanopartículas é dividida em duas técnicas, top-down e bottom-up. Na síntese por top-down nanopartículas são produzidas diretamente de materiais bulk (sólido massivo), ou seja, ocorre a remoção de partes do bulk para gerar pequenas partículas. O método usado dependerá do material usado no substrato e das dimensões do material desejado. Os processos poderão ser de natureza mecânico-físicos, eletroquímicos, químicos, etc.[4] e as técnicas podem ser atrito ou moagem (ball milling), laser ablation, técnicas de litografia, ciclos termais repetitivos, laser beam, etc.[5][6][2]
Sendo a técnica mais usada, o bottom-up é a construção de materiais átomo por átomo, molécula por molécula ou cluster por cluster (agregado atômico) desde a base do objeto. São muitas as técnicas de síntese que podem ser usadas, mas podemos classifica-las em abordagens de equilíbrio termodinâmico e de cinética. Na abordagem termodinâmica, as sínteses consistem de geração de supersaturação, nucleação (homogênea ou heterogênea) e crescimento. Na abordagem cinética a síntese ocorre limitando-se a quantidade de precursores disponíveis para o crescimento ou confinando o processo em um espaço limitado, como em sínteses com aerosol ou micelas.[2]
Top-Down[editar | editar código-fonte]
Trituração[editar | editar código-fonte]
Esta técnica pode ocorrer como um processo mecânico-físico ou mecânico-químico. O material a ser triturado(metálicos e cerâmicos), geralmente na forma de pó, é pulverizado por bolas de trituração altamente energéticas em moinhos oscilatórios. O material das bolas e do moinho de trituração deve ser escolhido de forma a serem resistentes à abrasão, como oxido de zircônio minimizando a contaminação da amostra pela a abrasão. Outro fator que se deve levar em conta é o meio de dispersão para garantir a melhor dispersão possível evitando agregados. Além disso, o tamanho das bolas de trituração e o tempo devem ser bem escolhidos dependendo da amostra. Esta técnica, no entanto, produz partículas de tamanhos relativamente amplos e não é possível o total controle sobre a forma da partícula.[7][8]
Ciclos termais repetitivos[editar | editar código-fonte]
Esta técnica é possível se o material tem uma pequena condutividade térmica, mas uma grande variação de volume em função da temperatura. Uma grande variação de volume associada com uma transformação de fase pode ser eficientemente utilizada nesta técnica. Apesar de ser possível obter partículas bem pequenas, esta não é uma técnica, a qual se pode controlar o tamanho e forma facilmente.[9]
Laser Ablation[editar | editar código-fonte]
É uma técnica de remoção de material de uma superfície sólida de um bulk mergulhado em solução líquida através de irradiação por laser. Em baixo fluxo, o material é aquecido ao absorver energia do laser e evapora ou sublima. Em um alto fluxo, o material é convertido em plasma. Neste último as nanopartículas são formadas durante a condensação da pluma de plasma . Esta técnica é considerada uma “técnica verde” alternativa ao método de redução química para obtenção de nanopartículas metálicas nobres . Entretanto, o problema desta técnica é a alta energia exigida por unidade de nanopartículas metálicas produzida e o pequeno controle sobre a taxa de crescimento das nanopartículas metálicas.[10][11]
Sonoquímica[editar | editar código-fonte]
Irradiações de ultrassom causam uma cativação acústica – formação, crescimento e colapso implosivo de bolhas em um líquido. Estes colapsos implosivos geram regiões extremamente quentes (temperaturas de aproximadamente 5000 °C) e de alta pressão (100 atm) no liquido, conhecidas como pontos quentes ("hot-spots").[4]
Nanolitografia[editar | editar código-fonte]
- Litografia óptica: É capaz de produzir padrões de 100 nm com a utilização de comprimentos de onda onda muito curtos (atualmente 193 nm). Esta técnica requer a utilização de imersão num líquido e uma série de tecnologias de aperfeiçoamento de resolução, como (phase-shift masks (PSM) e correção de proximidade óptico (OPC) na espessura de 32 nm. A maioria dos especialistas considera que as técnicas tradicionais de litografia óptica não vão ser rentáveis abaixo de 22 nm. Neste ponto, pode ser substituída por uma nova geração de litografia técnica (LGN).[12]
- Litografia por raio-x: Litografia por raios-x pode ser estendida para uma resolução óptica de 15 nm, utilizando os comprimentos de onda curtos de 1 nm para a iluminação. Isto é implementado através da abordagem de impressão de proximidade. A técnica foi desenvolvida para a extensão de processamento em lote. A extensão do método baseia-se na Near Field X-Ray na difração de Fresnel. O método é simples porque não necessita de lentes.
- Litografia por UV extemo: É uma forma de litografia ótica usando comprimentos de onda muito curtos (13,5 nm). É a técnica mais popular entre as Next-Generation Lithography (NGL) que é um termo usado na fabricação de circuitos integrados para descrever as tecnologias de litografia programados para substituir fotolitografia.
- Scanning Probe lithography (SPL): É uma promissora ferramenta para padronização na escala nanométrica. Por exemplo, os átomos individuais podem ser manipulados usando a ponta de um microscópio de tunelamento (STM). Dip Pen Nanolithography (DPN) é a primeira tecnologia SPL disponível comercialmente com base em microscopia de força atômica.
Bottom-up[editar | editar código-fonte]
Abordagem termodinâmica[editar | editar código-fonte]
- Nanopartículas por nucleação homogênea
Para a formação de nanopartículas por nucleação homogênea, é necessária uma supersaturação das espécies em crescimento. Uma redução da temperatura da mistura saturada poderia levar a uma supersaturação. Um exemplo seria a fabricação de rebites usados na carcaça de aeronaves, onde se usa o Duralumínio e o princípio do endurecimento por precipitação. Outra alternativa de gerar supersaturação seria através de reações químicas in situ convertendo soluções químicas altamente solúveis em soluções menos solúveis. Por exemplo, nanopartículas de semicondutores que são produzidas por pirólise de precursores organometálicos. Nanopartículas sintetizadas por nucleação homogênea podem ocorrer em três meios: liquido, gás e sólido.[2]
Nucleação homogênea
Na nucleação homogênea os núcleos da nova fase se forma de maneira uniforme ao longo e toda a fase original. Quando a concentração de um soluto em um solvente excede o equilíbrio de solubilidade ou a se a temperatura é diminuída abaixo do ponto de transformação de fase, uma nova fase aparece. Vamos considerar, por exemplo, o caso de uma nucleação homogênea na fase sólida de uma solução supersaturada. Ao exceder a solubilidade o soluto causa muita distorção na estrutura cristalina do solvente e a Energia livre de Gibbs aumenta muito. Para que esta energia possa diminuir e uma vez que o soluto não tem como sair da rede, a maneira encontrada é a nucleação e formação de uma nova fase.[2]
Observa-se então que quanto mais se abaixa o , ou seja, quanto mais negativo o delta G maior a força motriz para a ocorrência da nucleação e, posteriormente, crescimento. O excesso de energia livre, , entre uma pequena partícula de soluto (assumindo, por simplicidade, ser uma esfera de raio r) e o soluto em uma solução é igual à soma da energia livre de volume, × volume do núcleo esférico e a energia livre de superfície, × área de superfície do núcleo, ou seja, o excesso de energia livre entre uma partícula muito grande (r = ∞) e um soluto em uma solução. Sabendo que é positivo e proporcional a e é negativo e proporcional a , a equação total de energia livre é:[13]
onde é a diferença de energia livre de transformação por unidade de volume e é a tensão interfacial (energia de superfície) entre a superfície cristalina em desenvolvimento e a solução supersaturada onde esta localizada.

Os dois termos à direita da equação de energia livre total possuem sinais opostos e dependem diferentemente em relação ao r, assim o passa por um máximo ou valor crítico, que corresponde a um raio crítico, . Sabendo que , é definido pelas seguintes derivações:[13]
Substituindo a equação do raio crítico acima na equação de energia livre total, obtemos:
O comportamento da nova estrutura cristalina formada na solução supersaturada dependerá de seu tamanho. representa o tamanho mínimo que um núcleo deverá ter para ser estável. Caso (clusters ou embriões) o sistema pode ter sua energia livre abaixada pela dissolução das partículas sólidas ou pela evaporação se a partícula é um líquido em um vapor supersaturado. Se (núcleos) a energia livre diminuirá devido ao crescimento das partículas.[13]
O termo pode ser relacionado com a temperatura de equilíbrio, entalpia de fusão, , e o grau de subresfriamento, :[14]
Avaliando esta equaçao no ponto de equilíbrio() na temperatura de fusão teremos:
Substituindo na primeira equação temos:
Usando denominadores comuns e a definição , temos que:
A medida que a transformação de fase se torna mais e mais favorável, a formação de um determinado volume do núcleo de energia livre suficiente para formar uma superfície cada vez maior, permite que núcleos cada vez menores se tornarem viáveis Estes podem etão crescer até atingirem o Equilíbrio termodinâmico.
Um alto grau de sub-resfriamento favorece transformações de fase e podemos relacionar com sub-resfriamento e achar e como função de substituindo :[13]
e
Assim, com um abaixamento de temperatura abaixo da em condições de equilíbrio , a nucleação ocorre de maneira mais imediata. Além disso, o número de núcleos estáveis, n*, também esta em função da temperatura é dado por: [15]

onde é a Constante de Boltzmann e é o número total de núcleos no sistema. Outra dependência da temperatura é a frequência segundo a qual os átomos da solução se fixam ao núcleo sólido, :
onde é a energia de ativação ( parâmetro independente da temperatura) e é uma constante independente da temperatura.
Nucleação heterogênea

Quando uma nova fase é formada preferencialmente em heterogeneidades estruturais, como superfície de recipientes, impurezas insolúveis, contornos de grão ou em defeitos cristalinos o processo é chamado nucleação heterogênea. Isto ocorre, pois será mais fácil ocorrer a nucleação, a sub-resfriamentos baixos, quando a energia superficial é reduzida. Vamos considerar uma nucleação heterogênea em uma superfície plana e sólida. As espécies de crescimento se difundem e se agregam para formar um núcleo com um formato de tampa. A mudança global de energia livre associada com a formação de um núcleo crítico sob condições heterogêneas, , deverá ser menor do que o da nucleação homogênea:
onde esta entre 0 e 1. Como dito antes, as espécies de crescimento formam um núcleo no formato de uma tampa. Neste exemplo teremos então duas fases com contato, duas sólidas e uma líquida.

As três tensões de interfaces,, são chamadas de (entre a fase cristalina sólida e o líquido), (entre a superfície sólida e o líquido) e (entre a fase cristalina sólida e a superfície sólida) e o ângulo teta, ângulo de contato entre o depósito cristalino e a superfície sólida, corresponde ao ângulo de molhabilidade (Wetting) do sistema sólido/líquido:
Assim como na nucleação homogênea, o número de núcleos formados será dado pela formula:

A barreira de energia necessária para a nucleação heterogênea é reduzida, e menos de sub-resfriamento é necessário. O ângulo de molhabilidade determina a facilidade de nucleação através da redução da energia necessária. O volume pode ser significativamente menor para a nucleação heterogênea, devido ao ângulo de molhabilidade que afetado a forma do cluster. No caso da nucleação heterogênea, alguma energia é libertada pela destruição parcial da interface anterior. Por exemplo, se uma bolha de dióxido de carbono é formada entre a água e a superfície interior de uma garrafa, a energia inerente na interface água-frasco é libertada sempre que uma camada de gás intervier, e esta energia vai para a formação da bolha de água e da interface bolha-garrafa. O mesmo efeito pode fazer com que partículas de precipitado se formem nos contornos de grão de um sólido. Isto pode interferir com o fortalecimento da precipitação, que se baseia na nucleação homogênea para produzir uma distribuição uniforme de partículas de precipitado.
- Crescimento[2]
Para síntese de nanopartículas com distribuição uniforme de tamanho, é melhor se todos os núcleos forem formados ao mesmo tempo, uma que serão formados sob as mesmas condições. Além disto, todos os núcleos terão o mesmo crescimento. Na prática, para se obter uma curta nucleação, a concentração das espécies em crescimento é aumentada abruptamente até uma alta supersaturação e depois rapidamente levada a uma concentração mínima de nucleação. Abaixo dessa concentração nenhum novo núcleo é formado, enquanto que os núcleos existentes continuarão a crescer até que a concentração das espécies em crescimento se reduza a uma concentração de equilíbrio. A distribuição de tamanho das nanopartículas pode ser alterada na etapa de crescimento dependendo da cinética desta etapa. O crescimento dos núcleos envolve as seguintes etapas:
- Geração de espécies de crescimento
- Difusão das espécies de crescimento do bulk para a superfície de crescimento
- Adsorção das espécies de crescimento na superfície de crescimento
- Crescimento da superfície através da incorporação irreversível de espécies de crescimento na superfície sólida
Estes passos podem ser ainda divididos em dois processos. O fornecimento das espécies de crescimento para a superfície de crescimento é designada como a difusão, que inclui a geração, difusão e adsorção de espécies de crescimento sobre a superfície de crescimento, enquanto que a incorporação de espécies de crescimento adsorvida sobre a superfície de crescimento na estrutura do sólido é denotado como o crescimento. Um crescimento de difusão limitada poderia resultar numa distribuição de tamanho diferente de nanopartículas, em comparação com aquela de crescimento limitado.
A taxa de crescimento:
onde (energia de ativação)e (pre-exponencial)são independentes da temperatura.
Sol-gel[2][editar | editar código-fonte]
A técnica por sol-gel é uma via química úmida para a síntese de dispersões coloidais de compostos inorgânicos e materiais híbridos orgânicos-inorgânicos, em particular óxidos e óxidos híbridos básicos. A partir de tais dispersões coloidais, pós, fibras e películas finas podem ser prontamente preparados. Embora a fabricação de diferentes formas de produtos finais requerer algumas considerações específicas, os fundamentos e abordagens gerais na síntese de dispersões coloidais são os mesmos. O método sol-gel oferece muitas vantagens, incluindo a baixa temperatura de processamento e um nível homogeneidade molecular. O método sol-gel é particularmente útil na fabricação de óxidos metálicos complexos, materiais híbridos orgânicos-inorgânicos sensíveis a temperatura e os materiais termodinamicamente desfavoráveis ou metaestáveis. Processamentos típicos por sol-gel consistem de hidrólise e condensação de precursores. Precursores podem ser tanto metais Alcóxido ou sais orgânicos e inorgânicos. Solventes orgânicos ou aquosos os podem ser utilizados para dissolver os precursores, e os catalisadores são muitas vezes adicionados para promover reações de hidrólise e de condensação:
Hidrólise:
M(OEt)4 + xH20 ←→ M(OEt)4-x(OH)x + xEtOH
Condesação:
M(OEt)4-x(OH)x + M(OEt)4-x(OH)x ←→(OEt)4-x(OH)x-1MOM(OEt)4-x(OH)x-1+ H20
Síntese solvotérmica[16][editar | editar código-fonte]
síntese solvotérmica é um método de produção de compostos químicos. É muito semelhante à rota hidrotérmica (em que a síntese é realizada num autoclave de aço inoxidável), sendo a única diferença que a solução precursora geralmente não é aquoso (no entanto, este não é sempre o caso em toda a literatura que usa esta expressão) . Esta técnica proporciona um controle preciso sobre o tamanho, distribuição da forma e cristalinidade da cristalização das nanopartículas sintetizadas. Estas características podem ser alteradas, alterando alguns parâmetros experimentais, incluindo a temperatura de reação, tempo de reação, o tipo de solvente, tipo de agente tensoativo o tipo de precursor. O processo de reação é conduzida acima do ponto de ebulição do solvente e da pressão interna, e envolve um solvente quente dentro de um autoclave (vaso fechado). O processo é chamado de síntese hidrotérmica, quando o solvente é a água.
Gás Inerte de Condensação ou Inert gas condensation (IGC)[16][editar | editar código-fonte]
O IGC envolve a evaporação de uma substância de origem em uma atmosfera de gás inerte. Os nanopós produzidos são transportados por convecção e recolhida sobre um substrato frio. Embora este processo seja conhecido desde 1930 para a produção de partículas metálicas ultrafinas, a sua aplicação dirigida à produção de nanopartículas não ocorreu até recentemente. Com IGC, é geralmente inferido que o processo é um processo físico de deposição de vapor (PVD). Se, além disso um processo catalítico for envolvido, referimo-nos a ela como deposição de vapor químico (CVD). CVD envolve a reação ou decomposição térmica de espécies em fase gasosa a temperaturas elevadas (~500-1000 ° C). Os produtos de PVD e CVD são coletados em uma segunda etapa.
Abordagem cinética[2][editar | editar código-fonte]
Crescimento cineticamente controlado consiste em confinar espacialmente o crescimento, assim o crescimento para quando a quantidade limitada de materiais de base ou é consumido ou o espaço disponível é preenchido. Muitos confinamentos espaciais foram estabelecidos para a síntese de nanopartículas. Em geral confinamentos espaciais podem ser divididos em vários grupos: gotículas de líquido dentro de uma fase gasosa, incluindo sínteses aerossol e Metalização (spray pyrolysis), gotículas de líquido em líquidos tais como micelas e síntese de micro-emulsão, término de crescimento e síntese de auto término.
Síntese dentro de Micelas ou usando Micro-emulsões[2][editar | editar código-fonte]
Na síntese de micelas, as reações prosseguem entre os reagentes que estão disponíveis apenas no interior da micela e a partícula para de crescer quando os reagentes são consumidos. Agentes surfactantes ou polímeros de bloco iram residir na interface separando hidrocarbonetos e soluções aquosas. Uma micro-emulsão é uma dispersão de finas gotículas líquidas de uma solução orgânica em uma solução aquosa. As reações químicas podem ter lugar tanto nas interfaces entre as gotículas orgânicas e solução aquosa, quando os reagentes são introduzidos separadamente em duas soluções não-miscíveis, ou no interior das gotículas orgânicas quando todos os reagentes são dissolvidos nas gotículas orgânicas.
Aerossol[2][editar | editar código-fonte]
A formação de nanopartículas pelo método do aerossol é diferente de outros métodos em vários aspectos. Em primeiro lugar, o método de aerossol pode ser considerado como uma abordagem top-down, em comparação com outros métodos, os quais têm uma abordagem bottom-up. Em segundo lugar, as nanopartículas podem ser policristalinas em comparação tanto com um monocristalina quanto com uma estrutura amorfa de nanopartículas preparadas por outros métodos. Em terceiro lugar, as nanopartículas preparadas precisam ser coletadas e redispersas para muitas aplicações. Neste método, um precursor líquido é primeiramente preparado. O precursor pode ser uma simples solução de mistura de elementos desejados ou uma dispersão coloidal. Tal precursor líquido é então mistified para fazer um aerossol líquido, isto é, uma dispersão de gotículas uniformes de líquido em gás, o qual pode simplesmente solidificar pela evaporação do solvente ou ainda reagir com os produtos químicos que estão presentes no gás. As partículas resultantes são esféricas e seu tamanho é determinada pelo tamanho das gotículas de líquido iniciais e pela concentração do sólido. Os aerossóis podem ser facilmente produzidos por sonicação ou centrifugação.
Término de Crescimento[2][editar | editar código-fonte]
Na síntese de nanopartículas, o tamanho pode ser controlado pelo assim chamado Térmion de crescimento. A abordagem é conceitualmente simples. Quando componentes orgânicos ou íons estranhos são fortemente ligados à superfície de crescimento fazendo com que todos os locais de crescimento disponíveis estejam ocupados , o processo de crescimento para.
Metalização(spray pyrolysis)[17][editar | editar código-fonte]
Spray pyrolysis é, basicamente, um processo em solução e tem sido amplamente utilizada na preparação de pó metálico e de óxido de metálicos. O processo pode ser simplesmente descrito como a conversão de gotículas líquidas micrométricas de precursores ou uma mistura de precursor em partículas sólidas por meio de aquecimento. Na prática, spray pyrolysis envolve várias etapas: (china)
- gerar gotículas micrométricas de precursor líquido ou solução precursora
- evaporação do solvente
- condensação de soluto
- decomposição e reação do soluto
- sinterização das partículas sólidas
Outra utilização do spray pyrolysis é na fabricação de nanopartículas de GaO3 que é o material de partida para nanopartículas de nitrato de gálio (GaN) que têm grande potencial na fabricação de "laser diodes", transistores de efeito de alta velocidade, fotodetectores de UV, aparelhos eletrônicos de alta temperatura . Spray pyrolysis também foi aplicado com sucesso na produção de partículas. O processo envolveu a formação de micro-gotas de partículas nano-primárias misturadas com esferas de polímero de látex (poliestireno (PSL)), que foram depois removidas por secagem.
Sistemas 1D[editar | editar código-fonte]
Dentre os sistemas unidimensionais dos blocos básicos de construção se destacam os nanofios, nanobastões e nanotubos. Essas morfologias têm se mostrado de grande valia para a produção de fios moleculares para circuitos em escala nanométrica, transistores, sensores, elementos integrantes de LEDs e LASERS, dentre outras aplicações em que podem ser úteis.[18] A diferença entre nanofios e nanobastões reside na diferença de proporção de tela ("Aspect ratio" em inglês) entre as estruturas, isto é, a razão entre o comprimento do eixo maior e a largura do eixo menor da estrutura unidimensional [19]. Nanobastões possuem proporção de tela um pouco menor que nanofios, enquanto nanotubos possuem uma proporção de tela muito maior em relação a essas duas morfologias[18], isto é, nanotubos possuem seu comprimento bem maior em relação ao seu diâmetro. Além disso, nanofios e nanobastões apresentam, em geral, as mesmas técnicas de síntese, que diferem das técnicas de síntese de nanotubos.
Síntese de Nanofios e Nanobastões[editar | editar código-fonte]
Síntese Assistida por Moldes [20][editar | editar código-fonte]

Uma interessante estratégia de síntese em nanotecnologia, em geral, é produzir a morfologia de interesse a partir de um molde. Para a síntese de nanofios e nanobastões, os moldes mais utilizados na literatura consistem de uma matriz na qual são feitas poros com diâmetro e espaçamento desejado para os nanofios. Um dos moldes mais utilizados é a alumina (Al2O3) anodizada, retratada na figura ao lado.
Os moldes de alumina porosos são produzidos através da anodização de filmes de alumínio em meios ácidos. Sob cuidadosas condições de anodização, a camada de óxido resultante do processo possuirá um arranjo hexagonal de nanocanais paralelos, como se pode ver na figura ao lado. É possível controlar o diâmetro dos canais e a densidade de poros variando as condições de anodização. O fato de os poros possuirem diâmetros organizados é devido a um delicado ajuste nas taxas de crescimento e de dissolução da alumina no meio ácido [21] e acredita-se que o ordenamento dos poros se deve a um estresse mecânico na interface alumínio-alumina, o que faz com que os poros se organizem numa estrutura de rede hexagonal[22]. Existem também outros tipos de moldes que também são bastantes utilizado como, por exemplo, membranas fabricadas por bombardeamento de íons, peneiras moleculares mesoporosas, membranas sintetizadas por litografia de feixe de elétrons, dentre outras.
Após a formação do molde, é preciso preenchê-lo com o material com que se deseja formar os nanofios. Existem três formas de se depositar materiais nos poros:
- Injeção por pressão (Pressure Injection):
Através desse método, os nanofios ou nanobastões são formados a partir da injeção do material desejado na forma líquida no interior dos poros do molde. Entretanto, é necessário aplicar uma determinada pressão ao material para que ele vença a tensão superficial e possa preencher os poros do molde. A equação de Washburn fornece a pressão P necessária para que um material líquido preencha poros de diâmetro d, a saber:
onde d é o diâmetro do poro, γ é a tensão superficial do liquido, θ é o ângulo de contato entre o líquido e o molde. Muitas vezes, surfactantes são adicionados aos poros para reduzir a tensão superficial e o ângulo de contato, dessa forma, a pressão necessária para injetar o líquido nos poros diminui. Em geral, nanofios crescidos por esse processo, apresentam alta cristalinidade e uma orientação cristalina preferencial ao longo do eixo do fio.
- Deposição eletroquímica
Essa técnica é bastante utilizada na produção de nanofios, especialmente na produção de heteroestruturas de nanofios, isto é, nanofios que possuem dois constituintes diferentes em sua estrutura como nanofios de Cu/Co, por exemplo. Para ocorrer a deposição, uma fina camada metálica é depositada em um dos lados da membrana porosa para servir de cátodo para a eletrodeposição. Dessa forma, a deposição do metal de interesse acontece no anodo que está no interior dos poros. Dessa forma, os poros vão sendo preenchidos com o material de interesse e o comprimento dos nanofios podem ser controlados, variando-se o tempo de deposição. Em geral, os nanofios resultantes são policristalinos e não possuem orientação cristalina preferencial, o que difere dos nanofios sintetizados pelo método de injeção por pressão. Porém, como esse método não se baseia na alta pressão e na tensão superficial envolvida para inserir o material no interior dos poros, é possível sintetizar fios de diâmetros menores em relação ao método de injeção por pressão.
Entretanto, uma importante aplicação desse tipo de deposição é a fabricação de heteroestruturas, como nanofios compostos de dois elementos distintos ou os nanobastões "código de barra". Começa-se a deposição com um determinado metal A, essa deposição é interrompida e, em seguida, começa-se a deposição de um metal B e, desse modo, pode-se voltar a se depositar o material A ou fazer ainda, a deposição de um terceiro metal. O comprimento das camadas metálicas vão depender do tempo de deposição[18]. Na figura abaixo, é possível o que é uma heteroestrutura de nanofio com a estrutura de um nanofio de GaP/GaAs crescida pelo mecanismo VLS.
- Deposição em fase de vapor (Vapor Deposition)
A deposição em fase de vapor de nanofios inclui a deposição física de vapor e a deposição química em fase vapor. Na primeira técnica de deposição, o material a ser usado para preencher os poros é aquecido de forma s ser produzido um vapor desse material e então, esse material é introduzido nos poros e resfriado até se solidificar com a ajuda de um aparato experimental desenhado para este fim [23]. Na deposição química em fase vapor, o que ocorre, basicamente, é a reação de gases, dando origem a intermediários gasosos que, em seguida, entram em contato com a superfície dos poros o que, por sua vez, promove reações de deposição dos metais presentes nesses intermediários no interior dos poros.
Mecanismo Vapor-Líquido-Sólido (VLS)[editar | editar código-fonte]

Uma das estratégias de síntese mais bem sucedidas de nanofios é o mecanismo VLS, visto que é possível ter controle sobre o diâmetro, comprimento e composição dos fios. Inicialmente, essa não era uma técnica para a produção de nanofios, mas a para a produção de fios em escala micrométrica, porém foi bem adaptada para a produção de fios em escala nanométrica. Nessa técnica, precursores na forma gasosa reagem dando origem a produtos também gasosos. Para que o mecanismo ocorra, é preciso de gotas de ligas metálicas que vão catalisar a reação. Essa catálise ocorre com a adsorção, na superfície da gota catalítica, de componentes na forma gasosa, formados a partir da reação dos precursores colocados no reator. Isso ocorre até que a liga se torna supersaturada e isso faz com que, por sua vez, um dos componentes se precipite, dando origem a formação dos fios[24].

A figura ao lado ilustra esse processo. Pode-se observar que o SiCl4 reage com o gas H2 fornecendo Si e HCl como produtos. O Si, por sua vez, é incorporado à gota da liga de Au-Si. Quando a concentração de silício na gota deixa de estar no equilíbrio, isto é, quando o silício se torna supersaturado na gota, ele começa a precipitar e passa a se formar uma camada de silício com a forma na gota na interface sólido-líquido. Enquanto houver silício sendo produzido na reação dos gases e fornecido para a gota, o fio continuará crescendo. Como estão envolvidas as fases de vapor (contém os reagentes e o material do qual o fio será formado), líquida (gota da liga metálica que catalisa a reação) e sólida (elemento da liga que se precipita), o processo é chamado de mecanismo vapor-líquido-sólido[24].
Todavia, para fazer com que o fio resultando do processo esteja em escala nanométrica, é necessário que as gotas catalizadoras estejam também nessa escala. Esse obstáculo conseguiu ser superado com o avanço das técnicas de síntese de nanoclusters, o que possibilitou que eles pudessem ser dispersados num substrato e, quando a temperatura fosse elevada acima do ponto de fusão desses clusters, eles não se agregassem e coma descoberta de que ilhas metálicas em nanoescla podem se auto-organizar quando uma fina camada tensa é crescida ou tratada termicamente em um substrato não epitaxial[20].
Uma outra forma de produzir nanofios é combinar o mecanismo VLS com o mecanismo de "Laser Ablation". A reação gasosa ocorre no ambiente, entretanto ao invés de se ter gotas de ligas metálicas que catalisam a reação, tem-se nanoclusteres no substrato. Então, um feixe de laser extremamente colimado incide sobre alguns desses clusteres, fazendo com que o mecanismo VLS se inicie. Um exemplo disso é o de que quando se incide laser em nanoclusters de ouro na presença dos precursores silano e Argônio, aquecendo os clusteres a uma temperatura suficiente para iniciar o crescimento VLS, nanofios de silício são sintetizados. É interessante observar que essa é uma forma de sintetizar nanofios em posições bem determinadas[18].
Também é possível utilizar o mecanismo VLS para sintetizar heteroestruturas de nanofios, como se pode ver na figura ao lado. Para isso, é necessário variar a composição dos precursores da fase gasosa durante o crescimento. Por sua vez, para conseguir fazer isso é necessário um profundo conhecimento do diagrama de fase dos precursores gasosos e da liga presente na gota catalisadora.
Síntese de Nanotubos de Carbono[editar | editar código-fonte]


Em relação à síntese de nanotubos, destaca-se na literatura a síntese de nanotubos de carbono, em virtude de suas interessantes propriedades elétricas, térmicas, mecânicas e ópticas que podem são de grande interesse no meio industrial. Dessa forma, basicamente todas as técnicas citadas nessa seção dirão respeito à síntese de nanotubos de carbono.
Os nanotubos de carbono podem ser classificados como nanotubos parede única ou multi-parede. A primeira imagem mostra um nanotubo parede única, enquanto a imagem seguinte retrata um nanotubo multi-parede (na figura em questão o nanotubo possui parede tripla). É importante ter controle de síntese de ambas as estruturas, visto que as propriedades dos nanotubos variam de acordo com a estrutura que ele apresenta. Os nanotubos ainda podem ser classificados quanto a sua quiralidade, porém isso não será discutido nesse artigo.
Com relação à síntese de nanotubos, a situação ideal é saber controlar a quiralidade, pureza e qualidade estrutural dos nanotubos e conseguir fazer isso em larga escala. Entretanto, para isso, seria necessário entender perfeitamente os mecanismos de crescimento e nucleação de nanotubos, o que permanece objeto de muita controvérsia e intenso esforço experimental de grupos de pesquisa de todo o mundo. Esse problema é basicamente explicado pela ainda falta de conhecimento de como diversos parâmetros afetam as condições de síntese e no papel dos catalisadores durante o crescimento dos nanotubos.
Laser Ablation[editar | editar código-fonte]
O aparato experimental mais simples para se explicar essa técnica consiste de um tubo de quartzo que é aquecido por fornos em seu exterior a uma temperatura em torno de 1200ºC. NO interior do tubo, por sua vez, existe um alvo de grafite contendo catalisador metálico (geralmente um metal de transição ou uma liga de metais de transição) e um tubo coletor de cobre, que é resfriado com água. Além disso, o interior do tubo de quartzo é preenchido com um gás inerte. Então, um raio de laser é focado para atingir o alvo de grafite, vaporizando e sublimando o grafite. Isso, por sua vez, gera uma fuligem formada de carbono e catalisadores. É nessa fuligem que a reação ocorre e as espécies de carbono geradas após essa transferência de energia do laser para o alvo de grafite são arrastadas pelo fluxo de gás inerte e depositadas no coletor de cobre e nas paredes do tubo de quartzo[20].
Uma série de modificações foram feitas nesse método a fim de aumentar a eficiência como, por exemplo, empregar um segundo laser (pulsado) que segue os pulsos do primeiro laser, porém numa frequência diferente, fazendo com que os agregados de carbono que se formam após o primeiro laser incidir se desfaçam, fornecendo um maior estoque de carbono para que a síntese ocorra[25], dentre muitas outras modificações.
Na ausência de catalisador no alvo, a fuligem coletada continha, principalmente, nanotubos multi-parede (tipo c). A quantidade e a qualidade estrutural dependem da temperatura do forno. Estruturas com menos defeitos são obtidas quando se ajusta a temperatura do forno para 1200ºC, isto é, para temperaturas menores, as estruturas obtidas apresentam maior quantidade de defeitos. Porém, à medida que pequenas quantidades de metais de transição são incorporados ao alvo de grafite, a fuligem coletada apresenta maior quantidade de nanotubos de carbono parede única ao invés de nanotubos multi-parede, entretanto a síntese de nanotubos parede única depende do tipo de catalisador utilizado e parece aumentar com a temperatura do forno, dentre outros fatores. Uma outra característica da síntese de nanotubos parede única por esse método é a de que ele pode dar origem a nanotubos mais "limpos", ou seja, associado com uma menor quantidade de carbono em fase amorfa ligado à parede dos nanotubos, em relação a outras técnicas, embora isso dependa muito das condições de síntese. Pode-se, observar, portanto que as condições de síntese influenciam diretamente nos produtos resultantes. Nessa técnica, os parâmetros mais estudados são a natureza do alvo, a natureza e concentração dos catalisadores, a natureza do gás inerte no interior do tubo e a temperatura do forno externo ao tubo[20].
Descarga elétrica de arco [20][editar | editar código-fonte]

Essa é uma das técnicas mais utilizadas tanto no estudo de nanotubos de carbono quanto em sua produção em larga escala. Como se pode observar na figura ao lado, o aparato experimental consiste de um reator em cujo interior há um gás inerte. O anodo é formado por grafite dopado com catalisadores, que são metais de transição ou ligas desses metais. Quando o arco é ligado, um plasma composto de uma mistura de vapor de carbono, gás inerte e vapor de catalisadores é formado como consequência da energia transferida para o anodo. Como consequencia, uma parte dos produtos se depositam em torno do catodo, outra parte do produto se deposita acima do catodo e há ainda uma outra parte, na forma de fuligem, que se deposita nas paredes e no fundo do reator. Além disso, sempre há um depósito de nanotubos multi-parede no catodo. Cada um desses produtos possuem uma série de estruturas de carbono, como nanotubos parede única, multi-parede, fulerenos, formas amorfas de carbono, dentre muitas outras, dependendo das condições de síntese. Os principais fatores estudados nesse método são a dispersão dos catalisadores no anodo, a natureza e a concentração dos catalisadores, a natureza do gás plasmogênico, a intensidade da corrente e a distância entre os eletrodos.
Como há muitos parâmetros a serem estudados, é difícil tirar uma conclusão acerca do que influencia obter determinado tipo de produto. Entretanto, observa-se que sempre há formação de nanotubos multi-parede no catodo, mesmo sem a presença de catalisadores. Também é observado que utilizando uma liga formada por Ni/Y, a formação de nanotubos parede única aumenta[26] e que substituindo pó de grafite no anodo por pó de diamante misturado com pó de catalisadores, o resultado é um aumento significativo da formação de nanotubos parede única [27].
Algumas propostas de explicações de como funciona, de fato, a síntese de nanotubos vêm sendo feitas. O fato de nanotubos multi-paredes se formarem mesmo sem nenhum catalisador ser adicionado ao processo não é muito bem entendido ainda, entretanto, acredita-se que espécies compostas por C2 podem ser blocos de construção para nanotubos multi-paredes, mas não para nanotubos parede única [28]. Além disso, também há explicações de como pode ocorrer o processo de catálise para a síntese de nanotubos. Acredita-se que com a alta temperatura a que os alvos de carbono e catalisador são expostos, gotas de catalisador podem ser formadas e um processo semelhante ao mecanismo VLS começa a ocorrer. Uma liga de carbono e metal é formada e começa carbono gasosos, então, quando esse carbono se torna supersaturado na gota, átomos de carbono se deslocam para a superfície da gota e acabam encontrando espécies de carbono que estão no lado de fora, como o corannuleno (do inglês corannulene), que é responsável por dar o aspecto fechado da extremidade dos nanotubos. Então, tanto espécies de carbono que estão no interior da gota[29], quanto que estão no exterior da gota começam a se agregar aos nanotubos que estão crescendo, como no mecanismo VLS, fazendo com que o nanotubo atinja grandes comprimentos[30].
Forno solar[editar | editar código-fonte]
Nessa técnica, um espelho plano direciona raios solares a um outro espelho, côncavo, que, por sua vez, direciona os raios para um reator onde se encontra um alvo de grafite com catalisadores sob atmosfera de gás inerte. A transferência da energia solar para o alvo de grafite faz com que a temperatura no alvo seja de, aproximadamente, 4000K, fazendo com que tanto o carbono quanto os catalisadores sejam vaporizados. esse vapor é arrastado pelo gás inerte enquanto a reação ocorre e os produtos condensam ao entrarem em contato com as paredes do reator. Recentemente foi demonstrado que métodos de síntese baseados em energia solar podem ser um método versátil para a produção de nanotubos parede única e podem ser escalonadas para produzir até 100g/h usando fornos solares existentes[31][20].
Deposição química catalítica em fase de vapor ou catalytic chemical vapor deposition (CCVD)[20][editar | editar código-fonte]
Os métodos de CCVD para a síntese de nanotubos de carbono podem ser divididos em dois: o processo heterogêneo, no qual há uma coexistência de fase gasosa com fases sólidas, como os catalisadores da reação por exemplo e o processo homogêneo no qual há apenas fase gasosa.
- O processo heterogêneo
Nesse processo, partículas de metais de transição são colocadas sob um substrato inerte num reator que contem uma atmosfera de gás, também inerte, e um conjunto de hidrocarbonetos gasosos, como CH4, C2H2, C2H4 E C6H6, é colocado no reator. O reator é esquentado a temperaturas entre 600 e 1000ºC e a seguinte reação ocorre:
- CxHy → xC + y/2H2
Mas, para que essa reação ocorra, dando origem a nanotubos de carbono, é preciso que as partículas metálicas sejam nanopartículas. Dessa forma, a produção de nanopartículas é um ponto chave desse processo de síntese e elas não podem coalescer quando forem transferidas para o substrato, por isso ele precisa ser inerte. Há basicamente duas formas de preparação dos catalisadores: a primeira consiste em impregnar um substrato com uma solução do sal do metal de transição desejado e depois reduzir esse sal para obter as nanopartículas do metal desejado e a segunda, consiste na preparação de uma solução sólida de um óxido do metal catalítico escolhido num substrato inerte e depois o óxido do metal catalítico é reduzido de forma a dar origem às nanopartículas metálicas que vão catalisar o crescimento dos nanotubos. A preparação do catalisador é um dos parâmetros que influencia nas espécies de nanotubos formadas.
- O processo homogêneo
Esse processo ocorre de forma semelhante ao processo heterogêneo, a diferença reside no fato de que só se coloca no reator espécies gasosas, portanto, as nanopartículas que irão catalisar o crescimento dos nanotubos são produzidas durante o processo. O reator consiste de um tubo de quartzo colocado num forno que, por sua vez, será aquecido a temperaturas entre 700 e 1000ºC. É introduzido no reator, como no caso heterogêneo, gases inertes e hidrocarbonetos gasosos, entretanto n~~ao se coloca as nanopartículas em substrato inerte. Ao invés disso, coloca-se no reator composto organo-metálicos, que são gasosos. Então, na primeira zona do reator, esses compostos organo-metálicos são decompostos, gerando as nanopartículas que vão catalisar o crescimento dos nanotubos e, na segunda parte do reator, os hidrocarbonetos são decompostos, com a ajuda dos catalisadores, promovendo o crescimento dos nanotubos de carbono.
Tanto nanotubos de parede única quanto nanotubos multi-parede são obtidos com essa técnica dependendo do quanto de gás de hidrocarbonetos, fonte de carbono para os nanotubos, é colocado no reator. Ainda não é possível produzir nanotubos em escala industrial com essa técnica, mas uma descoberta significante com relação a essa técnica feita por pesquisadores da Rice University, nos Estados Unidos, mostrou que é possível produzir nanotubos de parede única com alta pureza[32].
No caso da técnica de CCVD, tanto no processo homogêneo quanto no heterogêneo, observa-se que o catalisador se encontra na base do nanotubo, porém isso só acontece quando se tem nanopartículas. Se as partículas são grandes, a catálise ocorre no modo "crescimento na ponta", isto é, as partículas vão catalisando a reação e vão sendo movidas "para cima", isto é, vão se distanciando do substrato. Em contrapartida, se as partículas metálicas são pequenas o suficiente, elas interagem com o substrato de forma que elas não se movem, permanecem no substrato, esse é o mecanismo conhecido como "crescimento na base". Portanto, o nanotubo cresce indo para fora do substrato deixando o catalisador preso ao substrato. Observa-se que os nanotubos encontrados possuem nanopartículas junto do substrato[33]. Além disso, o mecanismo de crescimento dos nanotubos se dá de forma semelhante que foi explicado na seção "descarga elétrica de arco". O crescimento ocorre num mecanismo VLS. As condições no reator fazem com que as nanopartículas de metais de transição se tornem gotas e uma liga de carbono e metal começa se formar, visto que a gota vai adsorvendo o carbono dos gases de hidrocarbonetos, até que o carbono se torna supersaturado na gota e a síntese de nanotubos começa a acontecer[34].
Sistemas 2D[editar | editar código-fonte]
As nanoestruturas 2D são representadas principalmente pelos filmes finos. O termo “filmes finos” é usado para descrever camadas com a espessura da ordem de micrômetros ou menores, chegando a poucas camadas atômicas [35]. Dentro da categoria de sistemas 2D podemos destacar o grafeno, que tem que tem ganhado destaque nos últimos anos. >. A deposição de filmes finos tem sido muito estudada ao longo da história e diversas técnicas foram aprimoradas e documentadas. Uma das classificações utilizadas para separar os processos de síntese separam as técnicas em: crescimento-líquido(solução), como as monocamadas de auto-montagem(Self-assembly monolayers) e deposição em fase vapor [2]. Essa última categoria pode ser dividas em dois grupos:
- Deposições físicas(PVD) : ocorrem a partir da vaporização de uma fonte(sólida ou líquida) contendo átomos ou moléculas do material desejado. Entre essas técnicas estão a evaporação, MBE(molecular beam epitaxy) e sputtering.
- Deposições químicas: são processos que ocorrem através de reações químicas, como por exemplo a técnica de CVD (e suas variações) e Atomic Layer Deposition (ALD)
Foram realizados diversos trabalhos e pesquisas que mostram a eficiência dos métodos acima para a obtenção de filmes com espessura menor que 100 nanômetros, entretanto, cada uma deles apresenta suas vantagens e limitações em aspectos como o controle da espessura do filme, a lisura das superfícies e a taxa de crescimento dos filmes.[35]
Abaixo são descritas algumas técnicas de síntese de sistemas 2D:
PVD por evaporação[editar | editar código-fonte]
É o processo no qual uma fonte contendo o material desejado sofre vaporização térmica e suas moléculas atingem o substrato em que será formado o filme com poucas ou nenhuma colisão com moléculas de gas no espaço entre os dois. A pureza do filme obtido é assegurada pelo ambiente a vácuo em que o processo é realizado, que reduz a contaminação por outros gases. A técnica é geralmente acontece em baixas pressões(10 -5 a 10-9 Torr) e a taxa de vaporização térmica é alta comparada a outros métodos de vaporização [36]. Na maioria dos casos a evaporação é feita usando fontes termicamente aquecidas(como fios de tungstênio) ou através de feixes se laser e o substrato é mantido há uma certa distância da fonte para não ser afetado pelo aquecimento.
As principais vantagens dessa técnica são as altas(e fáceis de monitorar) taxas de deposiçao, a facilidade de obter filmes com um alto grau de pureza e o baixo custo em relação as demais técnicas de PVD [35]. É usada para obter filmes para diversos tipos de revestimento e proteção de materiais.
PVD por pulverização (Sputter)[editar | editar código-fonte]
É uma técnica na qual os átomos são ejetados da fonte por um bombardeamento de partículas de alta energia(que geralmente são íons gasosos provenientes de um plasma), para que então esses átomos se condensem na superfície do substrato na forma de um filme fino. Embora diversas variações dessa técnica tenham sido desenvolvidas o processo é basicamente o mesmo, e pode ser descrito resumidamente nas seguintes etapas:
- Primeiramente ocorre o bombardeamento do material alvo com os íons. Ele pode ocorrer através da utilização de uma “pistola” de íons ou por plasma de baixa pressão. Também pode ser utilizado um plasma de alta pressão, porem nesse caso existe a colisão das partículas com moléculas gasosas no espaço entre o alvo e o substrato [36].
- A colisão dos íons bombardeados com a superfície alvo causa a ejeção de átomos do material, devido a transferência de momento entre as partículas.
- Esses átomos são transportados através de uma região de baixa pressão até o substrato. Geralmente a distância entre a fonte e o substrato é pequena comparada ao processo de PVD por evaporação.
- Os átomos então condensam sobre o substrato, formando um filme fino.

Algumas vantagens dessa técnica são: a possível utilização em qualquer tipo de material, incluindo aqueles com altos pontos de fusão; os filmes feitos por essa técnica geralmente possuem uma melhor adesão ao substrato; o procedimento é facilmente reproduzido, entre outras. Em contrapartida, esse método possui baixas taxas de deposição e custos elevados.
É uma das técnicas mais usadas na fabricação de filmes metálicos, materiais semicondutores e filmes magnéticos.
Deposição química em fase vapor(CVD) e a produção de grafeno[editar | editar código-fonte]
A técnica de síntese[editar | editar código-fonte]
A deposição química em fase vapor é uma técnica que permite a obtenção de filmes finos através da deposição de vapor químico sobre a superfície de diferentes tipos de substratos. Esse processo pode ocorrer por meio de diversas fontes de energia e a diferentes pressões. A ativação das reações químicas que ocorrem nessa técnica pode ser realizada de forma térmica (TCVD), cuja temperatura gira em torno de 900°C, ativação via plasma([[en:PECVD), que acontece em temperatura de 300-500°c, ativação foto-assistida,entre outras. Após os gases entram em contato com a superfície do substrato acontecem as reações de deposição em sua superfície, com crescimento de sítios ou ilhas de átomos após a nucleação, levando a formação de um filme.
O Grafeno[editar | editar código-fonte]
Grafeno é uma monocamada plana de átomos de carbono empacotados em uma estrutura bidimensional na forma hexagonal. É um bloco de construção para materiais de outras dimensões: ele pode ser embrulhado em fulerenos 0D, enrolados em nanotubos 1D ou empilhados em grafite 3D [37]. Os átomos ligados entre si com hibridização do tipo sp2 e formam uma estrutura cristalina. A estrutura do grafeno do ponto de vista químico também pode ser considerada como uma estrutura dos compostos aromáticos, mais propriamente dos hidrocarbonetos aromáticos policíclicos. O grafeno possuiu propriedades particulares que vem despertando o interesse dos pesquisadores e das industrias, especialmente na área de circuitos e dispositivos eletrônicos.
Utilização de CVD na síntese de Grafeno[editar | editar código-fonte]
A precipitação do grafeno em metais tem sido reportada por diferentes grupos de pesquisa por mais de 30 anos.Recentemente, o método de CVD tem sido usado para obter amostras de grafeno para o estudo de suas propriedades.
O crescimento de grafeno por CVD pode ser dividido em duas etapas: pirólise dos precursores até obtenção do carbono e formação da estrutura grafítica através dos átomos de carbono previamente dissociados. A equação da reação pode ser escrita como:
CH4(g)→ C(s) + 2H2(g)
Pesquisas mostram a síntese de grafeno sendo feita através de variações do método de CVD, com a utilização de substratos de diferentes materiais. Um estudo registrou o crescimento de grafeno em filmes de Níquel, através do processo de CDV realizado em pressão atmosférica(APCVD). Nesse processo foram obtidas folhas de grafeno com grande área. Através do uso de CH4 pirolisado a 1000C. [38] Outro estudo reportou a produção de fitas de grafeno usando ZnS como substrato e com a decomposição do gás metano a 750C[39]. Após a deposição do filme foram realizados tratamentos com ácido para dissolver o ZnS. O resultado desse processo foi a obtenção de fitas de aproximadamente 3 nm de espessura.
Algumas vantagens da utilização desse método para a síntese de grafeno são a alta qualidade dos filmes formados, alta taxa de deposição e um fácil controle da estequiometria da reação, alem da possibilidade de produção de amostras com áreas maiores.
Outros métodos de síntese de grafeno[editar | editar código-fonte]
Esfoliação Micromecância[editar | editar código-fonte]
O Prêmio Nobel de Física de 2010 foi atribuído a Andre Geim e Konstantin Novoselov, da Universidade de Manchester por “experiências inovadoras sobre o grafeno material bidimensional". [40]
A técnica usada por Geim e Novoselov (também chamada de "método da fita adesiva") é designada como esfoliação e baseia-se no arrancar micromecânico de finas camadas de grafite com a ajuda de fita adesiva e à repetição sucessiva da manobra nas amostras obtidas. Os flocos transparentes obtidos são depois dissolvidos em acetona e sedimentados sobre um molde de silício onde podem ser identificadas as amostras de camada única.
A esfoliação micromecânica é considerado o melhor método em termos de qualidade elétrica e estrutural do grafeno obtido, principalmente porque se beneficia da alta qualidade da fonte única e cristalina de grafite tomada como partida.Além disso, é uma técnica de baixo custo que não requer nenhum equipamento especial. No entanto, é desafiador trazer esta abordagem para uma grande escala do nível de produção, por isso que outras estratégias têm atraído novos interesses.
Crescimento Epitaxial[editar | editar código-fonte]
É conhecido desde os início de 1970 que o grafeno poderia ser cultivado diretamente em substratos sólidos e dois mecanismos diferentes podem ser exploradas: a decomposição térmica dos carbonetos ou o crescimento epitaxial de grafeno em metal ou de carbonetos metálicos substratos por deposição química de vapor de hidrocarbonetos.
O tratamento térmico de carboneto de silício em torno de 1300 ° C, sob vácuo, resulta na sublimação dos átomos de silício, enquanto a superfície rica em carbono sofre uma reorganização e, em temperaturas suficientemente elevadas, pode ocorrer grafitização. As dimensões do filme obtido dependem do tamanho do sbstrato.O controle cuidadoso da sublimação levou a recente formação de revestimentos de grafeno muito finos sobre toda a superfície das placas de SiC, as vezes com apenas uma camada de grafeno.[41] [42] Este método de crescimento levanta muitas esperanças que o grafeno poderia ser mais facilmente incorporado a crescente demanda da indústria eletrônica.
O método de crescimento epitaxial de grafeno em metais usa como fonte a estrutura atómica de um substrato de metal para semear o crescimento do grafeno (crescimento epitaxial). Folhas de grafeno cultivadas em rutênio normalmente não produzem uma amostra com uma espessura uniforme de camadas, e as propriedades do produto podem ser afetadas pela ligação entre a camada de fundo grafeno e do substrato[43]. Por outro lado, o grafeno cultivado em irídio é muito fracamente ligado, uniforme em espessura, e pode ser feito de forma ordenada. Como em muitos outros substratos, o grafeno formado em irídio é um pouco ondulado. As folhas obtidas foram transferidos com sucesso a vários substratos, o que demonstra a viabilidade dessa técnica para numerosas aplicações electrónicas. Em comparação a técnica de esfoliação micromecânica , o método de crescimento epitaxial forma filmes mais uniformes e de maior área.
Obtenção de grafeno a partir de nanotubos[editar | editar código-fonte]
Nanotubos de carbono podem ser descritos como folhas de grafeno enroladas, logo o processo inverso consiste em “desenrola-los” para obter grafeno. Os estudos sobre essa técnica são recentes, porém em poucos anos foram descorbestas diversas técnicas para desenrolar ou cortar(“unzip”) os nanotubos. Algumas dessas técnicas consistem em:
- Esfoliação de nanotubos de carbono de paredes múltiplas, envolvendo tratamentos em NH3 líquido e Li, seguido de esfoliação utilizando HCl e tratamentos com calor [44]
- Uma rota química envolvendo reações ácidas que começam a romper ligações carbono-carbono (por exemplo, H2SO4 e KMnO4 como agentes oxidantes) [45]
- Abordagem catalítica, em que nanopartículas metálicas “cortam” o nanotubo longitudinalmente como um par de tesouras [46]
- O método elétrico, pela passagem de uma corrente elétrica através de um nanotubo [47]
- O método físico-químico incorporando os tubos numa matriz de polímero, seguido por tratamento com plasma de Argônio [48]
As estruturas resultantes são nanofitas ou nanofolhas de grafeno
A maioria dos métodos mencionados acima podem produzir nanofitas bem definidas e relativamente cristalinas, desde que o material de partida seja cristalino e uniforme, em comprimento, diâmetro e número de camadas. Para algumas aplicações em que uniformidade borda não é necessária, a produção de maiores quantidades pode ser mais relevante. O método de corte catalítico é escalável, em princípio, se o controle da deposição de grande quantidade de nanopartículas sobre os nanotubos for conseguida.Os métodos químicos oferecem a possibilidade de controlar os comprimentos e larguras das nanofitas resultantes. No entanto, os desafios permanecem em controlar os processos de abertura de nanotubos, se este ocorre por esfoliação, redução ou oxidação. Além dos desafios de controlar a abertura de nanotubos de paredes múltiplas um processo escalonável teria de fornecer as condições que impedem a aglomeração, enrugamento e entrelaçamento das nanofitas produzidas, efeitos que ocorrem devido as forças de van der Waals.
Sistemas Porosos[editar | editar código-fonte]
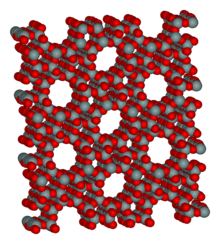
Peneiras moleculares são macromoléculas com cavidades internas de geometria e tamanho definidos cujo diâmetro pode variar da ordem de alguns angstrons até uma centena de nanômetros e podem ser encontradas na natureza como zeólitas naturais ou em membranas celulares, cuja seletividade é essencial para homeostase de organismos vivos.[49] [50].A topologia dos poros é definida pela geometria das ligações entre as moléculas que são usadas como matéria-prima deste material e como estas se arranjam no espaço. Tais peneiras têm grande aplicações em áreas como a nanotecnologia, química supramolecular, indústria petroquímica, catálise heterogênea etc. Podem ser usadas como blocos de construção de dispositivos moleculares ou catalisadores altamente seletivos, devido ao diâmetro e características físico-químicas de seus poros (selecionando substratos pelo seus diâmetro molecular, forma geométrica, carga elétrica, acidez, estado de oxidação, polaridade, etc) e à grande área de superfície por massa que aumenta a sua capacidade de adsorção e reatividade. [18]

A ação seletiva das peneiras moleculares pode atuar tanto nos reagentes, produtos ou no estado de transição, tornando-as catalisadores específicos comparáveis à enzimas biológicas. O diâmetro dos poros é tal que substratos podem difundir em seu interior. Podem ter composição tanto inorgânica (ex: Zeólitas), quanto orgânicas (ex : COFs - do inglês: "Covalent Organic Frameworks"- e MOFs - "Metal-Organic Frameworks" ). As peneiras moleculares são classificadas em microporosas (poros com menos de 2 nm de diâmetro), mesoporososas (entre 2 e 50 nm) ou macroporosas (mais de 50 nm). Seus poros podem ser modificados quimicamente em razão da aplicação de interesse, como por exemplo, poros com grupamentos polares para armazenar moléculas polares.[51]Também pode-se sintetizar materiais nanoporosos flexíveis (parcialmente compostos por cerâmicos e polímeros flexíveis) cuja estabilidade provem de interações intermoleculares(interações não ligadas, como por exemplo: pontes de hidrogênio, interação entre complexos pi, etc)[50]
Zeólitas são moléculas compostas por átomos de silício, alumínio que ligadas à átomos de oxigênio, formam estruturas tetraédricas e em sua maioria são microporosas. Estas estruturas tetraédricas se arranjam no espaço formando poliedros que são estruturas básicas da formação de zeólitas. Geralmente são produzidas por síntese hidrotermal. Zeólitas naturais são formadas em anos sob condições de alta pressão e temperatura e estabilização de seus poros por água e podem ser utilizados na purificação do ar (alta capacidade de adsorção) e no craqueamento de cadeias carbônicas, substituindo catalisadores petroquímicos.[49]
COFs e MOFs são estruturas tridimensionais cristalinas, onde suas topologias são determinadas pela coordenação de átomos metálicos (MOFs) ou pelo direcionamento de ligações covalentes (COFs). Estes tipos de peneiras apresentam grande vantagem devido ao fato de serem compostos por moléculas orgânicas, cuja síntese é bem conhecida, assim aumentando o número de possíveis estruturas com diferentes topologias e funcionalidades.[52]
Dispositivos de 2ª Geração[editar | editar código-fonte]
Dispositivos de Segunda Geração consistem em nanomateriais formados a partir de blocos de construção menores, usando métodos de automontagem para a formação de estruturas altamente ordenadas bi ou tridimensionais em nanoescala.
A ideia de criar nanomateriais átomo por átomo foi popularizada por K. Eric Drexler em meados da década de 1980, que previu a construção de 'nanorobôs', que teriam a capacidade de construir cópias deles mesmos e construir outros componentes, cada átomo por vez. Atualmente, sabe-se que moléculas são blocos de construção mais convenientes que átomos, e sua união por interações supramoleculares possuem um bom potencial para a formação de arquiteturas em nanoescala. Moléculas, tanto naturais quanto sinteticamente preparadas possuem formas características e podem já ter propriedades particulares, além de terem a capacidade se automontar para formar estruturas maiores.[1]
Automontagem (Self-Assembly)[editar | editar código-fonte]

Automontagem é a associação espontânea de duas ou mais moléculas de modo a criar uma estrutura supramolecular formada por ligações não covalentes reversíveis (por exemplo ligações de hidrogênio, coordenação metálica, efeito hidrofóbico, forças de van der Waals, interações π-π, e/ou eletrostáticas). Moléculas relativamente simples com funcionalidades complementares podem, sob certas condições, interagir uma com a outra para formar um complexo supramolecular, como por exemplo a formação da dupla hélice de DNA que requer a complementaridade entre duas fitas por ligação de hidrogênio e por empilhamento pi, onde uma fita reconhece a outra e se juntam para formar o produto termodinamicamente mais estável.[53]
Automontagem sintética depende da habilidade de desenhar moléculas contendo funcionalidades complementares, onde não há controle direto do processo de montagem, com o sistema se auto arranjando no produto termodinamicamente mais estável. O processo de montagem é cineticamente rápido e completamente reversível, o que gera a importante característica de corrigir erros durante a montagem. Quando várias moléculas são capazes de se unir, haverá mais de uma combinação possível, mas o produto mais termodinamicamente estável será predominante.[1]
Síntese Direcionada por Moldes[editar | editar código-fonte]
Reconhecimento molecular e automontagem podem ser usados com com espécies reativas de modo a pré-organizar o sistema para uma reação química (para formar ligações covalentes). Ligações não covalentes entre os reagentes e o molde mantém os sítios reativos próximos e na posição correta, facilitando a química desejada. Essa técnica é particularmente útil para situações onde a conformação necessária para a reação é termodinâmica ou cineticamente desfavorável, como na formação de grandes macrociclos. Essa pré-organização ainda é útil para minimizar reações paralelas, diminuir a energia de ativação da reação, e garantir uma estereoquímica desejada. O molde pode ser desde um simples íon metálico até uma molécula extremamente complexa.[54]

Arquiteturas Moleculares Intercaladas Mecanicamente[editar | editar código-fonte]
Interconexão mecânica de moléculas acontece quando duas ou mais espécies se conectam não por ligações químicas, mas quando estão enroscadas uma na outra, formando uma única entidade, com uma ligação topológica.
Rotaxanos[editar | editar código-fonte]


Rotaxano consiste em uma molécula linear que está envolvida por um anel com suas extremidades tampadas por grupos volumosos de modo a impedir a saída do anel. Pseudorotaxanos são rotaxanos que não possuem grupos terminais, permitindo a desassociação do anel.
Síntese de rotaxanos pode ser feita usando pseudorotaxanos como percursores: anel é atraído pelo eixo por interações intermoleculares, com posterior adição química dos grupamentos volumosos nas extremidades. Se o fio for sintetizado de forma que uma das extremidades já está bloqueada, há estatisticamente muito menos chance do anel sair antes da adição na outra extremidade, favorecendo a cineticamente a reação. Outra forma de síntese é a partir do eixo já completo com grupos volumosos terminais, e uma molécula linear ser introduzida se enrolando no eixo por coordenação, se automontando em uma estrutura circular, com posterior reação química entre suas extremidades, fechando o anel.[1]
Catenanos[editar | editar código-fonte]
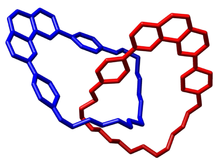
São moléculas cíclicas em que os anéis estão intercalados formando uma ligação topológica somente separável pela quebra de pelo menos uma ligação covalente.
A primeira forma de síntese orgânica de catenanos foi simplesmente a realização de reações de fechamento de anel em uma solução que já continha macrociclos. Essa abordagem estatística levou a primeira formação de um catenano, porém possui alta ineficiêcia, requerendo um alto excesso de anéis pré-formados. Uma segunda forma utiliza pré-organização supramolecular dos percursores de macrociclos utilizando interações não covalentes, que ajudam a posicionar os componentes na forma do catenano desejado. Essa abordagem direcionada associada com condições de alta pressão podem prover rendimentos de mais de 90%.
Uma propriedade interessante de muitos catenanos é a habilidade dos seus anéis girarem um em relação ao outro. Quando exitem regiões de reconhecimento molecular no catenano, podem haver um ou mais posições termodinamicamente preferíveis de um anel em relação ao outro. Quando a preferência entre um sítio ou outro pode ser cotrolado por um fator externo, formamos interruptores moleculares.[1]
Outros Tipos[editar | editar código-fonte]
-
Nó Molecular
-
Olimpidano
-
Modelo Esquemático de um Anel de Borromeu Molecular
-
Cristalografia de um Anel de Boromeu Molecular
Blocos de Construção Moleculares[editar | editar código-fonte]

Há uma grande variedade de blocos de construção com estruturas e funções bem estudadas que são usados para formação de grandes arquiteturas funcionais. Muitos deles existem como uma família de unidades similares, onde aquele com a geometria e funcionalidade específica para a nanoestrutura desejada podem ser escolhidos.[55]
Unidades de Reconhecimento[editar | editar código-fonte]
- Uso de éteres coroa se ligando a um metal ou um cátion amônio é de uso comum em química supramolecular.
- Formação de dímeros de ácidos carboxílicos e outras estruturas com ligações de hidrogênio simples.
- Complexação de bi ou tripiridinas com íons metálicos é de grande utilidade na construção de arquiteturas complexas de muitas moléculas individuais.
- A complexação de porfirinas ou ftalocianinas com íons metálicos levam a formação de propriedades catalíticas, fotoquímicas e eletroquímicas. Essas unidades são amplamente usadas pela natureza.
Macrociclos[editar | editar código-fonte]
Macrociclos são muito úteis em química supramolecular, pois provém cavidades que podem ser completamente preenchidas por moléculas hospedeiras, e podem ser quimicamente modificadas para aperfeiçoamento das suas propriedades.
- Ciclodextrinas, calixarenos e éteres coroa já são sintetizadas em grandes quantidades, logo, são muito convenientes.
- Metalociclos supramoleculares são agregados de macrociclos com íons metálicos no anel, usando ligantes lineares ou angulares. Tipos comuns incluem triângulos, quadrados e pentágonos que se conectam por automontagem.

Unidades Estruturais[editar | editar código-fonte]
Muitos sistemas supramoleculares requerem que seus componentes tenham espaçamentos e conformações específicos, logo precisam utilizar unidades estruturais simples.
- Grupos espaçadores e conectores geralmente usados incluem cadeias de poliéter, bi e trifenis e cadeias de alquila.
- Nanopartículas, fulerenos e dendrímeros oferem estruturas nanométricas e unidades de encapsulamento.
Unidades foto e eletroquimicamente ativas[editar | editar código-fonte]
- Porfirinas e Ftalocianinas possuem atividades fotoquímicas e eltroquímicas características, assim como possuem potencial de formação de complexos.
- Grupos fotocrômicos e fotoisomeráveis possuem a habilidade de mudar suas formas e propriedades (inclusive as de ligação) sob exposição a luz.
- TTF e quinonas possuem mais de um estado de oxidação estável, e podem sofrer modificações com reações de oxirredução ou eletroquímica.
Unidades Biológicas[editar | editar código-fonte]
- A ligação de enzimas com seus cofatores tem sido usado como uma roda de produzir enzimas modificadas quimicamente, eletroquimicamente e até mesmo fotoquimicamente.
- DNA tem sido usado tanto como unidade estrutural como funcional em sistemas supramoleculares sintéticos.
Aplicações[editar | editar código-fonte]
Interruptores Moleculares[editar | editar código-fonte]

Interruptores moleculares são estruturas que podem alternar entre dois ou mais estados estáveis em resposta a um estímulo ambiental, como mudança do pH, luz, temperatura, corrente elétrica, microambiente, ou na presença de um ligante.[56] Os interruptores moleculares mais avançados são aqueles baseados em arquiteturas moleculares mecanicamente interligados, onde os estados estáveis diferem na posição do macrociclo.
Em 1993, Fritz Vögtle sintetizou um interruptor baseado em um catenano. O composto era baseado em dois anéis: um que carrega duas estações paraquat além de um azobenzeno, que altera sua configuração (cis, trans) fotoquimicamente, e outro anel que é um poliéter com afinidade intermolecular pelas estações paraquat. Espectrocopia de RMN demonstrou que quando o grupamento azo está na conformação trans, o anel poliéter possui liberdade de rotação ao redor do outro anel. Mas quando um estímulo luminoso ativa a forma cis, essa rotação é interrompida. [57]
Portas Lógicas Moleculares[editar | editar código-fonte]

Ver artigo principal: Eletrônica Molecular
São estruturas que realizam operações lógicas baseadas em um ou mais estímulos de entrada. Normalmente respondem espectrocopicamente a um estímulo devido a um processo químico.
Por exemplo, uma porta lógica XOR molecular é feita a partir de um pseudorotaxano: um sal de diazopireno (eixo linear) elétron-deficiente com um macrociclo éter coroa com unidades 2,3-dioxinaftaleno ricas em elétrons que se associam espontaneamente em um complexo de transferência de carga. Ao adicionar uma amina terciária, como tributilamina, forma um aduto com o diazopireno e o complexo é desmontado. Esse processo é acompanhado num aumento da intensidade de emissão a 343 nm por causa do éter coroa livre. Adicionando Ácido tríflico, ele reage com a amina, e o complexo é reformado (diminuição da intensidade a 343 nm). O ácido excedente protona o éter coroa, e o complexo é desmontado novamente. [58]
| Amina Terciária | Ácido tríflico | Pseudorotaxano | Intensidade a 343nm | Causa |
|---|---|---|---|---|
| Não (0) | Não (0) | Montado | Baixa (0) | Estrutura formada. |
| Não (0) | Sim (1) | Desmontado | Alta (1) | Éter é protonado. |
| Sim (1) | Não (0) | Desmontado | Alta (1) | Diazopireno é sequestrado. |
| Sim (1) | Sim (1) | Montado | Baixa (0) | Estrutura formada. |
Motores Moleculares Sintéticos[editar | editar código-fonte]

Inspirados por proteínas que ocorrem naturalmente, como cinesina e dineína, a ideia de síntese de motores moleculares sintéticos foi primeiramente levantada por Richard Feynman em 1954 na sua palestra There's Plenty of Room at the Bottom. Os requisitos básicos para um motor sintético são: movimento repetitivo de 360 graus, consumo de energia, e rotação unidirecional.
O primeiro exemplo de motor molecular com rotação dirigida quimicamente foi reportado por Kelly et al em 1999.[59] O sistema era formado com um rotor de três hélices, tripticeno, ligado a um heliceno de sustentação, e tinha capacidade de fazer rotações unidirecionais de até 120 graus. A rotação acontece em cinco etapas: O grupo amina do tripticeno é convertido a isocianato por condensação com fosfogênio(a). Rotação térmica ou espontânea ao redor da ligação central leva o isocianato próximo a hidroxila do heliceno, permitindo sua reação (c). Essa reação trava o sistema irreversivelmente sob a forma de um uretano cíclico. Mais rotação do tripticeno requer apenas uma pequena ativação térmica para superar a barreira energética, e assim aliviando a tensão de anel (d). Finalmente, a cisão do grupamento uretano recupera a molécula.(e)
Dispositivos de 3ª Geração[editar | editar código-fonte]
Os dispositivos de terceira geração são complexos que envolvem dispositivos de segunda geração, mas também podem conter blocos básicos de construção. Eles têm grande importância no campo da nanotecnologia, pois eles estão diretamente relacionados a diversas aplicações da nanotecnologia em campos da física (como, por exemplo, na construção de diodos e transistores[60]), biologia (na produção de biosensores[61]), química (fabricação de estruturas moleculares funcionais[62]) e entre outros.
Dos elementos utilizados para a manufatura destes dispositivos, destaca-se o carbono[63] devido suas propriedades elétricas, mecânicas e ópticas únicas. Mas, a utilização de outros elementos também é comum e importante[64].
Os métodos de produção destes dispositivos variam muito, metodologias como a utilização de técnicas de litografia[65] ou manipulações feitas através de microscópios de força atômica[66] são muito utilizadas, mas não são as únicas.
Abaixo seguem exemplos de dispositivos de terceira geração.
Fabricação de Nanocircuitos[editar | editar código-fonte]
Este exemplo de dispositivo de terceira geração tem notável importância, pois trata-se de uma possível evolução no campo da eletrônica e na diminuição da escala dos componentes eletrônicos. A fabricação deste tipo de circuito pode ser feita com diversas estratégia, sendo uma delas o método nTP (do inglês, nanotransfer-printing,litografia de impressão por nanotransferência). Esse método se baseia na deposição dos nanofios sobre um filme, a deposição é feita por um molde que é construído por litografia de nanoimpressão (NIL, na sigla em inglês) onde o metal, que será usado para a construção dos fios, é depositado. Com o molde revestido pelo metal, ele é encostado sob a superfície do filme e são aplicados calor e radiação ultravioleta para que os fios se aderam a superfície do filme. Assim acabado os nanofios do circuito são fabricados, mas, pode-se também fazer disposições de circuitos tridimensionais, onde após depositados os nanofios se insere uma camada de um polímero específico formando assim um novo filme onde pode ser colocados mais fios. A vantagem deste tipo de técnica é sua simplicidade, a preservação das funções dos materiais orgânicos e a possibilidade de se construir circuitos em três dimensões, o que pode ajudar na redução de dimensões dos circuitos.[67]
Mas, como já citado anteriormente essa técnica de produção de nanocircuitos é apenas uma das diversas outras existentes. Por exemplo, existem técnicas de produção de nanocircuitos utilizando moléculas de DNA, proteínas e nanopartículas[68]. Sendo assim, o número de técnicas e procedimentos para a fabricação destes tipos de dispositivos é bem ampla.

Nanoestruturas com DNA[editar | editar código-fonte]
Nanoestruturas também podem ser feitas por meio da manipulação e modificação de moléculas de DNA. E as técnicas para se fazer essas estruturas podem ser simples, baseando-se na natureza do DNA de se ligar a suas bases complementares e na sua estrutura química. Por exemplo, "tesouras" de DNA podem ser feitas apenas pela a adição de oligonucleotídios num meio apropriado [69] e nanofios de DNA podem ser sintetizados pela associação do DNA com agregados de moléculas de prata[70]. Além dessas estruturas, podem ser fabricados com DNA dispositivos como semicondutores [71], cristais e entre outros.
Máquinas moleculares com ciclodextrina[editar | editar código-fonte]
Ciclodextrinas são moléculas cíclicas compostas por moléculas de glicose. Elas são utilizadas para a produção de estruturas complexas como rotaxanos e catenanos[72]. Rotaxanos são típicas estruturas para a produção de máquinas moleculares como rotores. Eles se baseiam na associação da ciclodextrina com uma outra molécula alifática que funciona como um eixo. A associação de diversas moléculas de ciclodextrina encaixadas numa molécula alifática pode criar também estruturas conhecidas como polirotaxanos e chamadas de "colares moleculares" (que se assemelham a um colar sendo a "corda" a molécula alifática e as "pérolas" as moléculas de ciclodextrina). Já os catenanos são moléculas de ciclodextrina que estão dentro de uma outra cadeia cíclica, funcionando assim como "trens" moleculares (sendo o "trem" a ciclodextrina e os "trilhos" a molécula cíclica onde a ciclodextrina está inserida). A síntese dessas moléculas pode ser feita de diversas formas, dependendo da formulação química das estruturas associadas a ciclodextrina, e podem ser realizadas tanto por métodos químicos como físicos (como radiação ou calor).
Ver também[editar | editar código-fonte]
Referências
- ↑ a b c d e Steed, J. W., Turner, D. R., Wallace, K. J. Core Concepts in Supramolecular nanochemistry, John Wiley & Sons (2007).
- ↑ a b c d e f g h i j k l m n o p Guozhong Cao Nanostructures and Nanomaterials: Synthesis, Properties, and Applications, ed. Imperial College Press (2004).
- ↑ a b http://www.nanobiotec.iqm.unicamp.br/download/preparation%20nanoparticles-chapter%205.pdf.
- ↑ a b Manoj Singh, S. Manikandan and A.K. Kumaraguru (2010. Nanoparticles: A New Technology with Wide Applications. Research Journal of Nanoscience and Nanotehcnology. p.4. ISSN 1996-5044. doi:10.3923/rjnn.2010.
- ↑ Vicent M. Rotello Nanoparticles: Building Blocks for Nanotechnology, ed. Springer (2004).
- ↑ Wei-Hong Zhong Nanoscience and Nanomaterials: Synthesis, Manufacturing and Industry Impacts, ed. DEStech Publications, Inc, 2012.
- ↑ Christina Raab, Myrtill Simkó,Ulrich Fiedeler, Michael Nentwich, André Gazsó. Production of nanoparticles and nanomaterials. Institute of Technology Assessment of the Austrian Academy of Sciences. Nanotrust Dossiers No. 006en • February 2011.
- ↑ Authors: Salah N, Habib SS, Khan ZH, Memic A, Azam A, Alarfaj E, Zahed N, Al-Hamedi S High-energy ball milling technique for ZnO nanoparticles as antibacterial material. |April 2011|Volume 2011:6|Pages 863 - 869|DOI: http://dx.doi.org/10.2147/IJN.S18267.
- ↑ Jitendra Behari. Principles of nanoscience: an overview. Indian Journal of Experimental Biology. Vol. 48, October 2010, pp.1008-1019.
- ↑ Prathna T.C., Lazar Mathew, N. Chandrasekaran, Ashok M. Raichur and Amitava Mukherjee (2010). Biomimetic Synthesis of Nanoparticles: Science, Technology & Applicability, Biomimetics Learning from Nature, Amitava Mukherjee (Ed.), ISBN: 978-953-307-025-4, InTech, Available from: http://www.intechopen.com/books/biomimetics-learning-from-nature/biomimetic-synthesis-of-nanoparticlesscience-technology-amp-applicability
- ↑ Sujoy K. Das and Enrico Marsili (2011). Bioinspired Metal Nanoparticle: Synthesis, Properties and Application, Nanomaterials, Prof. Mohammed Rahman (Ed.), ISBN: 978-953-307-913-4, InTech, Available from: http://www.intechopen.com/books/nanomaterials/bioinspired-metal-nanoparticle-synthesis-properties-andapplication
- ↑ " Storex Disclosed Quantum Optical Lithography Technique", Press Release, Storage Newsletter.com , February 24th, 2012
- ↑ a b c d J,W, Mullin " Crystallization - Fourth Edition", ed. Butterworth-Heinemann, 2001
- ↑ F. F. Abraham (1974) Homogeneous nucleation theory (Academic Press, NY)[Google Books|http://books.google.com/books?id=uftWE2eAH10C&lpg=PA76&dq=homogeneous%20nucleation&pg=PA78#v=onepage&q=homogeneous%20nucleation&f=false]
- ↑ William D. Callister, Jr., David G. Rethwisch " Materials Science and Engineering An Introduction - Eight Edition", ed. Wiley
- ↑ a b R.Overney Nanothermodynamics and Nanoparticle Synthesis,http://courses.washington.edu/overney/NME498_Material/NME498_Lectures/Lecture%20on%20Thermo%20and%20Nanoparticles%20v5.pdf.
- ↑ Jimmy C. Yu Nanoparticle Synthesis
- ↑ a b c d e Geoffrey A. Ozin, André C. Arsenault, Ludovico Cademartiri Nanochemistry : A chemical approach to nanomaterials, 2nd ed. RSC Publishing ISBN: 9780854046645.
- ↑ C.J. Murphy, N.R. Jana, Controlling the Aspect Ratio of Inorganic Nanorods and Nanowires, Advanced Materials, 2002, 14, 1.
- ↑ a b c d e f g B. Bhushan, Springer Handbook of nanotechnology, Bharat Bhushan ed. Springer-Verlag ISBN: 3-540-01218-4.
- ↑ J. P. O'Sullivan, G.C. Wood, The Morphology and Mecanism of Formation of Porous Anodic Films on Aluminium, Proc. Roy. Soc. London A, 1970, 317, 511-543.
- ↑ O. Jessenky, F. Müller, U.H. Gösele, Self Organized Formation of Hexagonal Pore arrays in Anodic Alumina, Appl. Phys. Lett., 1998, 72, 1173-1175.
- ↑ J. Herenmans, C.M. Thrush, Y.-M. Lin, S. Cronin, Z. Zhang, M.S. Dresselhaus, J.F. Mansfield, Bismuth nanowire Arrays: Synthesis and Galvanomagnetic properties, Phys. Rev. B, 2000, 61, 2921-2930.
- ↑ a b G.-C. Yi, Semiconductor Nanoestructures for Optoeletrônic Devices, G.-C. Yi ed. Springer-Verlag DOI: 10.1007/978-3-642-22480-5 1.
- ↑ A. Thess, R. Lee, P. Nicolaev, H. Dai, P. Petit, J. Robert, C. Xu, Y.H. Lee, S.G. Kim, D.T. Colbert, G. Scuseria, D. Tomanek, J.E. Fischer, R.E. Smalley, Cristalline Ropes of Metallic Carbon Nanotubes, Science, 1996, 73, 487-493.
- ↑ C. Journet, La Production de nanotubes de Carbone, Ph.D thesis, 1998, Universidade de Montpellier II.
- ↑ M. Monthioux, M. Pacheco, H. Allouche, M. Razafinimanana, N. Caprais, L. Donnadieu, A. Gleizes, Newdata about the formation of SWNTs by the electric arc method, Electronic Properties of Molecular Nanostructures, AIP Conf. Proc., Melville 2002, ed. por H. Kuzmany, J. Fink, M.Mehring, S. Roth (Springer, Berlin, Heidelberg 2002) 182–185
- ↑ M. Monthioux, M. Pacheco, H. Allouche, M. Razafinimanana, N. Caprais, L. Donnadieu, A. Gleizes, Newdata about the formation of SWNTs by the electric arc method, Electronic Properties of Molecular Nanostructures, AIP Conf. Proc., Melville 2002, ed. por H. Kuzmany, J. Fink, M.Mehring, S. Roth (Springer, Berlin, Heidelberg 2002) 182–185
- ↑ Y. Saito, M. Okuda, N. Fujimoto, T. Yoshikawa, M. Tomita, T. Hayashi, Single-wall carbon nanotubes growing radially from Ni fine particles formed by arc evaporation, Jpn. J. Appl. Phys.,1994, 33, L526–L529
- ↑ J. Bernholc, C. Brabec, M. Buongiorno Nardelli, A. Malti, C. Roland, B. J. Yakobson, Theory of growth and mechanical properties of nanotubes, Appl. Phys. A, 1998, 67,39–46
- ↑ G. Flamant, D. Luxembourg, C. Mas, D. Laplaze: Carbon nanotubes from solar energy; a chemical engineering approach of the scale up, Proc. Am. Inst. Chem. Eng. Ann. Meeting, Indianapolis 2002, in print
- ↑ R. E. Smalley, J. H. Hafner, D. T. Colbert, K. Smith: Catalytic growth of single-wall carbon nanotubes from metal particles, US patent US19980601010903 (1998)
- ↑ H. Dai, Carbon Nanotubes: Synthesis, integration, and properties, Acc. Chem. Res., 2002, 35, 1035–1044)
- ↑ H. Dai, Carbon Nanotubes: Synthesis, integration, and properties, Acc. Chem. Res., 2002, 35, 1035–1044)
- ↑ a b c Nanotechnology: Volume 8: Nanostructured Surfaces, edited by Lifeng Chi
- ↑ a b Mattox, Donald M. Handbook of Physical Vapor Deposition (PVD) Processing: Film Formation, Adhesion, Surface Preparation and Contamination Control.
- ↑ Geim, A. K. and Novoselov, K. S. (2007). "The rise of graphene". Nature Materials 6 (3): 183–191
- ↑ "A. Reina, S. Thiele, X. Jia, S. Bhaviripudi, M.S. Dresselhaus,J.A. Schaefer, J. Kong, Nano Res. 2 (2010) 509."
- ↑ D. Wei, Y. Liu, H. Zhang, L. Huang, B. Wu, J. Chen, G. Yu, J.Am. Chem. Soc. 131 (2009)
- ↑ "Nobel Foundation announcement"
- ↑ I. Forbeaux, J.M. Themlin, J.M. Debever Heteroepitaxial graphite on 6H–SiC(0001): interface formation through conduction-band electronic structure
- ↑ C. Berger, Z.M. Song, T.B. Li, X.B. Li, A.Y. Ogbazghi, R. Feng et al.Ultrathin epitaxial graphite: 2D electron gas properties and a route toward graphene-based nanoelectronics
- ↑ "A smarter way to grow graphene". PhysOrg.com. May 2008.
- ↑ A.G. Cano-Márquez, F.J. Rodríguez-Macías, J. CamposDelgado, C.G. Espinosa-González, F. Tristán-Loˇıpez, D.Ramírez-González, D.A. Cullen, D.J. Smith, M. Terrones, Y.I.Vega-Cantú, Nano Lett. 9 (2009)
- ↑ D.V. Kosynkin, A.L. Higginbotham, A. Sinitskii, J.R. Lomeda,A. Dimiev, B.K. Price, J.M. Tour, Nature 458 (2009)
- ↑ M. Terrones, Nature 458 (2009
- ↑ K. Kim, A. Sussman, A. Zettl, ACS Nano 4 (2010)
- ↑ ] L. Jiao, L. Zhang, X. Wang, G. Diankov, H. Dai, Nature 458(2009)
- ↑ a b Artur J. Santos Peneiras Moleculares: Selecionando as Moléculas por seu Tamanho, Artur J. Santos Mascarenhas, Erica C. Oliveira e Heloise O. Pastore http://qnesc.sbq.org.br/online/cadernos/02/peneiras.pdf
- ↑ a b Holister, Paul. «Nanoporous Materials» (PDF). Cientifica. Consultado em 6 February 2013 Verifique data em:
|acessodata=(ajuda) - ↑ Dekker Enciclopedia DEKKER Encyclopedia of nanoscience and nanotechnology,2nd ed, chaper 177, ISBN 978‑0‑8493‑9639‑7.
- ↑ James r. Holst, Abbie Trewin and Andrew i. Cooper, Porous organic molecules,Nature Chemistry, vol 2, November 2010,pages 915-920.
- ↑ Goddard, W.; Brenner,D.; Lyshevski, S.; Iafrate, G. Handbook of Nanoscience, Engineering, and Technology (2002),
- ↑ J. M. Lehn, (1990). "Perspectives in supramolecular chemistry - from molecular recognition towards molecular information-processing and self-organization". Angewandte Chemie-International Edition in English 29 (11): 1304–1319. doi:10.1002/anie.199013041
- ↑ Supramolecular Chemistry: From Molecules to Nanomaterials, P.A. Gale and J.W. Steed (Eds), Wiley (2012) ISBN 978-0-470-74640-0
- ↑ Molecular Machines & Motors (Structure and Bonding) J.-P. Sauvage Ed. ISBN 3-540-41382-2
- ↑ Photoswitchable Catenanes Fritz Vögtle, Walter Manfred Müller, Ute Müller, Martin Bauer, Kari Rissanen;1993.
- ↑ Alberto Credi, Vincenzo Balzani, Steven J. Langford, and J. Fraser Stoddart. Logic Operations at the Molecular Level. An XOR Gate Based on a Molecular Machine J. Am. Chem. Soc. 1997,119, 2679-2681.
- ↑ Unidirectional rotary motion in a molecular system T. Ross Kelly, Harshani De Silva and Richard A. Silva Nature 1999, 401, 150-152. doi:10.1038/43639 PMID 10490021
- ↑ S. J. Tans, R. M. Verschueren, C. Dekker, Nature 393, 49 (1998)
- ↑ Chen Jianrong, Miao Yuqing, He Nongyue, Wu Xiaohua, Li Sijiao, Nanotechnology and biosensors, Biotechnology Advances, Volume 22, Issue 7, September 2004, Pages 505–518
- ↑ http://lyle.smu.edu/~mitch/class/8381/papers/raja_nano_tut.pdf
- ↑ A. Vaseashta, J. Irudayaraja, NANOSTRUCTURED AND NANOSCALE DEVICES AND SENSORS,Journal of Optoelectronics and Advanced Materials Vol. 7, No. 1, February 2005, p. 35 - 42
- ↑ D. Golberg, Y. Bando, K. Kurashima and T. Sato, SYNTHESIS AND CHARACTERIZATION OF ROPES MADE OF BN MULTIWALLED NANOTUBES,Scripta mater. 44 (2001) 1561–1565
- ↑ Colin Stuart, Hee-Kun Park, and Yong Chen, Fabrication of a 3D Nanoscale Crossbar Circuit by Nanotransfer-Printing Lithography,small 2010, 6, No. 15, 1663–1668
- ↑ D. Golberg, Y. Bando, K. Kurashima and T. Sato, SYNTHESIS AND CHARACTERIZATION OF ROPES MADE OF BN MULTIWALLED NANOTUBES,Scripta mater. 44 (2001) 1561–1565
- ↑ Colin Stuart, Hee-Kun Park, and Yong Chen ; Fabrication of a 3D Nanoscale Crossbar Circuit by Nanotransfer-Printing Lithography ; small 2010, 6, No. 15, 1663–1668
- ↑ Lifeng Zhenga , James P. Brodyb , Peter J. Burke ; Electronic manipulation of DNA, proteins, and nanoparticles for potential circuit assembly ; Biosensors and Bioelectronics 20 (2004) 606–619
- ↑ Bernard Yurke, Andrew J. Turberfield, Allen P. Mills Jr, Friedrich C. Simmel & Jennifer L. Neumann ; A DNA-fuelled molecular machine made of DNA ; Nature - VOL 406 - 10 AUGUST 2000
- ↑ Braun, E., Eichen, Y., Sivan, U. & Ben-Yoseph, G. DNA-templated assembly and electrode attachment of a conducting silver wire. Nature 391, 775±778 (1998).
- ↑ Coffer, J. L. et al. Dictation of the shape of mesoscale semiconductor nanoparticle assemblies by plasmid DNA. Appl. Phys. Lett. 69, 3851±3853 (1996)
- ↑ AKIRA HARADA ; Cyclodextrin-Based Molecular Machines ; Acc. Chem. Res. 2001, 34, 456-464


















































