Evolução de íons metálicos em sistemas biológicos
A evolução de íons metálicos em sistemas biológicos refere-se à incorporação de íons metálicos em organismos vivos e como isso mudou ao longo do tempo. Os íons metálicos têm sido associados a sistemas biológicos há bilhões de anos, mas apenas no século passado os cientistas começaram a realmente apreciar a escala de sua influência. Íons metálicos maiores (ferro, manganês, magnésio e zinco) e menores (cobre, cobalto, níquel, molibdênio, tungstênio) se alinharam com os organismos vivos por meio da interação do intemperismo biogeoquímico e das vias metabólicas envolvendo os produtos desse intemperismo. Os complexos associados evoluíram com o tempo.[1]
O desenvolvimento natural de produtos químicos e elementos desafiava os organismos a se adaptarem ou morrerem. Os organismos atuais requerem reações redox para induzir o metabolismo e outros processos vitais. Os metais têm tendência a perder elétrons e são importantes para as reações redox.
Os metais se tornaram tão centrais para a função celular que a coleção de proteínas de ligação a metais (conhecidas como metalomas) é responsável por mais de 30% de todas as proteínas da célula. Os metais são conhecidos por estarem envolvidos em mais de 40% das reações enzimáticas, e as proteínas de ligação a metais realizam pelo menos uma etapa em quase todas as vias biológicas. [2]
Os metais também são tóxicos, portanto, um equilíbrio deve ser obtido para regular onde os metais estão em um organismo, bem como em que quantidades. Muitos organismos têm sistemas flexíveis nos quais podem trocar um metal por outro se um for escasso. Os metais nesta discussão são elementos que ocorrem naturalmente e têm tendência a sofrer oxidação. O elementos vanádio, molibdênio, cobalto, cobre, cromo, ferro, manganês, níquel e zinco são considerados essenciais porque sem eles a função biológica é prejudicada.
Origens[editar | editar código-fonte]

A Terra começou como um mundo aquático de ferro com pouco oxigênio. O Grande Evento de Oxigenação ocorreu aproximadamente 2,4 bilhões de anos atrás quando as cianobactérias e a vida fotossintética induziram a presença de dioxigênio na atmosfera do planeta.[1] O ferro se tornou insolúvel (assim como outros metais) e escasso, enquanto outros metais se tornaram solúveis. O enxofre foi um elemento muito importante nessa época. Depois que o oxigênio foi liberado no meio ambiente, os sulfatos dos metais tornaram-nos mais solúveis e os liberaram no meio ambiente; especialmente na água.[2] A incorporação de metais talvez combata o estresse oxidativo.
A química central de todas essas células deve ser redutora para que a síntese dos produtos químicos necessários, especialmente biopolímeros, seja possível. As diferentes vias metabólicas anaeróbicas, autocatalisadas, redutivas e metabólicas vistas nas primeiras células conhecidas desenvolveram-se em vesículas energizadas separadas, protocélulas, onde foram produzidas cooperativamente com certas bases dos ácidos nucléicos.[3]
A hipótese proposta de como os elementos se tornaram essenciais esta relacionada a sua quantidade relativa no ambiente à medida que a vida se formava. Isso produziu pesquisas sobre a origem da vida; por exemplo, Orgel e Crick levantaram a hipótese de que a vida era extraterrestre devido à alegada baixa abundância de molibdênio na Terra primitiva (suspeita-se agora que havia quantidades maiores do que se pensava anteriormente). Outro exemplo é a formação de vida em torno das fontes hidrotermais com base na disponibilidade de zinco e enxofre.[2] Em conjunto com esta hipótese está a teoria de que a vida evoluiu como quimioautotróficos. Portanto, a vida ocorria em torno dos metais e não em resposta à sua presença. Algumas evidências para essa teoria são que a matéria inorgânica possui atributos autocontidos que a vida adotou conforme mostrado pela compartimentalização da vida.[3] Outras evidências incluem a pronta ligação de metais por proteínas artificiais sem história evolutiva.[4]
Importância dos íons metálicos na evolução[editar | editar código-fonte]
Catalisadores redox[editar | editar código-fonte]
A química pré-biótica da vida tinha que ser redutora a fim de obter, por exemplo, monóxido de carbono (CO) e cianeto de hidrogênio (HCN) do CO2 e N2 existentes na atmosfera. CO e HCN foram moléculas precursoras de biomoléculas essenciais, proteínas, lipídios, nucleotídeos e açúcares.[5] No entanto, os níveis de oxigênio atmosférico aumentaram consideravelmente e foi então necessário que as células tivessem controle sobre a redução e oxidação dessas pequenas moléculas para construir e quebrar as células quando necessário, sem a inevitável oxidação (quebra) de tudo. Os íons de metais de transição, devido aos seus múltiplos estados de oxidação, eram os únicos capazes de controlar os estados de oxidação de tais moléculas e, portanto, foram selecionados.[6]
Condensação e hidrólise[editar | editar código-fonte]
Espécies químicas O-doadores omo HPO2−
4 eram abundantes na atmosfera pré-biótica.[7] A ligação de íons metálicos a tais O-doadores foi necessária para construir os polímeros biológicos, uma vez que a ligação é geralmente fraca, ela pode catalisar a reação necessária e dissociar depois (como, Mg2+ na síntese de DNA).
Abundância de metais na água do mar[editar | editar código-fonte]
| Elemento | Condições pré-bióticas (M) [7] | Condições aeróbicas (M) |
|---|---|---|
| Mg2+ | ~ 10−2 | ~ 10−2 |
| Mn2+ | ~ 10−6 | ~ 10−8 |
| Fe | ~ 10−7 [Fe (II)] | ~ 10−19 [Fe (III)] |
| Co2+ | ~ 10−9 | ~ 10−9 |
| Ni2+ | < 10−9 | < 10−9 |
| Cu | < 10−20 (muito baixo) [Cu (I)] | < 10−10 [Cu (II)] |
| Zn2+ | < 10-12 (muito baixo) | ~ 10−8 |
| Mo | ~10 −9 (MoS2− 4, Mo(OH)6) |
10−8 (MoO2− 4) |
| W | WS2− 4 |
10−9 (WO2− 4) |
| H+ | pH baixo (5,5? ) | pH 8,5 |
| H2S | 10−2 (alto) | baixo [SO2− 4(10 −2 )] |
| O2 | <10−6 atm | ~ 10−1 atm (21%) |
Condições pré-bióticas (anaeróbicas)[editar | editar código-fonte]
Por volta de 4 bilhões de anos atrás, a água do mar ácida continha grandes quantidades de H2S e, portanto, criou um ambiente redutor com um potencial em torno de −0,2 V.[7] Portanto, qualquer elemento que tivesse um grande valor negativo em relação ao potencial de redução do ambiente estava disponível em sua forma iônica livre e pôde, posteriormente, ser incorporado às células (como o Mg2+ que possui um potencial de redução de -2,372 V e estava disponível em sua forma iônica na época).
Condições aeróbicas[editar | editar código-fonte]
Por volta de 2 bilhões de anos atrás, ocorreu um aumento nos níveis de oxigênio atmosférico, causando uma oxidação de H2S nas proximidades, e um aumento no pH da água do mar. O ambiente resultante tornou-se mais oxidante e, portanto, permitiu a incorporação posterior de metais mais pesados, como cobre e zinco.[8]
Série Irving – Williams[editar | editar código-fonte]
Outro fator que afetava a disponibilidade de íons metálicos eram suas solubilidades com H2S. O sulfeto de hidrogênio era abundante no início do mar dando origem a H2S nas condições pré-bióticas ácidas e HS− nas condições neutras (pH = 7,0). Na série de sulfetos metálicos, a insolubilidade aumenta em pH neutro seguindo a série Irving – Williams:
- Mn(II) < Fe(II) < Co(II) ≤ Ni(II) < Cu(II) > Zn(II)
Portanto, em grandes quantidades de H2S, que era a condição pré-biótica, apenas o ferro estava mais disponível em sua forma iônica devido à sua baixa insolubilidade com sulfetos. A oxidação crescente de H2S em SO2−
4leva à liberação posterior de Co+2, Ni+2, Cu+2 e Zn+2, uma vez que todos os seus sulfatos são solúveis.
Íons de metal[editar | editar código-fonte]
Magnésio[editar | editar código-fonte]
O magnésio é o oitavo elemento mais abundante da Terra. É o quarto elemento mais abundante em vertebrados e o cátion divalente mais abundante dentro das células. A forma mais disponível de magnésio (Mg2+) para os organismos vivos pode ser encontrada na hidrosfera. A concentração de Mg2+ na água do mar é de cerca de 55 mM. O Mg2+ esteve prontamente disponível para as células durante a evolução inicial devido à sua alta solubilidade em água. Outros metais, como o cálcio, precipitam de soluções aquosas em concentrações muito mais baixas do que os sais de Mg2+ correspondentes.[9]
Como o magnésio estava disponível no início da evolução, ele pode ser encontrado em todos os organismos vivos de tipo celular. O magnésio em procariotos anaeróbicos pode ser encontrado no MgATP. O magnésio também tem muitas funções em procariotos, como glicólise, todas as quinases, reação NTP, sinalização, estruturas de DNA/RNA e captura de luz. Em eucariotos aeróbios, o magnésio pode ser encontrado no citoplasma e nos cloroplastos. As reações nesses compartimentos celulares são glicólise, fotofosforilação e fixação de carbono .
O ATP, a principal fonte de energia em quase todos os organismos vivos, deve se ligar a íons metálicos como Mg2+ ou Ca2+ para funcionar. O exame de células com suprimento limitado de magnésio mostrou que a falta de magnésio pode causar uma diminuição no ATP.[10] O magnésio na hidrólise do ATP atua como um cofator para estabilizar o estado de transição de alta carga negativa.[11] O MgATP pode ser encontrado em células procariotas e eucariotas. No entanto, a maior parte do ATP nas células é MgATP. Seguindo a série Irving – Williams, o magnésio tem uma constante de ligação mais alta do que o Ca2+. Portanto, o ATP dominante em organismos vivos é o MgATP. Uma maior constante de ligação também deu ao magnésio a vantagem como um melhor catalisador sobre outros metais concorrentes.
Manganês[editar | editar código-fonte]

As evidências sugerem que o manganês (Mn) foi incorporado pela primeira vez aos sistemas biológicos há cerca de 3,2 – 2,8 bilhões de anos, durante o Período Arqueano. Junto com o cálcio, formou o complexo manganês-óxido de cálcio (determinado por cristalografia de raios-X) que consistia em um aglomerado de manganês – essencialmente uma estrutura inorgânica cubana (cúbica). A incorporação de um centro de manganês no fotossistema II foi altamente significativa, pois permitiu a evolução do oxigênio fotossintético das plantas. O complexo evolutivo de oxigênio (OEC) é um componente crítico do fotossistema II contido nas membranas tilacóides dos cloroplastos; é responsável pela foto-oxidação terminal da água durante as reações à luz.[12]
A incorporação de Mn em proteínas permitiu aos complexos a capacidade de reduzir espécies reativas de oxigênio em Mn-superóxido dismutase (MnSOD) e catalase, em catálises dependentes da transferência de elétrons (por exemplo, em certas redutases de ribonucleotídeo classe I) e na oxidação de água pelo fotossistema II (PSII), onde a produção de substâncias reativas ao ácido tiobarbitúrico é diminuída. Isso se deve à capacidade do manganês de reduzir o ânion superóxido e os radicais hidroxila, bem como sua capacidade de quebrar a cadeia.[13]
Ferro[editar | editar código-fonte]
O Ferro (Fe) é o elemento mais abundante na Terra e o quarto elemento mais abundante na crosta, aproximadamente 5% em massa. Devido à abundância de ferro e seu papel nos sistemas biológicos,[1] a transição e os estágios mineralógicos do ferro têm desempenhado um papel fundamental nos sistemas da superfície terrestre. Ele desempenhou um papel importante no passado geológico na geoquímica marinha, como evidenciado pelos depósitos de sedimentos ricos em ferro do Pré-cambriano. A transformação redox de Fe (II) em Fe (III), ou vice-versa, é vital para uma série de processos biológicos e do ciclo de elementos. A redução de Fe (III) oxida o enxofre (de H2S a SO4−2 ), que é um processo central nos sedimentos marinhos. Muitas das primeiras metaloproteínas consistiam em complexos de ferro-enxofre formados durante a fotossíntese.[14] O ferro é o principal metal redox em sistemas biológicos. Nas proteínas, é encontrado em uma variedade de locais e cofatores, incluindo, por exemplo, osgrupos heme, locais Fe-O-Fe e os aglomerados de ferro-enxofre.
A prevalência de ferro é aparentemente devido à grande disponibilidade de Fe (II) na evolução inicial dos organismos vivos [1], antes do aumento da fotossíntese e um aumento nos níveis de oxigênio atmosférico que resultou na precipitação de ferro no meio ambiente na forma Fe(OH)3. Possui propriedades redox flexíveis porque tais propriedades são sensíveis à coordenação do ligante, incluindo a geometria. O ferro também pode ser usado em enzimas devido às suas propriedades de ácido de Lewis, por exemplo, na nitrila hidratase. O ferro é frequentemente encontrado em sítios mononucleares na forma reduzida de Fe(II) e atua na ativação de dioxigênio; essa função é utilizada como um dos principais mecanismos adotados pelos organismos vivos para evitar que a barreira cinética impeça a transformação dos compostos orgânicos pelo O2.[15] O ferro pode ser absorvido seletivamente como ferredoxinas, Fe-O-Fe (hemeritrina e ribonucleotídeo redutase), Fe (muitas oxidases), além da porfirina de ferro.
A variação nas proteínas relacionadas com qualquer uma dessas formas químicas de ferro produziu uma ampla gama de enzimas. Todos esses arranjos são modificados para funcionar tanto no sentido de reatividade quanto no posicionamento da proteína na célula. O ferro pode ter vários estados redox e spin, e pode ser mantido em muitas estereoquímicas.[16]
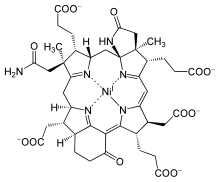
Níquel e cobalto[editar | editar código-fonte]

Por volta de 4–3 bilhões de anos atrás, procariotos anaeróbios começaram a desenvolver metais e cofatores orgânicos para absorção de luz. No final das contas, acabaram produzindo clorofila a partir do Mg (II), como é encontrado em cianobactérias e plantas, levando à fotossíntese moderna. No entanto, a síntese da clorofila requer várias etapas. O processo começa com a uroporfirina, um precursor primitivo do anel porfirínico que pode ser de origem biótica ou abiótica, que é então modificado nas células de forma diferente para formar complexos de magnésio (Mg), ferro (Fe), níquel (Ni) e cobalto (Co). Os centros desses anéis não são seletivos, permitindo assim a incorporação de uma variedade de íons metálicos. A porfirina de Mg dá origem à clorofila, a porfirina de Fe às proteínas heme,[1] a porfirina de Ni produz o fator F-430 e a porfirina de Co a vitamina B12.[17]
Cobre[editar | editar código-fonte]
Antes do Grande Evento de Oxigenação, o cobre não estava disponível para os organismos vivos. A maioria dos primeiros cobre era Cu+ e Cu. Este estado de oxidação do cobre não é muito solúvel em água. Um bilhão de anos atrás, após o grande evento de oxigenação, a pressão do oxigênio aumentou o suficiente para oxidar Cu+ a Cu2+, aumentando sua solubilidade em água. Como resultado, o cobre se tornou muito mais disponível para os organismos vivos.[1]
A maioria das proteínas e enzimas que contêm cobre podem ser encontradas em eucariotos. Apenas um punhado de procariontes, como bactérias aeróbias e cianobactérias, contém enzimas ou proteínas de cobre. O cobre pode ser encontrado na enzima superóxido dismutase (SOD) de procariontes e eucariotos. Existem três tipos distintos de SOD, contendo Mn, Fe e Cu, respectivamente.
As Mn-SOD e Fe-SOD são encontradas na maioria dos procariotos e mitocôndrias da célula eucariótica. O Cu-SOD pode ser encontrado na fração citoplasmática das células eucarióticas. Os três elementos, cobre, ferro e manganês, podem catalisar superóxido em oxigênio molecular comum ou peróxido de hidrogênio. No entanto, o Cu-SOD é mais eficiente do que Fe-SOD e Mn-SOD. A maioria dos procariontes utiliza apenas Fe-SOD ou Mn-SOD devido à falta de cobre no ambiente. Alguns organismos não desenvolveram Cu-SOD devido à falta de um pool de genes para a adoção de Cu-SOD.[18]
Zinco[editar | editar código-fonte]
O zinco (Zn) foi incorporado às células vivas em duas ondas. Quatro a três bilhões de anos atrás surgiram procariotos anaeróbicos, e a atmosfera estava cheia de H2S e altamente redutiva. Assim, a maior parte do zinco estava na forma de ZnS insolúvel. No entanto, como a água do mar na época era ligeiramente ácida, uma pequena quantidade Zn (II) estava disponível em sua forma iônica e tornou-se parte das primeiras proteases externas dos procariotos anaeróbios, nucleases externas, sintetases internas e desidrogenases.[8]
Durante a segunda onda, uma vez que ocorreu o Grande Evento de Oxigenação, mais íons Zn (II) estavam disponíveis na água do mar. Isso permitiu sua incorporação nos eucariotos unicelulares à medida que surgiam nessa época. Acredita-se que a adição posterior de íons como zinco e cobre permitiu que eles deslocassem o ferro e o manganês da enzima superóxido dismutase (SOD). Os complexos de Fe e Mn se dissociam prontamente (série Irving-Williams), enquanto o Zn e o Cu não. É por isso que a SOD eucariótica contém Cu ou Zn e sua contraparte procariótica contém Fe ou Mn.[8]
O Zn (II) não representa uma ameaça de oxidação ao citoplasma. Isso permitiu que ele se tornasse um importante elemento citoplasmático nos eucariotos. Tornou-se associado a um novo grupo de proteínas de transcrição, dedos de zinco. Isso só poderia ter ocorrido devido à longa vida dos eucariotos, que deu tempo para trocar o zinco e, portanto, tornar-se um mensageiro interno coordenando a ação de outros fatores de transcrição durante o crescimento.[8]
Molibdênio[editar | editar código-fonte]
O molibdênio (Mo) é o elemento de transição mais abundante em solução no mar (principalmente como íon molibdato dianiônico) e em organismos vivos, sua abundância na crosta terrestre é bastante baixa. Portanto, o uso de Mo por organismos vivos parece surpreendente à primeira vista. Arquéias, bactérias, fungos, plantas e animais, incluindo humanos, requerem molibdênio. Também é encontrado em mais de 50 enzimas diferentes. Sua hidrólise em espécies oxo-aniônicas solúveis em água torna o Mo facilmente acessível. O Mo é encontrado nos sítios ativos de metaloenzimas que realizam transformações importantes no metabolismo de compostos de carbono, nitrogênio, arsênio, selênio, enxofre e cloro. As enzimas mononucleares de molibidênio são amplamente distribuídas na biosfera; elas catalisam muitas reações significativas no metabolismo de compostos contendo nitrogênio e enxofre, bem como vários compostos de carbonila (por exemplo, aldeídos, CO e CO2 ). Enzimas redutases de nitrato são importantes para o ciclo do nitrogênio. Elas pertencem a uma classe de enzimas com um centro mononuclear de Mo e catalisam a reação do metabolismo de C, N, S, etc., em bactérias, plantas, animais e humanos. Devido à oxidação dos sulfetos, o primeiro desenvolvimento considerável foi o de bactérias aeróbias que agora podiam utilizar Mo. À medida que o oxigênio começou a se acumular na atmosfera e nos oceanos, a reação de MoS2 a MoO4 também aumentou.
Essa reação tornou o íon molibdato altamente solúvel disponível para incorporação em metaloenzimas críticas e pode ter permitido que a vida prosperasse. Permitiu que os organismos ocupassem novos nichos ecológicos. O molibidênio desempenha um papel importante na redução do dinitrogênio em amônia, que ocorre em um tipo de nitrogenases. Essas enzimas são usadas por bactérias que geralmente vivem em uma relação simbiótica com as plantas; seu papel é a fixação de nitrogênio, que é vital para sustentar a vida na Terra. As enzimas Mo também desempenham papéis importantes no metabolismo do enxofre de organismos que variam de bactérias a humanos.
Tungstênio[editar | editar código-fonte]

O tungstênio é um dos íons metálicos mais antigos a ser incorporado em sistemas biológicos, precedendo o Grande Evento de Oxigenação. Antes da abundância de oxigênio na atmosfera da Terra, os oceanos fervilhavam de enxofre e tungstênio, enquanto o molibdênio, um metal muito semelhante quimicamente, era inacessível na forma sólida.
A abundância de tungstênio e a falta de molibdênio livre provavelmente explica por que os primeiros organismos marinhos incorporaram o primeiro em vez do segundo. No entanto, à medida que as cianobactérias começaram a encher a atmosfera de oxigênio, o molibdênio tornou-se disponível (o molibdênio torna-se solúvel quando exposto ao oxigênio) e o molibdênio começou a substituir o tungstênio na maioria dos processos metabólicos, o que é visto hoje, já que o tungstênio está presente apenas em complexos biológicos de procariotos (metanógenos, bactérias gram-positivas, aeróbios gram-negativos e anaeróbios), e só é obrigatório em arquéias hipertermofílicas como P. furiosus. O ponto de fusão extremamente alto do tungstênio (3.422 °C), parcialmente explica sua necessidade nestas arqueias, encontradas em áreas extremamente quentes.[19]
Embora as pesquisas sobre os complexos enzimáticos específicos nos quais o tungstênio é incorporado sejam relativamente recentes (década de 1970), as tungstoenzimas naturais são abundantemente encontradas em um grande número de microrganismos procarióticos. Estes incluem formato desidrogenase, formil metanufurano desidrogenase, acetileno hidratase e uma classe de oxidorredutases relacionadas filogeneticamente que catalisam a oxidação reversível de aldeídos. A primeira estrutura cristalina de uma enzima contendo tungstênio ou pterina, a da aldeído ferredoxina oxidoredutase de P. furiosus, revelou um sítio catalítico com um átomo de tungstênio coordenado a duas moléculas de pterina que são interligadas por um íon de magnésio.[20]
Referências
- ↑ a b c d e f Lima, Ricardo Junio Feitosa (2020). «A SELEÇÃO NATURAL DOS ELEMENTOS QUÍMICOS: Estudo da Seleção de Elementos Para os Processos Vitais». Centro Universitário Uniages. Publicações Even3. doi:10.29327/4119406. Consultado em 22 de fevereiro de 2021
- ↑ a b c Monosson, Emily (2012). Evolution in a Toxic World. Springer (em inglês). [S.l.: s.n.] ISBN 978-1-59726-341-2. doi:10.5822/978-1-61091-221-1
- ↑ a b Russel, MJ; William, M (2003). «On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes,and from prokaryotes to nucleated cells». Philosophical Transactions of the Royal Society of London B: Biological Sciences. 358 (1429): 59–85. PMC 1693102
 . PMID 12594918. doi:10.1098/rstb.2002.1183
. PMID 12594918. doi:10.1098/rstb.2002.1183
- ↑ Wang, MS; Hoegler, KH; Hecht, M (2019). «Unevolved De Novo Proteins Have Innate Tendencies to Bind Transition Metals». Life. 9 (8): 8. PMC 6463171
 . PMID 30634485. doi:10.3390/life9010008
. PMID 30634485. doi:10.3390/life9010008
- ↑ Gonzalez, R.N.; Ponnamperuma, C. (1995). «Role of Trace Metal ions in Chemical Evolution. The case of free radical reactions». Advances in Space Research. 15 (3): 357–364. Bibcode:1995AdSpR..15..357N. PMID 11539250. doi:10.1016/s0273-1177(99)80107-0
- ↑ Kleczkowski, M; Garncarz, M (2012). «The role of metal ions in biological oxidation- the past and the present». Polish Journal of Veterinary Sciences. 15 (1): 165–173. PMID 22708374. doi:10.2478/v10181-011-0130-8
- ↑ a b c Williams, R.J.P.; Frausto da Silva, J.J.R. (2006). The Chemistry of Evolution. Elsevier. Amsterdam: [s.n.] ISBN 9780080460529
- ↑ a b c d Williams, R.J.P. (2012). «Zinc in Evolution». Journal of Inorganic Biochemistry. 111: 104–109. PMID 22855949. doi:10.1016/j.jinorgbio.2012.01.004
- ↑ Maguire, Michael E.; Cowan, James A (2002). «Magnesium chemistry and biochemistry». BioMetals. 15: 203–210. PMID 12206387. doi:10.1023/a:1016058229972
- ↑
Gout, Elisabeth; Rébeillé, Fabrice; Douce, Roland; Bligny, Richard (13 de outubro de 2014). «Interplay of Mg2+, ADP, and ATP in the cytosol and mitochondria: Unraveling the role of Mg2+ in cell respiration». Proceedings of the National Academy of Sciences. 111 (43): E4560–E4567. Bibcode:2014PNAS..111E4560G. PMC 4217410
 . PMID 25313036. doi:10.1073/pnas.1406251111
. PMID 25313036. doi:10.1073/pnas.1406251111
- ↑ Williams, Nicholas H. (2000). «Magnesium Ion Catalyzed ATP Hydrolysis». Journal of the American Chemical Society. 122 (48): 12023–12024. doi:10.1021/ja0013374
- ↑ Williams, R.J.P. (2007). «Systems biology of evolution: the involvement of metal ions». BioMetals. 20 (2): 107–112. PMID 17295048. doi:10.1007/s10534-007-9087-6
- ↑
Salomon, Etian; Keren, Nir (2011). «Manganese in Biological systems: Transport and Function». [S.l.: s.n.] ISBN 9780470682531. doi:10.1002/9780470682531.pat0540 Em falta ou vazio
|título=(ajuda) - ↑ Taylor, K.G.; Konhauser, K.O. (2011). «Iron in Earth surface systems: A major player in chemical and biological processes». Elements. 7 (2): 83–88. doi:10.2113/gselements.7.2.83
- ↑ Andreini, C.; Bertini, I.; Cavallaro, G.; Holliday, G.L.; Thornton, J.M. (2008). «Metal ions in biological catalysis: from enzyme databases to general principles». Journal of Biological Inorganic Chemistry. 13 (8): 1205–1218. PMID 18604568. doi:10.1007/s00775-008-0404-5
- ↑ Williams, R.J.P. (1985). «The symbiosis of metal and protein functions». European Journal of Biochemistry. 150 (2): 231–248. PMID 2990929. doi:10.1111/j.1432-1033.1985.tb09013.x
- ↑ Frank, S.; Brindley, A.A.; Deery, E.; Heathcote, P.; Lawrence, A.D.; Leech, H.K.; Pickersgill, R.W.; Warren, M.J. (2005). «Anaerobic synthesis of vitamin B12: characterization of the early steps in the pathway». Biochemical Society Transactions. 33: 811–814. PMID 16042604. doi:10.1042/BST0330811
- ↑ Ochiai, Ei-Ichiro (1983). «Copper and the Biological Evolution». Biosystems. 16: 81–86. PMID 6640084. doi:10.1016/0303-2647(83)90029-1
- ↑ Kletzin, Arnulf; Adams, Michael W. (1996). «Tungsten in Biological Systems». FEMS Microbiology Reviews. 18: 5–63. PMID 8672295. doi:10.1111/j.1574-6976.1996.tb00226.x
- ↑ Sigel; Sigel, eds. (2002). Metal ions in biological systems: molybdenum and tungsten: their roles in biological processes. Taylor & Francis. 39. [S.l.: s.n.]
