Ácido fosfórico: diferenças entre revisões
m Foram revertidas as edições de 177.43.254.84 (usando Huggle) (3.1.20) |
|||
| Linha 53: | Linha 53: | ||
== Fabricação == |
== Fabricação == |
||
Na indústria, o ácido fosfórico pode ser feito por dois métodos: |
Na indústria, o ácido fosfórico pode ser feito por dois métodos: |
||
* via |
* via úmida; |
||
* via seca ou térmica; |
* via seca ou térmica; |
||
Revisão das 19h13min de 5 de novembro de 2016
Este artigo não cita fontes confiáveis. (Maio de 2014) |
Este artigo ou se(c)ção está a ser traduzido. |
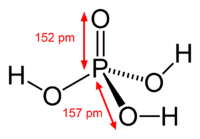
Ácido fosfórico ou ácido ortofosfórico é um composto químico fórmula molecular H3PO4. É o ácido de fósforo mais importante. Dentre os ácidos minerais, pode ser considerado um ácido mais fraco. A partir do ácido fosfórico derivam-se o ácido difosfórico ou pirofosfórico, o ácido metafosfórico e o ácido polifosfórico.
Características
O ácido H3PO4 é monovalente, isto é, os três hidrogênios ácidos podem ser convertidos por substituição gradual a fosfatos primários, secundários e terciários. Os valores respectivos de pKa são 2,15 / 7,1 e 12,4. O ácido fosfórico é, portanto, um ácido que varia de fraco a medianamente forte. Seus sais são chamados de fosfatos.
É muito solúvel em água e solúvel em etanol. O ácido fosfórico é muito deliquescente e é geralmente fornecido como uma solução aquosa concentrada a 85%.
É o derivado do fósforo mais importante comercialmente, respondendo por mais de 90% da rocha fosfática que é extraída.
O ácido fosfórico origina três séries de sais contendo os íons fosfato (V) cujos ânions são: [(HO)2PO2]-, [(HO)PO3]2- e PO43-. Estes sais apresentam um carácter respectivamente ácido, neutro e alcalino e são muitas vezes utilizados para se obter soluções tampão.
Fabricação
Na indústria, o ácido fosfórico pode ser feito por dois métodos:
- via úmida;
- via seca ou térmica;
A via húmida é responsável pela maior parte da produção industrial de ácido fosfórico. Nesse processo, rochas sedimentares ou magmáticas portadoras do mineral apatita (Ca5(PO4)3(X)), sendo X = F, OH ou Cl, reagem com ácido sulfúrico. Os subprodutos do processo são o CaSO4 (gesso, anidrita ou gipsita) e o H2SiF6.
A via seca ou térmica consiste na queima de fósforo branco ao ar, com a formação de P4O10 e sua hidrólise subsequente. O ácido fosfórico produzido dessa forma é de grau farmacêutico.
Propriedades
- Densidade: 1,69 típica.
- Massa molecular: 97,97 g/mol
- pH: < 1.
- Ponto de congelamento: 21 °C.
- Ponto de ebulição: 158 °C.
- Pressão de vapor: (mmHg, 25 °C) 2,24 (água).
- Solubilidade em água: Incompleta, 93%.
- Concentração: 55%.
Principais usos
- Indústria de fertilizantes, industria de produção de sal mineral para alimentação animal, formulação de detergentes, decapante, refrigerantes.
- Indústria de bebidas
- Odontologia: utilizado para condicionamento de tecido dentário para fixação de sistemas adesivos
- Indústria farmacêutica
- Indústria de bebidas
- Usina de chocolate
- Indústria farmacêutica
- Indústria farmacêutica
Fonte: https://sites.google.com/site/scientiaestpotentiaplus/acido-fosforico