Primeira lei da termodinâmica
Esta página ou seção foi marcada para revisão devido a incoerências ou dados de confiabilidade duvidosa. |
| Termodinâmica | ||||||
|---|---|---|---|---|---|---|
 Processo de convecção. | ||||||
| Glossário de termodinâmica | ||||||
|
Ramos |
||||||
|
Sistema termodinâmico
|
||||||
|
Grandezas físicas |
||||||
|
Potencial termodinâmico |
||||||
|
||||||
A primeira lei da termodinâmica é uma versão da lei de conservação da energia. Também conhecido como Princípio de Joule, este postulado admite que diversas formas de trabalho podem ser convertidas umas nas outras, elucidando que a energia total transferida para um sistema é igual à variação de sua energia interna, ou seja, em todo processo natural, a energia do universo se conserva sendo que a energia do sistema quando isolado é constante. Observa-se também a equivalência entre trabalho e calor, onde constatou-se que a variação Q - W é a mesma para todos os processos termodinâmicos.
Descrição[editar | editar código-fonte]
Termodinâmica é o ramo da física que estuda as leis que regem as relações entre trabalho, calor e energia térmica, geralmente tratada como a energia interna dos sistemas. A termodinâmica está preocupada com a modelagem matemática do mundo real, sendo que os conceitos centrais neste estudo servem para caracterizar um sistema termodinamicamente em equilíbrio, sendo que Pressão, Temperatura e Volume são variáveis mensuráveis macroscopicamente e determinam o estado de equilíbrio termodinâmico.
A primeira declaração explícita da primeira lei da termodinâmica, dada por Rudolf Clausius em 1850, refere-se a processos termodinâmicos cíclicos. Sempre que o trabalho for produzido pelo órgão gerador de calor, certa quantidade desta energia é consumida, que é proporcional ao trabalho realizado; por outro lado, por o gasto de uma quantidade igual de trabalho a mesma quantidade de calor é produzida.
Clausius descreveu a primeira lei de outra forma, referindo-se a existência de uma função do estado do sistema chamada energia interna (U), expressa em termos de uma equação diferencial para os estados de um processo termodinâmico. Esta equação pode ser traduzida em palavras como se segue:
"Em um processo termodinâmico fechado, a alteração da energia interna do sistema é igual à diferença entre a alteração do calor acumulado pelo sistema e da alteração do trabalho realizado".
A energia interna é a soma das energias cinética e potencial de todas as partículas que constituem este sistema. Por esta razão, é considerada uma propriedade do sistema, depende somente do estado inicial e estado final do processo. Ainda, quanto maior a taxa de calor que está sendo transferida a determinado sistema, maior será sua energia interna. Assim, temos:
, quando o sistema recebe calor;
, quando o sistema perde calor.
Desta forma, quanto maior a energia interna de um sistema, maior será seu potencial para a realização de trabalho, sendo que convenciona-se que W>0, quando o sistema se expande e perde energia para o meio externo e W<0, quando o sistema se contrai e recebe energia do meio externo.
Termodinamicamente, se o estado de um sistema muda, então ele está passando por um processo. A sucessão de estados através da qual passa o sistema define o caminho do processo. Se, no final do processo, as propriedades tiverem regressado aos seus valores iniciais, o sistema foi submetido a um processo cíclico. A equação que descreve a relação entre a pressão, volume e temperatura é dada por:
onde: é o número de mols e é a constante universal dos gases, R = 8,31 J/mol.K
Formulação matemática[editar | editar código-fonte]
Calor, trabalho e propriedades termodinâmicas[editar | editar código-fonte]
Para introduzir aos conceitos da primeira lei da termodinâmica é valido antes apresentar o conceito de o que são propriedades termodinâmicas e como o calor e o trabalho estão envolvidos com as mesmas. Primeiramente, as propriedades termodinâmicas são aquelas que definem o estado termodinâmico, entre elas, a pressão, temperatura, volume e energia interna, vale ressaltar que o estado termodinâmico muda quando pelo menos uma das propriedades do sistema é alterada.
No entanto o que acontece com o calor e o trabalho é que nenhum sistema possui calor ou trabalho, o sistema apenas os produz, fazendo com que eles dependam do processo termodinâmico envolvido durante uma mudança de estado. Portanto, calor e trabalho, não são propriedades termodinâmicas e sim efeitos de fronteira do sistema.
Processos Cíclicos[editar | editar código-fonte]
A primeira lei da termodinâmica pode ser definida a partir das integrais cíclicas de calor e trabalho, onde durante qualquer ciclo termodinâmico gerado, a integral cíclica do calor será diretamente proporcional a integral cíclica do trabalho:
Em um ciclo termodinâmico, o processo envolvido retorna ao seu estado original, ou seja se houver uma mudança de estado de 1 a 2 por uma curva "a" em um ciclo terá um retorno de 2 a 1 por uma curva "b". Então tem-se:
ajustando a formula para isolar o processo a do processo b:
Com isso pode-se concluir que a diferença entre calor e trabalho independe do calor e do trabalho, portanto é uma propriedade termodinâmica sendo essa a energia[1][2]. A Lei zero da termodinâmica define temperatura, enquanto a Primeira Lei define a função de estado Energia Interna. Podemos simplificar dizendo que existe uma função (energia interna) cuja variação durante uma transformação depende unicamente de dois estados, o inicial e o final. Num sistema fechado a indicação desta variação é dada como:
Na equação acima, convencionou-se Q positivo quando é acrescida energia ao sistema e negativo quando retirada; do mesmo modo, a energia interna diminui se for cedida energia para a vizinhança sob a forma de trabalho W, ou seja, se o sistema realizar trabalho.
- Para o cálculo de trabalho (W):
onde, F = pressão (p) . área (A)
onde p é a pressão e dV, volume na forma infinitesimal.
Pelo cálculo da integral,
=
Para o cálculo do calor (Q):
onde, c é o calor específico, m é a massa e T temperatura
Quando a mudança de estado físico, temos:
onde, m é massa e L é calor de transformação (específico a cada substância)
Podemos transferir energia para dentro ou para fora do sistema, seja sob forma de calor ou pela forma de trabalho. Suponhamos que o sistema esteja em um estado inicial i e realiza trabalho, expandindo-se. Este trabalho mecânico diminui a energia interna do sistema, então:
=
Podemos também variar o estado do sistema colocando-o em contato térmico com outro sistema cuja temperatura esteja diferente. Assim, há certa quantidade de energia em trânsito, que se desloca do sistema de maior valor Q para o menor, fazendo com que haja um aumento da energia interna do sistema inicialmente com menor quantidade de energia. Assim,
=
Casos especiais[editar | editar código-fonte]
- Processos adiabáticos: Processo em que não há troca de calor com o meio externo, . A variação da energia interna se deve ao trabalho pelo sistema. Exemplo: desodorante aerossol e champagne.
- Processos a volume constante: Também chamado processo isocórico, o sistema não realiza trabalho, W = 0. A variação da energia interna depende da diferença de temperatura.
- Processos cíclicos: A energia interna não varia porque obtém volume, pressão e temperatura iguais no estado inicial e final. O trabalho será negativo e corresponde à área dentro da figura. Por convenção: +W quando se desloca no sentido horário e -W quando desloca-se no sentido anti-horário.
- Expansões livres: Transformações adiabáticas (sem troca de calor, enquanto a temperatura pode variar) nas quais nenhum trabalho é realizado. Ocorre uma ocupação de um espaço vazio, então .
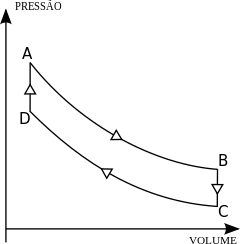
No segmentos e são processos isotérmicos (temperatura constante). Já os segmentos e são processos isovolumétricos (volume constante), sendo que a energia interna do sistema varia somente pela troca de calor com as vizinhanças do sistema
Em resumo
| Adiabático | , = - |
| V constante | , = |
| Cíclicos | , |
| Expansões livres | , |
História[editar | editar código-fonte]
A primeira lei da termodinâmica para sistemas fechados foi originalmente comprovada pela observação empírica; no entanto, é hoje considerado como a definição de calor através da lei da conservação da energia e da definição de trabalho em termos de mudanças nos parâmetros externos de um sistema. A descoberta original da lei foi gradual ao longo de um período de talvez meio século ou mais.
Em meados do século XIX, um dos assuntos mais intrigantes aos cientistas da época era a transformação de calor em movimento através das máquinas térmicas. Neste período, ocorria a Revolução Industrial na Inglaterra e as máquinas térmicas a vapor foram as grandes responsáveis por parte do seu sucesso. O princípio dessas máquinas era bastante simples: aquecendo um gás ele se expandia. Em 1763, o escocês James Watt percebeu que havia um grande desperdício de vapor, que custava dinheiro e diminuía os lucros das indústrias. Entretanto, acredita-se que a primeira máquina térmica seja datada de 50 d.C. e desenvolvida por Héron de Alexandria. Héron, descobriu que o ar se expandia quando aquecido, e assim, poderia utilizá-lo para produzir força mecânica. O grande Leonardo da Vinci também usou o vapor d'água para produzir movimentos.
Preocupado em aperfeiçoar as máquinas térmicas, o cientista francês Sadi Carnot (1796-1832), desenvolveu, em 1824, a teoria que explicava o rendimento de uma máquina, ou seja, quanto de calor a máquina transformava em trabalho. Ele então desenvolveu um modelo teórico para as máquinas térmicas e descobriu qual deveria ser a maneira mais eficiente de transformar calor em movimento. A esse modelo teórico, deu-se o nome de Máquina de Carnot.
O estabelecimento do princípio da conservação de energia também ocorreu no século XIX, em estudos da termodinâmica. Nessa época, já se sabia que o calor poderia ser gerado pelo atrito (energia mecânica), eletricidade e reações químicas. Por volta de 1840, o físico inglês Joule (1818-1889) em seus estudos, procurou quantificar a energia mecânica necessária que equivalesse a uma caloria. Em sua homenagem, atribuiu-se o seu nome à unidade de energia, Joule [J]. 1 cal = 4,186 J.
Em 1848,o engenheiro, físico e matemático William Thomson, também conhecido como Lorde Kelvin, publicou um artigo fundamentado na teoria de Carnot. Nele, buscou a equivalência entre a escala dos gases ideais e a escala termodinâmica, desenvolvendo uma escala cujas referências eram os pontos fixos: zero absoluto (0) e a temperatura do gelo fundente (273,15). Essa escala é utilizada até hoje e, em sua homenagem, sua unidade no SI é Kelvin [K].
Baseados nos trabalhos de Joule e um outro cientista, denominado Mayer, Rudolf Clausius e Lorde Kelvin, em 1850, desenvolveram a Primeira e a Segunda Lei da Termodinâmica. Isso, mudaria completamente a compreensão do calor como forma de energia e ampliou o campo de atuação da termodinâmica.[3][4]
Referências
- ↑ Moran, Michael J.; Scofano Neto, Francesco, (2002). Principios de termodinamica para engenharia 4. ed ed. Rio de Janeiro: LTC. OCLC 69933738
- ↑ Sonntag, Richard E.; Van Wylen, Gordon John.; Zerbini, Euryale Jorge Godoy de Jesus, (2003). Fundamentos da termodinâmica. São Paulo: Edgard Blucher. OCLC 57019212
- ↑ Clausius, R. (1850) «Über die bewegende Kraft der Wärme» Annalen der Physik und Chemie. Vol. 79. pp. 368-397, 500-524.
- ↑ Thomson, W. (Lord Kelvin) (1851) «On the Dynamical Theory of Heat, with Numerical Results Deduced from Mr Joule’s Equivalent of a Thermal Unit, and M. Regnault’s Observations on Steam» Transactions of the Royal Sociey of Edinburgh. Vol. 20. pp. 261-268, 289-298.
Bibliografia[editar | editar código-fonte]
- Lee, John F.; Sears, Francis W.. Termodinâmica. ed SEDEGRA, 1969
- Pauli, Wolfgang. Thermodynamics and the kinetic theory of gases. Vol. 3. Cambrige
- Clausius, R. (1850) «Über die bewegende Kraft der Wärme» Annalen der Physik und Chemie. Vol. 79. pp. 368–397, 500-524.
- Thomson, W. (Lord Kelvin) (1851) «On the Dynamical Theory of Heat, with Numerical Results Deduced from Mr Joule’s Equivalent of a Thermal Unit, and M. Regnault’s Observations on Steam» Transactions of the Royal Sociey of Edinburgh. Vol. 20. pp. 261–268, 289-298.
- Halliday, David; Walker, Jearl; Resnick, Robert. Fundamentos de Física: Gravitação, Ondas e Termodinâmica. Vol. 2. ed. LTC. 7ªed., 2003.
- Atkins, J. de Paula. Físico-Química, LTC Editora. 7ªed, 2003.
- Passos, Júlio César. Os experimentos de Joule e a primeira lei da termodinâmica. Revista Brasileira de Ensino de Física. vol.31 no.3. São Paulo. edição jul./set, 2009.
- Ferreira, G.F. Leal. Uma definição natural de energia cinética e potencial em termodinâmica. Revista Brasileira de Ensino de Física. v.29 n.1. São Paulo, 2007.
- Moran, Michel; Shapiro, Howard N.. Princípios de termodinâmica para engenharia. Rio de Janeiro: LTC, 2002. ISBN 8521613407; 9788521613404.
- Sonntag, Richard E.; Borgnakke, Claus; Van Wylen, Gordon J.. Fundamentos da termodinâmica. São Paulo: Edgard Blücher, 2003. ISBN 8521203276; 9788521203278.













































