Difusão molecular
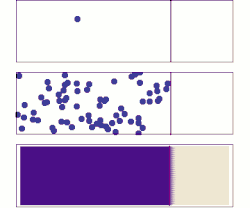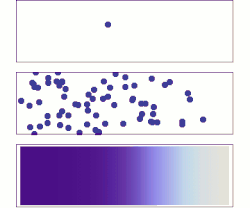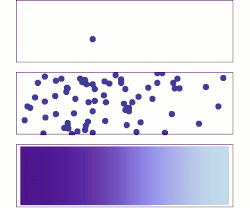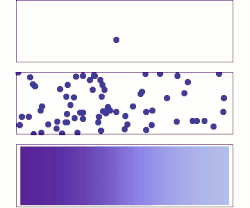
A difusão molecular é um exemplo de fenômeno de transporte de matéria à curta distância no qual um soluto é transportado devido aos movimentos das moléculas de um fluido (líquido ou gás), pelo movimento térmico de todas as partículas a temperaturas acima do zero absoluto. Estes movimentos fazem com que, do ponto de vista macroscópico, o soluto passe das zonas mais elevadas de concentração para zonas de baixa concentração.
A difusão molecular de um solvente ocorre no sentido inverso, ou seja, de uma solução menos concentrada para uma solução mais concentrada. Quando esta difusão do solvente ocorre através de uma membrana semi-permeável é denominada de osmose. A solução menos concentrada é denominada hipotônica e a mais concentrada de hipertônica. Este processo de difusão do soluto ou solvente é extremamente importante na absorção de nutrientes pelas células, através da membrana celular. A difusão acontece até as duas soluções ficarem "isotônicas", isto é, com a mesma concentração.
A taxa deste movimento é uma função da temperatura, viscosidade do fluido e o tamanho (massa) das partículas, mas não é função da concentração. Difusão explica o fluxo líquido (o balanço) de moléculas de uma região de concentração mais alta para uma de concentração mais baixa, mas é importante se notar que difusão também ocorre onde não existe um gradiente de concentração. O resultado da difusão é uma gradual mistura de materiais. Em uma fase com temperatura uniforme, ausência de forças externas líquidas atuando sobre as partículas, o processo de difusão acabará por resultar em mistura completa.
A difusão molecular é tipicamente descrita matematicamente usando-se as leis de Fick da difusão.
Classificações
[editar | editar código-fonte]Para efeitos de classificação, e dos equacionamentos específicos, a difusão é dividida quanto à homogeneidade ou heterogeneidade das espécies em difusão como autodifusão, quando a difusão se dá entre átomos de mesma espécie (como entre seus isótopos) e interdifusão, quando a difusão se dá entre átomos de espécies diferentes.
Exemplificando: quando se tem duas misturas gasosas, consideradas a mesma pressão e temperatura, formadas apenas de hidrogênio prótio e seu isótopo mais pesado, com um nêutron a mais no núcleo, deutério, mas de composições destes diferentes, e que são colocadas em contato, a difusão dos isótopos na mistura trata-se de autodifusão.
Quando temos carbono em liga de ferro, e este migra para outra parte da liga com menor concentração de carbono, como os átomos são de diferentes elementos, de núcleos de diferentes números de prótons, trata-se de interdifusão.
Aplicações
[editar | editar código-fonte]Difusão é de importância fundamental em muitas disciplinas de física, química e biologia. Alguns exemplos de aplicações da difusão são:
- Sinterização para produzir materiais sólidos (metalurgia do pó, produção de cerâmicas)
- Projeto de reatores químicos
- Projeto de catalisadores em indústria química
- Aço pode passar por processos que incluam difusão (e.g., com carbono ou nitrogênio) para modificar suas propriedades
- Aplicação de dopantes durante a produção de semicondutores.
Significância
[editar | editar código-fonte]
Difusão é parte dos fenômenos de transportes. Dos mecanismos de transporte de massa, a difusão molecular é conhecida como a mais lenta.
Em Biologia
[editar | editar código-fonte]Em biologia celular, difusão é a principal forma de transporte para materiais necessários tais como aminoácidos no interior das células.[1] A difusão de água (H2O) através de uma parcialmente permeável membrana é classificada como osmose.
O metabolismo e a respiração dependem, em parte, da difusão, além de processos em massa ou ativos. Por exemplo, nos alvéolos de pulmões de mamíferos, devido à diferenças em pressões parciais através da membrana dos capilares do alvéolo, o oxigênio difunde-se no sangue e o dióxido de carbono difunde-se para o exterior. Pulmões possuem uma grande área de superfície para facilitar este processo de troca gasosa.
Difusão de marcador e química
[editar | editar código-fonte]

Fundamentalmente, dois tipos de difusão são distinguidos:
- Difusão de marcador, a qual é uma mistura espontânea de moléculas tomando lugar na ausência de gradiente de concentração (ou potencial químico). Este tipo de difusão pode ser acompanhado usando-se marcadores isotópicos, daí seu nome. A difusão do marcador normalmente é assumido como sendo idêntico a autodifusão (assumindo-se que não há significativo efeito isotópico). Esta difusão pode ocorrer sob equilíbrio.
- Difusão química ocorre na presença de gradiente de concentração (ou potencial químico) e resulta no transporte de massa em balanço, líquido. Esta difusão é sempre um processo em não equilíbrio, aumentando a entropia do sistema, e conduz o sistema mais próximo do equilíbrio.
Os coeficientes de difusão para estes dois tipos de difusão são geralmente diferentes porque o coeficiente de difusão para difusão química é binário e inclui os efeitos devido à correlação do movimento de diferentes espécies em difusão.
Sistemas em desequilíbrio
[editar | editar código-fonte]
Porque difusão química é um processo de transporte em balanço, o sistema no qual ele toma lugar é um sistema em equilíbrio (i.e., não está em repouso até o momento). Muitos resultados na termodinâmica clássica não são facilmente aplicados a sistemas em desequilíbrio (não em equilíbrio). No entanto, há vezes em que ocorrem os chamados estados quase-estacionários, onde o processo de difusão não muda no tempo, onde os resultados clássicos podem aplicar-se localmente. Como o nome sugere, este processo não é um verdadeiro equilíbrio dado que o sistema ainda está evoluindo.
Sistemas fluidos em desequilíbrio podem podem ser modelados com sucesso com a hidrodinâmica flutuante de Landau-Lifshitz. Neste quadro teórico, a difusão é devida às flutuações cujas dimensões variam de escala molecular à escala macroscópica.[2]
Difusão química aumenta a entropia do sistema (i.e., difusão é um processo espontâneo e irreversível). As partículas podem espalhar-se por difusão, mas não de forma espontânea reporganizar-se (ausência de alterações no sistema, assumindo que não há criação de novas ligações químicas, e de ausência de forças externas atuando sobre as partículas).
Um experimento para demonstrar difusão
[editar | editar código-fonte]A difusão não é fácil de se observar, porque outros fenômenos de transporte, especialmente a convecção, são mais eficientes em escalas de comprimento acima de milímetros. Difusão é mais importante em escalas microscópicas.
Difusão pode ser demonstrada com um tubo de vidro longo, papel, duas rolhas de cortiça, uma certa quantidade de algodão embebido em solução de amônia e alguns pedaços de papel de tornassol vermelho. Fixa-se o algodão numa das rolhas e diversos pedaços de papel harmoniosamente espaçados numa linha ou barbante preso na outra, por exemplo, com alfinetes. Arrolhando-se as duas extremidades do tubo de vidro com as rolhas e seus anexos, tomando-se o cuidado do fio com os papéis de tornassol se alongar pelo comprimento do tubo, e deitando o tubo na mesa (o que elimina a ação da gravidade), sem nenhuma agitação, pode-se observar que o papel de tornassol vermelho fica azulado.
Isto ocorre porque as moléculas de amônia viajam por difusão da extremidade com mais alta concentração no algodão para a extremidade de mais baixa concentração no restante do tubo de vidro. Isso não significa que as partículas não se movimentam em outras direções, mas há um fluxo líquido (em balanço) da região de concentração mais alta para a região de concentração mais baixa. Como a solução de amônia é alcalina, o papel tornassol vermelho torna-se azul. Pela alteração da concentração de amônia, a taxa de mudança da cor dos papéis de tornassol pode ser alterada. Note-se que a taxa de difusão em si não é aumentada, mesmo quando existe um gradiente de concentração mais acentuado, pois não é função da concentração. O que é realmente maior é o fluxo.
Difusão "coletiva" dependente da concentração
[editar | editar código-fonte]Difusão coletiva é a difusão de um grande número de partículas, mais frequentemente num solvente.
Ao contrário do movimento browniano, o qual é a difusão de uma única partícula, interseções entre partículas pode ter de ser considerada, a menos que as partículas formem uma mistura ideal com o seu solvente (condições de mistura ideal correspondem ao caso onde as interações entre o solvente e as partículas são idênticas às interações entre partículas e as interações entre as moléculas do solvente, neste caso, as partículas não interagem quando no interior do solvente).
No caso de uma mistura ideal, a equação de difusão da partícula mantém-se verdadeira e o coeficiente de difusão D, a velocidade de difusão na equação de difusão da partícula é independente da concentração da partícula. Em outros casos, resultando em interações entre partículas no solvente irão sofrer os seguintes efeitos:
- O coeficiente de difusão D, na equação de difusão da partícula torna-se dependente da concentração. Para uma interação atrativa entre as partículas, o coeficiente de difusão tende a diminuir à medida que aumenta a concentração. Para uma interação repulsiva entre as partículas, o coeficiente de difusão tende a aumentar à medida que aumenta a concentração.
- No caso de uma interação atrativa entre as partículas, as partículas apresentam uma tendência a se fundirem e formares clusters, se a sua concentração encontra-se acima de um certo limite. Isso é equivalente a uma reação química de precipitação (e se as partículas consideradas em difusão são moléculas químicas em solução, então é uma precipitação.
Difusão molecular de gases
[editar | editar código-fonte]Transporte de material em fluido estagnado ou através de linhas de fluxo de um fluido em fluxo laminar ocorre por difusão molecular. Dois compartimentos adjacentes, separados por partição contendo gases puros A e B, podem ser previstos. Movimento aleatório de todas as moléculas de modo a que, após um período, moléculas são encontradas distante das suas posições originais. Se a partição é removida, algumas moléculas de A movem-se em direção à região ocupada por B, passando por um plano O intermediário. O número de moléculas transportadas de A depende da ocupação de moléculas no ponto considerado. Simultaneamente, moléculas de B difundem-se para os regimes anteriormente ocupados por A puro.
Finalmente, a mistura completa ocorre. Antes deste ponto no tempo, uma variação gradual na concentração de A ocorre ao longo do eixo, designado x, o qual une os compartimentos originais. Esta variação, expressa matematicamente -dCA/dx, onde CA é a concentração de A. O sinal negativo surge porque a concentração de A diminui à medida que a distância x aumenta. Similarmente, a variação na concentração de gás B é -dCB/dx. A taxa de difusão de A, JA, depende do gradiente de concentração a a velocidade média com a qual as moléculas de A movem-se na direção x. Esta relação é expressa pela lei de Fick
O caminho teórico que nos leva à formulação dessa lei começa com as moléculas gasosas, que são de baixa densidade e monoatômicas. Imagina-se todas essas moléculas como pertencentes à mesma espécie química e com o mesmo tamanho, representado pelo diâmetro 'd'. Cada molécula possui uma energia cinética associada ao seu movimento de translação dentro do sistema gasoso, resultado das colisões entre elas com as paredes do recipiente.[3]
Ao se assumir que as moléculas no plano A só interagem com outras quando alcançam o plano O, pode-se entender que elas percorrem uma distância característica, representada por "λ", antes de colidirem com as moléculas no plano B.[3]
Como a Lei de Fick se dá nas três direções (x,y,z), a sua forma inteira é obtida a partir da análise do fluxo de matéria entre os planos.
Na intenção de se obter o fluxo de matéria na direção x, analisou-se as concentrações da espécie estudada (CA) nos planos A e B, e fez-se o limite de delta x tendendo a zero:[3]
Linearizando, encontra-se o parâmetro CA*:
Assim, obteve-se CA*, que é o parâmetro que indica a concentração de matéria a ser ganha no plano B ou perdida no plano A para que o sistema entre em equilíbrio termodinâmico.
Para se determinar a lei de Fick, é necessário entender como as moléculas se movem e interagem umas com as outras. Isso implica em analisar o comportamento das moléculas da espécie A em um plano específico. Para isso, pode-se adotar uma velocidade média Ω para essas moléculas devido à homogeneidade da população molecular. O fluxo líquido da espécie A através deste plano, na direção x positiva, é representado como JAI,x. Esse fluxo é determinado pelo produto da velocidade média das moléculas com a concentração de A no plano, CAI. Em um espaço tridimensional, as moléculas fluem livremente em todas as direções.
Chega-se na equação do DAA, que é a autodifusão. Em que pode ser substituída no fluxo difusivo:
Por fim, chega-se na equação do fluxo dada por:
No caso da difusão de um soluto gasoso A em um meio também gasoso B, a equação torna-se:
Esta equação é chamada de Primeira Lei de Fick. Nela, vê-se que o fluxo de difusão de A, JA,x, depende do gradiente de concentração e da velocidade média com a qual as moléculas de A movem-se na direção x. Tal como acontece com a equação básica de transferência de calor, a taxa de força é diretamente proporcional à força motriz, que é o gradiente de concentração.
Para situações onde a difusão ocorre predominantemente em uma direção, como em muitos processos de difusão em sistemas unidimensionais, utiliza-se uma simplificação, considerando apenas a direção x. A derivada dC/dx representa a taxa de variação da concentração C em relação à distância x. Em um sistema de difusão, a concentração de uma substância pode variar ao longo de uma determinada direção espacial, que é representada pelo eixo x neste caso. A derivada dC/dx nos diz como a concentração muda conforme nos movemos ao longo desse eixo.
Por exemplo, se tivermos uma concentração C que diminui à medida que nos afastamos de uma certa origem ao longo do eixo x, então a derivada dC/dx será negativa, pois a concentração está diminuindo com o aumento de x. Por outro lado, se a concentração aumenta com o aumento de x, então a derivada dC/dx será positiva.
Esta equação básica é aplicada a diversas situações. Restringindo-se o debate exclusivamente para o estado de equilíbrio, em que nem dCA/dx ou dCB/dx alteram-se com o tempo, a contradifusão equimolecular é considerada primeiro.
Vale ressaltar que para gases, a relação DBA = DAB se torna válida. Isso ocorre porque, em condições ideais, a difusão de um gás em outro é principalmente influenciada pelas colisões entre as moléculas dos gases envolvidos. Nessas condições, as moléculas de gás se movem livremente e se difundem umas nas outras de forma semelhante, resultando em uma relação simplificada entre os coeficientes de difusão.
No entanto, para líquidos, essa relação nem sempre é válida. A difusão em líquidos é influenciada por uma variedade de fatores, como a viscosidade do líquido, a polaridade das moléculas e as interações intermoleculares. Além disso, a estrutura molecular dos líquidos pode variar significativamente, o que pode levar a coeficientes de difusão binária diferentes dos coeficientes de difusão em meio gasoso.
Para o cálculo do coeficiente de difusão, pode-se utilizar de diferentes correlações levando em consideração diferentes fatores, O coeficiente de difusão para pares apolares A e B, considerando o potencial de Lennard Jones; as correlações de Chapman-Enskog, Wike e Lee; Fuller, Schetter e Giddings. Além disso, pode-se estimar o valor de um DAB a partir de outro DAB conhecido em outra temperatura e pressão.[4]
Além disso, o ideal é sempre pegar os valores de difusão tabelados, para evitar erros, mas caso não tenha o requerido, esse valor pode ser calculado.
Contradifusão equimolecular
[editar | editar código-fonte]Se nenhum fluxo massivo ocorre num elemento de comprimento dx (lembrando que trata-se de uma difusão, não de um deslocamento de massas de gás), as taxas de difusão de dois gases A e B devem ser iguais e opostas, o que é NA=NB.
A pressão parcial de A altera-se por dPA na distância dx. Similarmente, a pressão parcial de B altera-se dPB. Como não existe diferença na pressão total através do elemento (nenhum fluxo massivo, embora possa haver uma alteração de densidade, exatamente pela alteração de composição), dPA/dx deve igualar-se a -dPB/dx. Para um gás ideal a pressão parcial é relacionada à concentração molar pela relação
onde nA é o número de moles de gás A em um volume V. Como a concentração molar CA é igual a nA/V portanto
Consequentemente, para o gás A,
onde DAB é a difusividade de A em B. Similarmente,
Portanto, permite que DAB=DBA=D. Se a pressão parcial de A em x1 é PA1 e x2 é PA2, pode-se integrar a equação acima,
Um equação similar pode ser derivada da contradifusão do gás B.
Ver também
[editar | editar código-fonte]- Difusão facilitada
- Difusão simples
- Difusão turbulenta
- Osmose
- Escala de Batchelor
- Difusão ambipolar
- Difusão anômala
- Difusão de Bohm
- MRI de difusão
- Convecção difusiva dupla
- Arrasto
- Leis de Fick da difusão
- Tempo local (matemática)
- Transferência de massa
- Osmose
- Permeação
- Condução de calor relativística
- Fenômenos de transporte
- Viscosidade
- Dopante (química)
Referências
- ↑ Maton, Anthea; Jean Hopkins, Susan Johnson, David LaHart, Maryanna Quon Warner, Jill D. Wright (1997). Cells Building Blocks of Life. Upper Saddle River, New Jersey: Prentice Hall. pp. 66–67
- ↑ D. Brogioli and A. Vailati, Diffusive mass transfer by nonequilibrium fluctuations: Fick's law revisited, Phys. Rev. E 63, 012105/1-4 (2001)
- ↑ a b c Cremasco, Marco Aurélio (2016). Fundamentos de transferência de massa. [S.l.]: Editora Blucher
- ↑ Welty, James R. Fundamentos de Transferência de Momento, de Calor e de Massa. [S.l.: s.n.]
Bibliografia
[editar | editar código-fonte]- Maxwell, J. C.: Illustrations of the Dynamical Theory of Gases, Phil. Mag., 19, 19–32, 20,21–
37, 1860.
- Maxwell, J. C.: On the Dynamical Theory of Gases, Phil. Trans. R. Soc. London, 157, 49–88,
1867.
- Kestin, J.; Knierim, K.; Mason, E. A.; Najafi, B.; Ro, S. T.; Waldman, M.: Equilibrium and Transport Properties of the Noble Gases and Their Mixtures at Low Density, J. Phys. Chem. Ref. Data, 13, 229–303, 1984.
- Peter W. Atkins: Physikalische Chemie. Wiley-VCH, ISBN 3-527-30236-0.
- Reinecke, S.; Kremer, G. M.: Transport Coeficients for Monatomic Gases According to a Lennard-Jones 6-12 Potential, J. Non-Equilib. Thermodyn., 20, 183-189, 1995.
- E. L. Cussler: Diffusion – Mass Transfer in Fluid Systems. Cambridge University Press, Cambridge, New York 1997, ISBN 0-521-56477-8.
- J. Crank: The Mathematics of Diffusion. Oxford University Press, 1980, ISBN 0-19-853411-6.
- P. Heitjans, J. Kärger (Hrsg.): Diffusion in Condensed Matter – Methods, Materials, Models. Springer, Berlin 2005, ISBN 978-3-540-20043-7.
- W. Jost: Diffusion in solids, liquids, gases. 6. Auflage. Academic Press, New York 1970.
- H. J. V. Tyrell, K. R. Harris: Diffusion in Liquids. Butterworth, London 1984.
Ligações externas
[editar | editar código-fonte]- Diffusion - hyperphysics.phy-astr.gsu.edu (em inglês) - Algumas figuras que mostram a difusão e a osmose.
- Animation: How Diffusion Works - .mcgraw-hill.com (em inglês) - Uma animação descrevendo a difusão.
- Tristan S. Ursell; The Diffusion Equation - A Multi-dimensional Tutorial Department of Applied Physics, California Institute of Technology, Pasadena; October 2007. - www.rpgroup.caltech.edu (em inglês) - Um tutorial sobre a teoria e solução da equação de difusão.
- Johannes Kottonau; Simulation of Diffusion (Reaching a Dynamic Equilibrium Looking Like "Transport" of Particles) (em inglês) - Simulação de modelo NetLogo para uso educacional (Java Applet).
- Brownian Movement - www.composite-agency.com - Filme curto sobre movimento Browniano (inclui cálculo do coeficiente de difusão) (em inglês)
- Zoltán Erdélyi; Diffusion on the nanoscale - dragon.unideb.hu - Uma introdução básica à teoria clássica de difusão de volume (com figuras e animações) (em inglês)











