Bronze de sódio-tungsténio

O bronze de sódio-tungsténio é uma forma de composto de intercalação com fórmula NaxWO3, em que x é igual ou menor que 1. Assim designado devido ao seu brilho metálico, as suas propriedades elétricas vão de semicondutoras a metálicas dependendo da concentração de iões de sódio presentes; pode também exibir supercondutividade.
História[editar | editar código-fonte]
Preparado em 1823 pelo químico Friedrich Wöhler, o bronze de sódio-tungsténio foi o primeiro bronze de metal alcalino a ser descoberto.[1] Por causa da estabilidade relativa do catião tungsténio (V) que se forma, só na década de 1960 foram descobertos os bronzes de molibdénio.[2]
Propriedade[editar | editar código-fonte]
O bronze de sódio-tungsténio, como ouros bronzes de tungsténio, é resistente à reação química tanto em condições ácidas como alcalinas. A cor depende da proporção de sódio no composto, indo do dourado com x≈0,9, passando pelo vermelho, laranja e púrpura, até ao preto-azulado para x≈0,3.
A resistividade elétrica do bronze depende da proporção de sódio no composto, com resistências específicas de 1,66 mΩ medidas em algumas amostras.[3] Foi sugerido que os eletrões, libertados quando os átomos de sódio são ionizados, são prontamente conduzidos pelas orbitais t2g do tungsténio e π do oxigénio.[2] Tal pode ser observado nos espectros de XPS[4] and UPS:[5] o pico que representa a banda 5d do tungsténio torna-se mais intenso à medida que x aumenta.
Para valores de x abaixo de 0,3, o bronze é semicondutor em vez de metálico.[2] Quando arrefecido suficientemente, o bronze de sódio-tungsténio torna-se supercondutor, com temperatura crítica (Tc) para Na0,23WO3 de aproximadamente 2,2 K.[6] O primeiro registo de supercondutividade num bronze de tungsténio foi feito em 1964, com Tc de 0,57 K.[7]
Estrutura[editar | editar código-fonte]
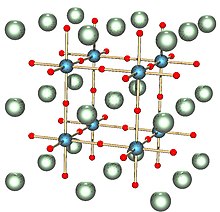
Quando x=1, o bronze de sódio-tungsténio adopta uma fase cúbica: a estrutura perovskite.[8] Nesta forma, a estrutura consiste de octaedros de WO6 partilhando vértices com iões de sódio nos espaços intersticiais. Para valores de x entre 0,9 e 0,3, a estrutura permanece semelhante mas com maior deficiência de iões de sódio e uma parâmetro de malha menor.[8]
Podem ser adoptados vários outros tipos de estruturas, com propriedades elétricas variáveis: as fases cúbica, tetragonal I e hexagonal são metálicas, enquanto as estruturas ortorrômbica e tetragonal II são semicondutoras.[9]
Síntese[editar | editar código-fonte]
A síntese feita por Wöhler em 1823, envolvia a redução de tungstato de sódio e trióxido de tungsténio com gás hidrogénio a temperatura elevada. Uma abordagem mais moderna reduz os reagentes fundidos com eletricidade em vez do hidrogénio.[10] Também é possível a síntese com micro-ondas,[11] usando pó de tungsténio como agente redutor.
Compostos relacionados[editar | editar código-fonte]
O sódio deste composto pode ser substituído por outros metais alcalinos para formar os seus bronzes de tungsténio, e por outros metais como o estanho e o chumbo.[12] Também existem bronzes de molibdénio mas são menos estáveis que os seus equivalente de tungsténio.[2]
Referências[editar | editar código-fonte]
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Sodium tungsten bronze», especificamente desta versão.
- ↑ Hagenmuller, P (1973). «Chapter 50: Tungsten bronzes, vanadium bronzes, and related compounds». Comprehensive Inorganic Chemistry. 4. [S.l.]: Pergamon. pp. 541–605. ISBN 978-0080169897
- ↑ a b c d Greenwood, N. N. & Earnshaw, A. (1993) [Reprint of corrected version of 1986, original version printed 1984]. Chemistry of the Elements 1st ed. [S.l.]: Pergamon Press. pp. 1185–6. ISBN 0-08-022057-6
- ↑ Straumanis, M. E.; A. (1 de fevereiro de 1949). «The Sodium Tungsten Bronzes. II. The Electrical Conductivity of the Bronzes». Journal of the American Chemical Society. 71 (2): 683-687. ISSN 0002-7863. doi:10.1021/ja01170a086
- ↑ West, Anthony (1984). Solid state chemistry and its applications. [S.l.]: Wiley. p. 96. ISBN 0-471-90874-6
- ↑ Cheetham, A K.; Day, P. (1987). Solid state chemistry: techniques. [S.l.]: Clarendon. p. 110. ISBN 0-19-855286-6
- ↑ Ostenson, J. E; H. R (1 de novembro de 1978). «Superconductivity in the tungsten bronzes». Journal of the Less Common Metals. 62: 149-153. doi:10.1016/0022-5088(78)90024-3
- ↑ Raub, Ch. J.; A. R. (21 de dezembro de 1964). «Superconductivity of Sodium Tungsten Bronzes». Physical Review Letters. 13 (25): 746-747. doi:10.1103/PhysRevLett.13.746
- ↑ a b HÄGG, GUNNAR (1 de janeiro de 1935). «The Spinels and the Cubic Sodium-Tungsten Bronzes as New Examples of Structures with Vacant Lattice Points». Nature. 135 (3421). doi:10.1038/135874b0
- ↑ Ngai, K L; T L (1 de janeiro de 1978). «Structural instabilities and superconductivity in the alkali tungsten bronzes». Journal of Physics F: Metal Physics. 8 (1). doi:10.1088/0305-4608/8/1/018
- ↑ Conroy, Lawrence E. (1 de janeiro de 1977). «The preparation and characterization of a sodium tungsten bronze. An inorganic experiment». Journal of Chemical Education. 54 (1). 45 páginas. ISSN 0021-9584. doi:10.1021/ed054p45
- ↑ Guo, Juan; Cheng (1 de janeiro de 2005). «A green route for microwave synthesis of sodium tungsten bronzes NaxWO3 (0». Journal of Solid State Chemistry. 178 (1): 58-63. doi:10.1016/j.jssc.2004.10.017
- ↑ Smart, Lesley E.; Moore, Elaine A. (2005). Solid State Chemistry: An Introduction 3rd ed. [S.l.]: CRC Press. p. 227. ISBN 0-7487-7516-1
