Iodato de sódio
| Iodato de sódio Alerta sobre risco à saúde | |
|---|---|
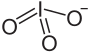
| |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | NaIO3 |
| Massa molar | 197.89 g/mol |
| Aparência | pó branco |
| Densidade | 4,28 g·cm-3[1] |
| Solubilidade em água | moderadamente solúvel (81 g·l-1 a 20 °C)[1] |
| Riscos associados | |
| NFPA 704 | |
| Frases R | R8, R22, R42/43 |
| Frases S | S2, S17, S22, S36/37, S45 |
| LD50 | 505 mg·kg-1 (camundongo, per os)[1] |
| Compostos relacionados | |
| Outros aniões/ânions | Iodeto de sódio Periodato de sódio Bromato de sódio Clorato de sódio |
| Outros catiões/cátions | Iodato de potássio Iodato de prata |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Iodato de sódio é um composto químico de fórmula NaIO3. É também um agente oxidante e, como tal, pode provocar incêndios se em contato com materiais combustíveis ou agentes redutores. Pode ser preparado através da reação de uma base contendo sódio, como o hidróxido de sódio, com o ácido iódico, por exemplo:
Pode também ser preparado através da adição de iodo a uma solução quente e concentrada de hidróxido de sódio.
3 I2 + 6 NaOH → NaIO3 + 5 NaI + 3 H2O
Condições/substâncias a serem evitadas são: calor, choque mecânico, fricção, materiais combustíveis, materiais redutores, alumínio, compostos orgânicos, carbono, peróxido de hidrogênio, sulfetos.

