Apoptose

A morte celular programada ou apoptose celular (do grego apoptosis, de apo - “de, desde” - e ptosis - “queda” -, numa referência à queda das folhas das árvores[1]) é imprescindível para o desenvolvimento dos animais. Nos tecidos de um ser humano saudável, a cada dia, bilhões de células (de um total de aproximadamente 37 trilhões e 200 bilhões de células) ativam um programa de morte intracelular, por mecanismos celulares complexos e variados. Esse processo mata as próprias células que o iniciam, ocorrendo de maneira controlada e ordenada - processo conhecido como morte celular programada. Nos anos de 1970, foi proposta a ideia de que existia um programa de morte embutido nas células animais. Tal proposta teve aceitação geral após 20 anos e dependeu de estudos genéticos que identificaram os primeiros genes envolvidos na morte celular programada - estudos realizados no nematodo Caenorhabditis elegans.
Em geral, a morte celular em animais ocorre por apoptose, sendo um dentre vários mecanismos de controle celular. Após modificações morfológicas características – como condensação e encolhimento, colapso do citoesqueleto, dissolução do envelope nuclear e fragmentação da cromatina –, células morrem por apoptose. Como a superfície da célula ou de seus pedaços – corpos apoptóticos – são alterados, os macrófagos rapidamente fagocitam tais estruturas. Entre as funções da apoptose, destaca-se a eliminação de células desnecessárias (ex.: degradação das membranas interdigitais) e/ou defeituosas.
Nem todas as células morrem por apoptose; portanto, o processo de apoptose não é sinônimo de morte celular. A morte celular pode ocorrer de várias maneiras, e uma delas é a apoptose, que é uma morte programada, também tratada como suicídio celular. Outra maneira muito frequente de morte celular é a necrose. Esta é uma morte acidental de células animais – processo chamado de necrose celular – , desencadeada após trauma, falta de suprimento sanguíneo, injúria aguda, dentre outras. As células necrosadas se expandem e sofrem lise, espalhando, assim, seu conteúdo nas vizinhas e acarretando uma resposta inflamatória, diferentemente da apoptose.
Processos fisiológicos e morfológicos similares à apoptose animal também ocorrem em plantas, durante o desenvolvimento (nas células do xilema) e na senescência de folhas e flores, bem como em interações com patógenos e parasitas e sob estresse ambiental, mas nas plantas não há fagocitose (o vacúolo em geral cumpre tal função) e nem caspases (proteínas exclusivas dos animais, explicadas a seguir nos Mecanismos Apoptóticos), e ainda não há consenso se os processos genéticos são os mesmos, já que os genes causadores podem ser outros; os genes se conservaram dos nematódeos aos humanos, entre os animais, mas parecem diferentes nos vegetais, que só produzem proteases distintas das caspases. Processos fisiológicos similares à apoptose animal ainda acontecem em organismos unicelulares, incluindo leveduras e bactérias.
Mecanismos Apoptóticos[editar | editar código-fonte]
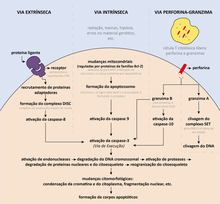
Os mecanismos da apoptose são extremamente complexos e sofisticados, envolvendo cascatas de eventos moleculares dependentes de energia. Há duas principais vias de sinalização da apoptose: a via extrínseca (ou via dos receptores de morte celular) e a via intrínseca (ou via da mitocôndria), e evidências recentes apontam que essas duas vias estão ligadas e que moléculas de uma delas podem influenciar na outra. Outra via mais recentemente descrita é a via perforina-granzima, que envolve células T citotóxicas. As vias de sinalização desencadeiam, então, a via de execução. Para melhor entender essas vias, algumas características bioquímicas da apoptose devem ser esclarecidas.[2][3]
Células em apoptose exibem muitas modificações bioquímicas, como clivagem de proteínas, degradação do DNA e reconhecimento fagocítico, por exemplo. Um dos principais conjuntos proteicos responsável pela apoptose é composto por caspases , que são proteases que têm uma cisteína em seu sítio ativo e clivam suas proteínas-alvo em ácidos aspárticos específicos, por isso têm esse nome (c para cisteína e asp para ácido aspártico).
As caspases são sintetizadas com precursores inativos, ou procaspases, que são ativadas por clivagem proteolítica. Algumas procaspases podem se agregar e autoativar. Uma vez ativadas, as caspases podem ativar outras procaspases, de forma que essa cascata proteolítica amplifica a via de sinalização da apoptose e leva a uma rápida morte celular. Uma vez que as caspases são inicialmente ativadas, o processo de morte celular programada parece se tornar irreversível.
As procaspases que atuam no início da cascata proteolítica são as iniciadoras (caspase-2,-8,-9,-10), que quando ativadas, clivam e ativam as executoras (caspase-3,-6,-7) e outras proteínas-alvo na célula. As caspases executoras atuam, por exemplo, na clivagem de lâminas nucleares, um processo irreversível. Ademais, essas proteínas ativam, de maneira indireta, endonucleases, que digerem o DNA no núcleo da célula. Outros alvos são os componentes do citoesqueleto e proteínas de adesão célula-célula. A cascata de caspases é um processo irreversível, destrutivo, autoamplificador e que apresenta duas vias principais de sinalização: via extrínseca e intrínseca, mas também pode ser ativada pela via perforina-granzima.
Via Extrínseca[editar | editar código-fonte]
O mecanismo da via extrínseca consiste na indução externa por associação de outra célula àquela que sofrerá apoptose. Essa interação ocorre por meio de receptores localizados na membrana celular e proteínas sinalizadoras (ou ligantes). Tais receptores são homotrímeros pertencentes à superfamília dos receptores de necrose tumoral (rTNF). Eles são compostos por um domínio extracelular rico em cisteína, que se associa ao ligante; um domínio transmembrana; e um "domínio de morte" intracelular, que tem o papel crucial de transmitir a sinalização de morte para as vias intracelulares. Os ligantes referidos também são homotrímeros e pertencentes à família TNF de proteínas sinalizadoras.
Um exemplo que ilustra esse mecanismo é a ativação de FasR pelo seu ligante FasL (similar também ao modelo TNF-α/TNFR1), que estimula os domínios de morte a recrutar proteínas adaptadoras intracelulares (FADD, no caso da ligação Fas, e TRADD no caso da ligação TNF) que, uma vez recrutadas, reúnem procaspases iniciadoras (procaspase-8, no caso da ligação Fas), formando o complexo de sinalização indutor de morte (DISC, death-inducing signaling complex). A partir desse complexo, os domínios “pro” das procaspases iniciadoras são clivados e essas proteínas, então, são dimerizadas, tornando-se ativas. Após esse processo, as caspases iniciadoras podem ativar as procaspases executoras ao clivar o domínio “pro” destas. A célula pode acionar ainda mecanismos intrínsecos a fim de amplificar a cascata de caspases e, assim, tornar a apoptose mais efetiva.
Algumas células apresentam maneiras de inibição e controle da via extrínseca. Ela pode ser inibida pela proteína c-FLIP, que se liga ao FADD e à caspase-8, intativando-as e impedindo que a cascata siga para a via de execução. Outra proteína, chamada Toso, também bloqueia a apoptose induzida por Fas em células T ao inibir a caspase-8.
Via Intrínseca[editar | editar código-fonte]
As vias intrínsecas de sinalização da apoptose envolvem diversos estímulos que produzem sinais intracelulares iniciados na mitocôndria que irão agir diretamente em alvos na célula. Esses estímulos podem ser separados em duas principais categorias: sinais positivos e sinais negativos. Sinais negativos são aqueles que estão relacionados com a perda da supressão da apoptose e subsequente ativação deste processo, como a ausência de certos fatores de crescimento, hormônios ou citocinas. Os sinais positivos são aqueles que induzem a apoptose, como radiação, toxinas, hipóxia, infecções virais, radicais livres, erros no material genético, etc.
Todos esses estímulos causam mudanças na membrana interna da mitocôndria, resultando na transição da permeabilidade mitocondrial (MPT - mitochondrial permeability transition) pela formação de um poro que leva à perda do potencial de transmembrana da mitocôndria e liberação de dois principais grupos de proteínas pro-apoptóticas intermembranais no citosol.
O primeiro grupo consiste de citocromo c, Smac/DIABLO e a protease HtrA2/Omi. Essas proteínas ativam as vias dependentes de caspases: o citocromo c se liga à e ativa Apaf-1 e a procaspase-9, formando um complexo chamado apoptossomo, que resulta na ativação da caspase-9; já as outras duas promovem a apoptose ao inibir a atividade de inibidores de proteínas da apoptose (IAP - Inhibitors of apoptosis proteins).
O segundo grupo de proteínas proapoptóticas AIF, endonuclease G, e CAD, são liberadas pela mitocôndria durante a apoptose somente após o processo se tornar irreversível (ou seja, quando a célula já está fadada a morrer) e estão relacionadas com processos de gramentação e condensação da cromatina.
Essa via é regulada pelas proteínas da família Bcl2 (extremamente conservada ao longo do caminho evolutivo humano), que a controla rigidamente para evitar que o processo apoptótico se inicie por acaso e o organismo perca uma célula saudável. As proteínas da família Bcl-2 controlam a permeabilidade da membrana mitocondrial e é composta por duas subfamílias: as proapoptóticas (que inclui Bcl-10, Bax, Bak, Bid, Bad, Bim, Bik e Blke) as antiapoptóticas (que inclui Bcl-2, Bcl-x, Bcl-XL, Bcl-XS, Bcl-w e BAG). A primeira subfamília é responsável por estimular o processo apoptótico permitindo a saída mais fácil do citocromo c para o citoplasma, além de outras proteínas mitocondriais intermembranares. Já a segunda família tem ação contrária, impedindo que as proteínas intermembranares sejam expulsas para o citosol.
O balanço entre as duas subfamílias proteicas é crucial para que o processo de apoptose não se inicie ao acaso, já que elas tem a capacidade de se auto-anular, interagindo entre elas mesmas, formando heterodímeros (proapoptótica + antiapoptótica = inatividade).
As proapoptóticas são subdivididas em duas subfamílias (BH123 e BH3-apenas). As proteínas BH3-apenas, sendo a maior subfamília da família Bcl2, são responsáveis pela inibição das antiapoptóticas e, algumas vezes, pela polimerização das Bak e Bax (proteínas proapoptóticas). São elas as primeiras proteínas ativadas com o sinal apoptótico, sendo que proporcionam a ativação e inativação das outras proteínas, de acordo com a necessidade celular de vida ou de morte. Elas, também, são responsáveis por fazer a conexão entre o sinal apoptótico e a via intrínseca da apoptose celular. No caso, por exemplo, de dano irreparável no DNA, o gene p53 (gene supressor de tumor codificador de uma proteína de 53kDa) produz uma proteína que se acumula e ativa as BH3-apenas Puma e Noxa, que disparam a via intrínseca da apoptose, impedindo a propagação do erro no material genético
Além disso, as BH3-apenas são as responsáveis por ligar o processo extrínseco com o intrínseco, já que, em alguns casos, o processo apoptótico extrínseco recruta o intrínseco para potencializar a cascata de ativação das caspases. A BH3-apenas responsável por esse link é a Bid.
Com a ativação dos receptores apoptóticos da superfície da membrana plasmática, ocorre a ativação da caspase 8 (caspase iniciadora), ela cliva a BH3-apenas Bid que adquire a forma tBid; esta forma vai em direção à membrana externa da mitocôndria e passa a realizar a inativação de proteínas Bcl2 antiapoptóticas, permitindo a oligomerização das proteínas BH123 e a consequente liberação do citocromo C para o citosol.
Quando, então, estímulos proapoptóticos são recebidos, as BH3-apenas estimulam as proteínas BH123 a formarem conglomerados proteicos na membrana externa da mitocôndria, permitindo a saída do citocromo C. As duas principais proteínas da subfamília BH123 são a Bax e Bak. Enquanto, na maior parte do tempo, a Bax fica dispersa no citosol e só se insere na membrana mitocondrial em casos de disparo apoptótico, a Bak está continuamente inserida nessa membrana (na face citosólica), de forma que, com o sinal, precisa apenas polimerizar-se e formar os poros para a passagem do citocromo. Algumas vezes, as Bak e Bax têm sua polimerização catalisada pelas BH3-apenas.
Já as antiapoptóticas (Bcl2 e Bcl-XL) estão localizadas na superfície citosólica da membrana mitocondrial externa e garantem a integridade da membrana, impedindo a formação de poros. Elas realizam sua função a partir da inativação de proteínas proapoptóticas, tanto na membrana mitocondrial, quanto no citosol. Assim, ao inativar as BH123, elas impedem a formação de poros e a saída do citocromo C, impedindo, consequentemente, o início da cascata apoptótica de ativação das caspases.
Não são apenas as proteínas Bcl2 que são responsáveis pela regulação intracelular da apoptose, sendo que proteínas inibidoras de apoptose (IAPs) também desempenham papel crucial nesse mecanismo.
Via perforina-granzima[editar | editar código-fonte]
Embora linfócitos T citotóxicos (CTLs) sejam capazes de matar células-alvo ativando a via extrínseca e a interação FasL/FasR seja o principal método de apoptose induzida por CTLs, existe uma outra via que permite que a apoptose seja ativada. Essa via envolve a secreção da molécula perforina, que forma poros na membrana celular, e a subsequente liberação exofítica de grânulos citoplasmáticos presentes nessas células T para o interior das células-alvo pelo poro criado. Esses grânulos são compostos principalmente de granzima A e granzima B.
A granzima B cliva proteínas a resíduos de aspartato e, dessa maneira, ativa a procaspase-10 e cliva fatores como ICAD (Inibidor da DNAse Ativada por Caspase). A caspase-10 então é capaz de ativar a caspase-3, iniciando a via de execução. No entanto, a granzima B também pode ativar diretamente a caspase-3. Desta forma, há indução direta da via de execução da apoptose. Esta via se mostra extremamente importante para o controle da expansão de células Th2, enquanto a típica interação FasL/FasR está relacionada com a regulação de células Th1.
A granzima A também é importante para esse processo e ativa uma via independente de caspases. Uma vez na célula, a granzima A cliva o complexo SET, que normalmente inibe o gene NM23-H1, um gene supressor de tumor. Sem o complexo SET, NM23-HI deixa de ser inibido, o que resulta em degradação apoptótica do DNA.
Via de Execução[editar | editar código-fonte]
Tanto as vias extrínseca, intrínseca e parte da via perforina-granzina levam à via de execução, considerada a via final da apoptose. Essa fase é iniciada com a ativação das caspases executoras (caspase-3,-6,-7), que ativam endonucleases citoplasmáticas, degradando o material nuclear, e proteases que degradam proteínas nucleares e citoplasmáticas.
A caspase-3 é considerada a mais importante caspase executora, sendo iniciada por diversas caspases iniciadoras (caspase-8,-9,-10). Essa caspase ativa a endonuclease CAD, que em células normais é associada ao seu inibidor ICAD, a caspase-3 cliva ICAD, de forma que CAD passa a degradar o DNA cromossomal dentro do núcleo e condensa a cromatina. Ela também induz reorganização do citoesqueleto e desintegração da célula em corpos apoptóticos.
Mecanismos Inibidores da Apoptose[editar | editar código-fonte]
IAPs, primeiramente identificadas em vírus de insetos (baculovírus) — animais nos quais a atuação de IAPs é bem observada e descrita —, possuem um ou mais domínios BIR, que permitem a ligação delas em caspases ativadas e suas consequentes inibições. Algumas IAPs também fazem a poliubiquitinação das caspases, marcando-as para destruição pelos proteossomos. Assim, pode-se dizer que as IAPs determinam um limiar de inibição que deve ser cruzado por caspases ativadas para disparar a apoptose.[2]
Em Drosophila, a barreira inibitória criada pelas IAPs pode ser neutralizada por proteínas antiIAP, produzidas em resposta a estímulos apoptóticos. Em moscas, existem cinco antiIAPs, nos quais estão inclusos: Reaper, Grim e Hid. Possuem similaridade estrutural em seus motivos N-terminais de ligação a IAP, que se ligam ao domínio BIR e impedem sua ligação a uma caspase. A deleção dos genes codificantes de Reaper, Grim e Hid bloqueia a apoptose em moscas. Entretanto, a inativação de um dos dois genes que codificam IAPs em Drosophila faz com que todas as células do embrião da mosca em desenvolvimento entrem em apoptose. Por isso, o balanço entre IAPs e antiIAPs é firmemente regulado e crucial para o controle da apoptose em moscas.
Em mamíferos, a função de proteínas antiIAP, na apoptose, é controverso. Quando a via intrínseca da apoptose é ativada, antiIAPs são liberadas do espaço intermembranas da mitocôndria para o citosol quando a via intrínseca da apoptose é ativada, bloqueando IAPs e promovendo a apoptose. Contudo, quando os genes que codificam duas antiIAPs conhecidas de mamíferos (chamadas de Smac ou DIABLO e Omi) são inativadas em células de camundongos, a apoptose aparentemente não é afetada - por isso a controvérsia sobre seus papéis em sua regulação.
Assim, as atividades combinadas de proteínas Bcl2, IAPs e antiIAPs determinam como uma célula animal reage aos estímulos indutores de apoptose — com a predominância de IAPs e antiIAPs em moscas e de proteínas Bcl2 em mamíferos.
Causas da Apoptose[editar | editar código-fonte]
Apoptose por Estímulos Fisiológicos[editar | editar código-fonte]
A apoptose é um mecanismo útil para manter o equilíbrio interno dos organismos multicelulares e pode ocorrer fisiologicamente em humanos em alguns casos, como:
- No desenvolvimento embrionário, várias estruturas do feto (como o ducto tireoglosso e a notocorda) sofrem involução ao longo do período gestacional. Esta involução deve-se à morte programada das células que compõem estas estruturas.[4]
- Em casos de corte no suprimento de hormônios estimulatórios. Ocorre fisiologicamente durante a menopausa, período no qual os tecidos endometrial e mamário sofrem atrofia devido à queda nos níveis séricos dos hormônios sexuais femininos. Caso o estímulo hormonal não seja retomado, a atrofia não será reversível e as células destes tecidos entrarão em apoptose.[5]
- Renovação de células lábeis localizadas em tecidos cujas células se renovam constantemente. Este é o caso do epitélio que reveste a pele. As células basais multiplicam-se constantemente com o objetivo de substituir as células envelhecidas que estão nos extratos apicais do tecido. As células mais velhas, por sua vez, sofrem apoptose para que o número celular no tecido continue constante.[6]
- Apoptose estimulada pelo linfócito T citotóxico. Nestes casos a apoptose ocorre quando uma célula do organismo é infectada por um vírus e passa a apresentar antígenos dele em sua membrana (via complexo de histocompatibilidade tipo 1, ou MHC-1). As células T citotóxicas reconhecerão este antígeno e induzirão a apoptose na célula infectada, sendo este processo muito importante na eliminação de vírus do organismo e também na geração de sintomas em várias patologias.[7]
- Após uma resposta imunológica do indivíduo a um agente biológico, é preciso que haja eliminação da superpopulação de leucócitos que foram usados na defesa do organismo. O mecanismo para essa eliminação é a apoptose.
- Nas células fibrosas que darão origem ao cristalino. Essas células sofrerão apoptose nuclear (apenas o núcleo é destruído), enquanto o citoplasma permanece intacto.[4]
Apoptose por Causas Patológicas[editar | editar código-fonte]
- Indução à apoptose por lesão do material genético celular,[8] que pode ser causada por estímulos radioativos, químicos ou virais. Quando a lesão causada ao DNA é maior que a capacidade da célula de revertê-la, é mais seguro para o organismo que o programa de morte celular seja ativado, já que a multiplicação de uma célula mutante pode dar origem a neoplasias.
- Lesão por isquemia ou hipóxia moderadas podem levar as células de determinado tecido, tanto à necrose, quanto à apoptose. Muitos estímulos à morte celular por necrose também desencadeiam morte celular por apoptose.[7]
Mudanças Morfológicas na Célula Apoptótica[editar | editar código-fonte]

Algumas mudanças só podem ser vistas quando a célula é analisada em microscopia eletrônica, mas, de maneira geral, os fenômenos que culminam com a morte celular programada são:
- Diminuição da célula com agregação dos componentes celulares, deixando a célula bastante eosinofílica;
- O núcleo celular muda de aspecto, a cromatina se prende à carioteca e toma um aspecto mais denso[9] (condensação). Além disso pode ocorrer a fragmentação do núcleo (cariorréxis);
- Formam-se bolhas de citoplasma partindo da membrana plasmática celular, que se desprendem e formam corpos apoptóticos. Eles serão, então, reconhecidos e fagocitados por macrófagos. Alguns destes corpos apoptóticos podem conter fragmentos de material genético.[10]
Funções[editar | editar código-fonte]
A apoptose é responsável, por exemplo, por delinear nosso desenho anatômico durante o desenvolvimento intrauterino. Especialmente nesse caso é interessante o fato de não haver resposta inflamatória, pois como o corpo da mãe está trabalhando sob condições de imunossupressão – a fim de não expulsar o corpo estranho que se instalou no endométrio –, gerar a ação do sistema imune para responder a fatores pró-inflamatórios poderia acarretar em perda do embrião ou feto.[2][11]
O tamanho de órgãos também pode ser assim controlado. O equilíbrio entre a taxa de divisão celular e a de apoptose atuam de maneira bastante precisa nesses casos, como quando a ingestão de uma droga promove divisão celular e o fígado aumentado retorna ao seu tamanho original por apoptose, fato já observado em ratos. Ela também ocorre frequentemente na medula óssea humana em que é necessário manter um estoque de células prontas para serem utilizadas a qualquer momento, fato esse que acontece, a saber, com os neutrófilos. Também está relacionada à destruição do endométrio durante a menstruação e à degradação das criptas nas células do epitélio intestinal.
A apoptose também pode ocorrer quando há identificação de organelas que não estejam funcionando de forma adequada. A célula optará em realizar apoptose para eliminar problemas de acordo com sua extensão e gravidade, já que, em alguns contextos, é possível que uma autofagia específica resolva a situação. Um caso clássico está relacionado ao fato de surgirem mutações desfavoráveis no material genético que podem culminar em câncer.
Nesse contexto, dentre vários mecanismos, pode haver o envio de sinalização para o citoplasma a partir do gene p53, o qual participa do controle da divisão celular. Assim, uma molécula inativa a proteína Bcl2, que está situada e ativa na membrana das mitocôndrias, dando início à indução de apoptose por meio da via intrínseca.
Durante o desenvolvimento, a apoptose pode realizar algumas funções básicas, como: esculpir e eliminar estruturas, regular a quantidade de células e eliminar células defeituosas.[12]
Esculpir estruturas[editar | editar código-fonte]
A apoptose tem papel fundamental na organogênese e no remodelamento de tecidos.[12] Abaixo estão alguns exemplos desta função da apoptose:
- Formação de dígitos
- Durante o desenvolvimento de camundongos, os dígitos já começam a se formar unidos por meio de membranas interdigitais. Essas membranas são, então, gradualmente eliminadas ao longo dos estágios seguintes.[13] Contudo, em camundongos knock-out para o gene da proteína Bak, as membranas interdigitais foram mantidas em todas as patas na fase adulta,[14] revelando a necessidade da apoptose no processo de formação dos dígitos livres.
- Formação de tubos e cavidades
- A formação de tubos e cavidades durante o desenvolvimento, geralmente se dá, ou pelo enrolamento de uma camada epitelial já estabelecida, ou pela criação de uma cavidade em um estroma celular.[15] No último caso, o processo se da por meio de apoptose. Algumas evidências comprovam presença da apoptose, nestes processos, como: a presença de células apoptóticas, tanto durante a formação de cavidades em corpos embrióides, quanto durante a formação da cavidade pré-amniótica em embriões de camundongos e ratos no desenvolvimento;[15] e o não fechamento do tubo neural em embriões de galinha quando estes são tratados com inibidores de caspases.[16]
- Modelamento de órgãos
- A apoptose também auxilia no modelamento de outros órgãos durante o desenvolvimento, como a orelha interna e o coração, por exemplo. No caso do desenvolvimento da orelha interna de galinha, é sugerido que a apoptose ajuda, não somente na formação do padrão celular de células ciliadas e de células de suporte, como também na formação do labirinto, durante os estágios iniciais do desenvolvimento [17]. Quanto ao coração, a apoptose auxilia na regulação do tamanho e da forma da almofada cardíaca no embrião, sendo importante, junto com os processos de proliferação e diferenciação celular, para a formação das câmaras do coração.[18]
Eliminação de estruturas[editar | editar código-fonte]
Ao longo do desenvolvimento, várias estruturas temporárias são formadas e depois eliminadas por meio de apoptose quando não mais necessárias, como estruturas juvenis ou estruturas restritas a apenas um dos sexos.[12] Um exemplo clássico desse processo ocorre durante a metamorfose de sapos, evento em que há aumento na taxa do hormônio tiroxina (T3), estimulando a apoptose nas células da cauda e, consequentemente, ajudando na reabsorção da estrutura.[19] Pode-se citar também a metamorfose em insetos, evento em que há eliminação de grande parte dos tecidos larvais – como as glândulas salivares, o trato digestivo e o sistema nervoso[20] –, por meio de apoptose regulada por esteroides, para dar lugar aos tecidos adultos.[21] Outro exemplo da apoptose sendo empregada na eliminação de estruturas envolve os ductos de Müller e os ductos de Wolff. O primeiro é responsável pela formação dos ovidutos e do útero em fêmeas, sendo, portanto, eliminados em machos, enquanto que o segundo forma o ducto deferente, o epidídimo e a vesícula seminal em machos, sendo, portanto, degenerados em fêmeas.[22]
Regulação da quantidade de células[editar | editar código-fonte]
A quantidade de células no organismo é resultado de um balanço entre a proliferação celular e a morte celular.[12]. Alguns órgãos, como os do sistema nervoso e do sistema reprodutivo, possuem um excesso de células que é, posteriormente, eliminado. No caso de ovários em fetos, existem cerca de 250.000 células germinativas durante o 5º mês de gravidez, antes de começar a oogênese [23]. Contudo, eventos de apoptose durante o paquíteno da meiose I e a formação dos folículos primordiais[24] acabam por reduzir este número a menos de 20% antes do nascimento[23]. Já no caso do sistema nervoso, pode-se citar o nervo óptico, em que mais da metade dos oligodendrócitos formados sofrem apoptose de dois a três dias após a sua formação[25], ajudando a balancear o número de oligodendrócitos com o número de axônios com os quais podem interagir[26]
Eliminação de células defeituosas[editar | editar código-fonte]
Células anormais podem ser potencialmente perigosas para o organismo, independentemente do estágio do desenvolvimento.[12] Entre os mecanismos básicos de proteção, está a apoptose.
Um exemplo clássico da proteção oferecida pela apoptose está na seleção de linfócitos B e T funcionais. Durante a seleção positiva, linfócitos B e T que não expressam receptores de células B e receptores de células B funcionais, respectivamente, não recebem os sinais necessários para evitar a apoptose [27]. Passando para a seleção negativa, linfócitos cujos receptores de antígenos interagem contra autoantígenos (oferecendo, portanto, o risco de desencadear uma resposta autoimune) são estimulados a entrar em apoptose[28]. Outro exemplo importante de proteção por apoptose consiste na eliminação de células com danos ao DNA que, por algum motivo (seja pelo número excessivo de danos ao DNA, por defeitos nos sistema de reparo ou por outras razões), não foram reparados e que apresentam o potencial risco de se tornarem células cancerosas [29][30].
Consequências na Desregulação da Taxa de Apoptose[editar | editar código-fonte]
A apoptose excessiva[editar | editar código-fonte]
O excesso de atividade apoptótica, causado por diferentes adversidades que atingem os mecanismos regulatórios, causa danos severos em alguns tecidos devido à morte em demasia de células. Por exemplo, em casos de derrame e ataque do coração, um grande número de células morre por necrose devido à isquemia (diminuição da irrigação sanguínea). Nestes casos, é desencadeada reação inflamatória e há liberação do conteúdo celular, apesar de uma pequena parte das células morrer por apoptose (no caso, aquelas menos afetadas pela limitação de suprimento sanguíneo). Assim, acredita-se no desenvolvimento futuro de alguns fármacos que bloqueiem a apoptose e, dessa forma, possam preservar estas células (como inibidores de caspases).[2]
Outra enfermidade associada à apoptose excessiva é a AIDS (síndrome da imunodeficiência adquirida). Acredita-se que o vírus HIV (vírus da imunodeficiência humana), causador desta doença, possa induzir a apoptose de linfócitos T auxiliadores, ou CD4 (relacionados a respostas imunes). Contudo, essa indução não se dá somente nas células infectadas diretamente, isso ocorre devido a um produto viral solúvel (gp120) capaz de se ligar ao domínio CD4 das células não infectadas. Esse mecanismo indireto potencializa ainda mais a derrocada do sistema imune. É justamente a diminuição do número de linfócitos T que provoca danos na resposta imunológica dos soropositivos, tornando-os extremamente susceptíveis a complicações.
Há também as doenças neurodegenerativas, nas quais a apoptose é induzida em neurônios ou células neuronais. Na esclerose lateral amiotrófica (ELA), a enzima superóxido-dismutase, de efeito antioxidante, tem sua produção comprometida devido a mutações no gene que a codifica. Assim, os radicais livres não são metabolizados pelos neurônios motores e seu acúmulo induz a apoptose neuronal, devido à agressão química provocada por estas substâncias nas células. Na doença de Alzheimer, há o acúmulo de peptídio-β-amilóide, que influencia os processos metabólicos celulares e também induz a morte celular programada. Já nas atrofias musculares espinhais, o problema decorre de mutações no gene que codifica as IAPs, logo, o processo torna-se facilitado, uma vez que elas não se ligarão às caspases, que estarão ativas, promovendo a apoptose.
Por fim, a apoptose exagerada também causa distúrbios na produção de células sanguíneas. Isso ocorre pois, normalmente, o processo de morte celular é inibido nestas células para que possa ocorrer a sua diferenciação. Dessa forma, o acúmulo de toxinas ou mutações que ativem genes indutores de apoptose levam a doenças hematológicas, como neutropenia crônica (baixa produção de neutrófilos), anemia aplástica (redução da fabricação de células sanguíneas em geral) ou β-talassemia (problemas na produção de hemoglobina).
Apoptose reduzida[editar | editar código-fonte]
O processo de morte celular controlada é importante para eliminar células velhas, danificadas ou que apresentem riscos ao sistema corporal como um todo. Apesar de seus malefícios quando acionado demasiadamente, a falta deste mecanismo biológico também traz sérias consequências.
Uma das mais importantes consequências é a contribuição no desenvolvimento do câncer. Assim, neste tipo de doença, somado ao fato de haver um incremento da multiplicação celular, há também uma inibição da apoptose em células cancerígenas de tumores malignos, que podem se espalhar pelo corpo e desfrutar de uma vantagem seletiva, já que não sofrem apoptose. Isso decorre do fato de alguns oncogenes (aqueles cujo ganho de função leva à proliferação celular) e genes supressores de tumor (a perda de função induz a multiplicação das células) estarem intimamente relacionados ao processo de morte celular programada. Um exemplo são os oncogenes do Bcl2 e Bcl-XL, que participam do bloqueio da apoptose. Mutações no gene que codifica a p53 (um supressor de tumor) estão associadas a cerca de 50% dos casos de câncer, já que esta proteína é um regulador do ciclo celular que induz a morte celular em casos de erros. Dessa forma, a inibição da apoptose influi no processo de proteção celular contra falhas ocasionais, contribuindo para o surgimento de tumores malignos. As doenças autoimunes também se enquadram neste quesito.
O sistema imunológico precisa ser bastante dinâmico e diversificado para poder atuar contra diferentes antígenos recebidos ao longo da vida. Assim, rearranjos no DNA são frequentemente necessários. Contudo, este processo pode desencadear falhas, como células que combatem antígenos do próprio organismo. Para que o quadro de doença autoimune não se instale, a apoptose é necessária para eliminar estes linfócitos que atacam o próprio sistema. Todavia, caso haja intercorrências na morte celular, os linfócitos defeituosos passarão por um amadurecimento inadequado no timo, já que não serão eliminados e, consequentemente, trarão injúrias ao organismo. O mecanismo de apoptose inibida, neste caso, relaciona-se com mutações em genes que codificam a proteína Fas ou o ligante Fas.
Por fim, alguns tipos de vírus desenvolveram estratégias para evitar a apoptose nas células infectadas. Por exemplo, o vírus da varíola bovina consegue inibir a ICE (enzima conversora de interleucina-1), que é um tipo de caspase. Há patógenos que codificam proteínas semelhantes ao Bcl2 ou que elevam a sua expressão como inibidores de apoptose (vírus Epstein-Barr e o da peste suína africana). Os baculovírus agem por meio de IAPs, que se ligam às caspases impedindo-as de desencadear a morte celular programada.
Possíveis Aplicações[editar | editar código-fonte]
A apoptose possui potencial uso terapêutico, pois sua modulação pode ser utilizada para tratamento de doenças. Diversos estudos nesse sentido buscam alternativas para atuar em problemas como o câncer, usando também outras ferramentas biológicas como micro-RNAs. No estudo “Role of micro-RNAs in drug resistance of multiple myeloma”, há uma série de observações que embasam essa aplicação. Neste contexto, os micro-RNAs mais estudados são: miR-137/197, miR-21 e miR-221/222. Acredita-se que eles estejam relacionados com uma modulação negativa da sensibilidade às drogas pelas células de mieloma múltiplo.
Micro-RNAs (miRNAs) são pequenas moléculas de RNA não codificantes que têm papel na regulação pós-transcricional de alguns genes humanos, como oncogenes e supressores de tumor (essa regulação pode ter caráter positivo ou negativo). Eles também podem regular a resposta de células tumorais a drogas através da modulação dos processos de apoptose, anti-apoptose ou de vias proliferativas. Contudo, o estudo destas modulações é desafiador, visto que o processo de resistência ao tratamento é bastante complicado, somando-se ao fato de que alguns miRNAs têm a capacidade de atingir, pelo menos, 200 genes diferentes.
Referências
- ↑ «apoptose | Palavras | Origem Da Palavra». origemdapalavra.com.br. Consultado em 1 de dezembro de 2016. Arquivado do original em 2 de dezembro de 2016
- ↑ a b c d Alberts, Bruce (2010). Biologia Molecular da Célula. [S.l.]: Artmed. pp. 1115–1127
- ↑ Elmore, Susan (2007). «Apoptosis: A Review of Programmed Cell Death». Toxicologic pathology. 35 (4): 495–516. ISSN 0192-6233. PMC 2117903
 . PMID 17562483. doi:10.1080/01926230701320337
. PMID 17562483. doi:10.1080/01926230701320337
- ↑ a b Apoptose 1: papel no desenvolvimento embrionário[ligação inativa] Obtido em 15 de agosto de 2009 (em português)
- ↑ 2. Fisiopatologia Arquivado em 19 de novembro de 2008, no Wayback Machine. Obtido em 15 de agosto de 2009 (em português)
- ↑ Neoplasias epiteliais de preenchimento[ligação inativa] Obtido em 15 de agosto de 2009 (em português)
- ↑ a b Apoptose Obtido em 15 de agosto de 2009 (em português)
- ↑ Mecanismos de indução de apoptose pela presença de danos ao DNA: um estudo sobre... Obtido em 15 de agosto de 2009 (em português)
- ↑ Neupatimagem-UNICAMP Obtido em 15 de agosto de 2009 (em português)
- ↑ Arquivos de Gastroenterologia - Apoptosis as a mechanism of tissue injury in hepatobiliary diseases Obtido em 15 de agosto de 2009 (em português)
- ↑ Abdi, Jahangir; Hou (2 de agosto de 2016). «Role of micro-RNAs in drug resistance of multiple myeloma». Oncotarget. 7 (37). ISSN 1949-2553. doi:10.18632/oncotarget.11032
- ↑ a b c d e Yaron Fuchs; Hermann Steller (11 de novembro de 2011). «Programmed Cell Death in Animal Development and Disease». Cell. 147 (4): 742-758. doi:10.1016/j.cell.2011.10.033
- ↑ «emouseatlas»
- ↑ Tullia Lindsten; Tullia Lindsten, Wei-Xing Zong, Helena A. Shiels, Patryce Mahar, Michael Wei, Andrea J. Ross, Jeffrey C. Rathmell, Eugen Ulrich, Kenneth Frauwirth, Vicki M. Eng, M. Celeste Simon, Averil Ma, Ayala King, Katrina G. Waymire, Yifeng Chen, David M. Adelman, Jeffrey A. Golden, Gerard Evan, Stanley J., Korsmeyer, Grant R. MacGregor,Craig B. Thompson (dezembro de 2000). «The Combined Functions of Proapoptotic Bcl-2 Family Members Bak and Bax Are Essential for Normal Development of Multiple Tissues». Molecular Cell. 6 (6): 1389-1399
- ↑ a b Electra Coucouvanis; Gail R. Martin (20 de outubro de 1995). «Signals for Death and Survival: A Two-Step Mechanism for Cavitation in the Vertebrate Embryo». Cell. 83 (2): 279-287
- ↑ Miguel Weil; Michael D. Jacobson and Martin C. Raff (fevereiro de 1997). «Is programmed cell death required for neural tube closure?». Current Biology. 7 (4): 281-284
- ↑ B. Avallone; G. Balsamo, S. Trapani, and F. Marmo (2002). «Apoptosis during chick inner ear development: some observations by TEM and TUNEL techniques». European Journal of Histochemistry. 46 (1): 53-59
- ↑ ELTYEB ABDELWAHID; LAURI J. PELLINIEMI, EERO JOKINEN (2002). «Cell Death and Differentiation in the Development of the Endocardial Cushion of the Embryonic Heart». MICROSCOPY RESEARCH AND TECHNIQUE. 58 (5): 395–403
- ↑ J. F. R. KERR; B. HARMON, J. SEARLE (1974). «AN ELECTRON-MICROSCOPE STUDY OF CELL DELETION IN THE ANURAN TADPOLE TAIL DURING SPONTANEOUS METAMORPHOSIS WITH SPECIAL REFERENCE TO APOPTOSIS OF STRIATED MUSCLE FIBRES». Journal of Cell Science. 16 (3): 571-585
- ↑ Restifo, L. L.; White, K. (1992). «Mutations in a steroid hormone-regulated gene disrupt the metamorphosis of internal tissues in Drosophila: salivary glands, muscle, and gut». Developmental Biology. 201 (4): 221-234
- ↑ Baehrecke, E. H. (2000). «Steroid regulation of programmed cell death during Drosophila development». Cell Death and Differentiation. 7: 1057-1062
- ↑ Pascal Meier; Andrew Finch, Gerard Evan (2000). «Apoptosis in development». Nature. 407: 796-801
- ↑ a b Baker, T.G. (1963). «A quantitative and cytological study of germ cells in human ovaries». Proceedings of the Royal Society B: Biological Sciences. 158: 417-433
- ↑ Gondos, B. (1978). The vertebrate ovary (Oogonia and oocytes in mammals) 1 ed. New York: Plenum Press. p. 653-663
- ↑ Martin C. Raff; Barbara A. Barres, Julia F. Burne, Harriet S. Coles, Ysuki Ishizaki, Michael D. Jacobson (1993). «Programmed Cell Death and the Control of Cell Survival: Lessons from the Nervous System». Science. 262: 695-700
- ↑ Ben A. Barres; Martin C. Raff (1999). «Axonal Control of Oligodendrocyte Development». The Journal of Cell Biology. 147 (6): 1123–1128
- ↑ Jameson, S.C.; Hogquist, K.A. & Bevan (1995). «Positive selection of thymocytes». Annual Review of Immunology. 13: 93–126
- ↑ Ashton-Rickardt, P.G; Tonegawa, S. A (1994). «A differential-avidity model for T-cell selection». ImmunologyToday. 15: 362–366
- ↑ Kastan, M. B.; Bartek, J. (2004). «Cell-cycle checkpoints and cancer». Nature. 432: 316–323
- ↑ Marcos Malumbres; Mariano Barbacid (2009). «Cell cycle, CDKs and cancer: a changing paradigm». 9: 153-166

