Anti-inflamatórios não esteroides

Os anti-inflamatórios não esteroides (abreviadamente, AINEs ou NSAIDs, do inglês Non-steroidal anti-inflammatory drugs) são um grupo variado de fármacos que têm em comum a capacidade de controlar a inflamação, de analgesia (reduzir a dor), e de combater a febre. O termo foi criado em 1960 por Michael W. Whitehouse.[1] Apesar de em sua maioria serem constituídos por ácidos orgânicos, sua estrutura química não é relacionada. Caracterizam-se por inibir a atividade de subtipos da ciclo-oxigenase, impedindo assim a síntese de eicosanoides pela via metabólica da cascata do ácido araquidónico. Fazem parte deste grupo medicamentos muito conhecidos, em parte por alguns já estarem disponíveis há muito tempo, por serem de venda livre (MNSRM), e pelo vasto número de situações em que são usados. Alguns nomes sonantes incluem o ácido acetilsalicílico, ibuprofeno e naproxeno. O paracetamol, embora possua um mecanismo de ação semelhante e tenha efeito antipirético e analgésico,[2] é praticamente desprovido de efeito anti-inflamatório.
Classificação química[editar | editar código-fonte]
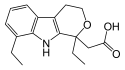
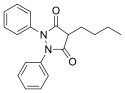
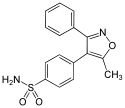
Existem diversos modos de classificar os AINE, por potência inibidora de COX-2 sobre COX-1, concentração para atingir efeitos clínicos, etc. Abaixo, estão classificados de acordo com sua estrutura química:
Mecanismo ação[editar | editar código-fonte]
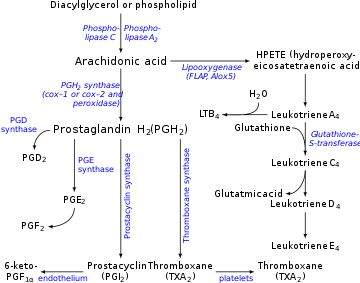
Os AINEs são inibidores específicos da enzima ciclooxigenase (COX). A COX possui duas formas ligeiramente diferentes, designadas COX-1 e COX-2. Estas são importantíssimas na cascata do ácido araquidónico, pois transformam o ácido araquidônico, uma substância formada a partir de lípidos presentes na membrana celular pela acção da fosfolípase A2, em dois tipos de compostos, as prostaglandinas e os tromboxanos.[4] O papel destes mediadores na inflamação e na dor, assim como em vários outros processos fisiológicos (como na coagulação), é amplamente aceite.[3] No início da década de 1990, a descoberta dos dois subtipos de COX criou expectativas quanto à criação de novos fármacos que mantivessem as propriedades dos AINEs existentes e permitissem diminuir a incidência de efeitos colaterais. A diferente distribuição dos subtipos de COX levou a que fosse colocada a hipótese de que a COX-1 seria "constitutiva", ou seja, estaria sempre presente no corpo e era responsável por funções fisiológicas importantes, e que a COX-2 seria "induzida", surgindo na resposta inflamatória. Desta forma, os efeitos colaterais dos AINEs dever-se-iam à inibição da COX-1.[5] Com o aparecimento de fármacos que inibem especificamente a COX-2, designados por coxibs (o primeiro fármaco deste grupo foi o celecoxib), foi possível constatar uma quase completa redução dos efeitos colaterais a nível gastrointestinal. Contudo, alguns estudos vieram colocar em causa o fundamento desta abordagem, ao demonstrar que a COX-2 também desempenhava um papel fisiológico (protector) importante tanto no estômago como no rim.[6] A inibição destas enzimas pelos AINE na redução da febre ou efeito antipirético é causada pela inibição da formação de prostaglandina E2 pela COX-1. Esta prostaglandina é um mediador importante para a ativação do centro nervoso (no hipotálamo), regulador da temperatura corporal. Altos níveis de prostaglandina E2 em estados inflamatórios (como infecções) elevam a temperatura. O efeito analgésico é devido à inibição da produção local de prostaglandinas aquando da inflamação. Estas prostaglandinas, se forem produzidas, vão sensibilizar as terminações nervosas locais da dor, que será iniciada por outros mediadores inflamatórios como a bradicinina. Os efeitos anti-inflamatórios também estão largamente dependentes da inibição da produção de prostanoides, já que estes mediadores são importantes em quase todos os fenómenos associados à inflamação, como vasodilatação, dor e atração de mais leucócitos ao local.
Efeitos desejados[editar | editar código-fonte]
Os AINEs têm três efeitos benéficos principais:
Alguns AINEs, como os salicilatos, também tem efeito antiagregante plaquetar, útil para prevenir tromboses.
Algumas pesquisas revelam possíveis efeitos preventivos em relação à doença de Alzheimer, em particular o Ibuprofeno reduziu a ocorrência da doença em 40% em pessoas que tomaram Ibuprofeno por mais de 5 anos [2].
Efeitos adversos[editar | editar código-fonte]
A maioria é devida à inibição da COX-1. No estômago as prostaglandinas levam à produção de muco que protege as células da mucosa dos efeitos corrosivos do ácido gástrico.
- Dispepsia
- Diarreia ou constipação
- Em administração prolongada, risco de úlcera gástrica e hemorragia gastrointestinal
- Náuseas e vómitos
- Alergias como urticária na pele, eritemas e até raros casos de choque anafilático
- Insuficiência renal reversível com a cessação da medicação
- Nefropatia associada ao uso de analgésicos e anti-inflamatórios: por vezes irreversível, decorre do uso contínuo de aspirina, paracetamol, indometacina, ibuprofeno, diclofenaco. O consumo crônico (por mais de três anos) de NSAIDs pode levar a formas irreversíveis de nefrotoxicidade.[7]
- Síndrome de Reye: emergência rara causada principalmente pela aspirina em crianças.
- Overdose de aspirina causa salicismo com acidose metabólica.
Alguns inibidores da COX-2 foram recentemente retirados do mercado voluntariamente devido a mortes por trombose e enfarte do miocárdio ou AVC.[8]
Usos clínicos[editar | editar código-fonte]
São usados como analgésicos e anti-inflamatórios:[9]
- Dores de cabeça
- Dores nas costas
- Dores de dente
- Dores abdominais
- Dores pós-cirúrgicas
- Dor menstrual (Dismenorreia primária)
- Menstruação prolongada (menorragia)
- Câimbras/Contraturas
- Tendinite, bursite e/ou sinovite
- Artrite reumatoide
- Osteoartrite
- Gota
- Qualquer outra condição inflamatória dolorosa.
São usados como antipiréticos em caso de febre alta maior que 40 °C. Qualquer indivíduo com febre acima de 40 °C deve consultar o médico imediatamente. As prostaglandinas são conhecidas por mediarem o desenvolvimento da febre.
Histórico[editar | editar código-fonte]

As propriedades no alívio da febre, inflamação e dores proporcionadas pela casca do salgueiro são conhecidas há vários anos. Edmund Stone, um reverendo da Inglaterra, escreveu para um presidente da Royal Society ainda no século XVIII sobre as propriedades de cura do salgueiro no combate à febre. Este reverendo sugeriu que como a planta gostava de nascer em locais de umidade, teria como característica reduzir o calor do corpo.
O salgueiro tem como princípio ativo a salicina, que é muito amarga.[10] Este glicosídeo foi isolado por Leroux em 1829. Numa reação de hidrólise, produz glicose e álcool salicílico que pode ser transformado pelo organismo ou via síntese química em ácido acetilsalicílico. Em 1875 o salicilato de sódio foi utilizado pela primeira vez para tratar febre reumática e para reduzir a febre. Assim, Hoffman da Bayer aproveitou uma técnica deixada por Gehardt em 1853, para produzir o salicilato de sódio. Com o sucesso do anti-inflamatório, Heinrich Dreser colocou o produto na medicina com o nome de ácido acetilsalicílico. Depois foram surgindo drogas sintéticas e outros compostos mais seletivos de inibição da COX-2.
Desde o isolamento do ácido salicílico em 1828,[11] os AINE tornaram-se uma parte importante do tratamento da febre e da dor. Uma parte da sua popularidade deve-se a não causarem dependência ou depressão respiratória, ao contrário dos opioides. Ainda assim, não são desprovidos de efeitos secundários, sendo os mais comuns a nível gastrintestinal.
Referências
- ↑ Buer, JK: «Origins and impact of the term 'NSAID'», Inflammopharmacology, vol. 22, no 5, 2014, p. 263-7. (PMID 25064056, DOI 10.1007/s10787-014-0211-2, ler on-line [arquivo]).
- ↑ Bertolini, A; Ferrari A, Ottani A (2006). «Paracetamol: new vistas of an old drug». CNS Drug Reviews. pp. 12(3–4):250–75. PMID 17227290
- ↑ a b Brunton, Laurence L.; John S. Lazo, Keith L. Parker (2006). Goodman & Gilman's The Pharmacological Basis of Therapeutics 11 ed. [S.l.]: McGraw-Hill. ISBN 0-07-142280-3
- ↑ Khanapure SP; Garvey DS, Janero DR, Letts LG (2007). «Eicosanoids in inflammation: biosynthesis, pharmacology, and therapeutic frontiers». Current Topic in Medicinal Chemistry. pp. 7(3):311–40. PMID 17305573
- ↑ Süleyman H; Demircan B, Karagöz Y (2007). «Anti-inflammatory and side effects of cyclooxygenase inhibitors». Pharmacological reports: PR. pp. 59(3):247–58. PMID 17652824
- ↑ Bertolini A; Ottani A, Sandrini M (2001). «Dual acting anti-inflammatory drugs: a reappraisal». Pharmacological Research. pp. 44(6):437–50. PMID 11735348
- ↑ Loureiro, Ana Paula de Melo. «Nefrotoxicantes e Mecanismos de Lesão Renal» (PDF)[ligação inativa]
- ↑ Gotzche, Peter (2013). Deadly Medicines and Organised Crime: How Big Pharma Has Corrupted Healthcare. [S.l.: s.n.] ISBN 978-1846198847
- ↑ Curso de Farmacologia clínica 2011 [1] Arquivado em 4 de agosto de 2016, no Wayback Machine.
- ↑ «Cópia arquivada». Consultado em 8 de junho de 2016. Arquivado do original em 25 de junho de 2016
- ↑ Lafont, O (2007). «From the willow to aspirin». Revue d'histoire de la pharmacie. pp. 55(354):209–16. PMID 18175528