Ibuprofeno
| Ibuprofeno Alerta sobre risco à saúde | |
|---|---|
| |

| |
| |
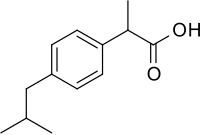
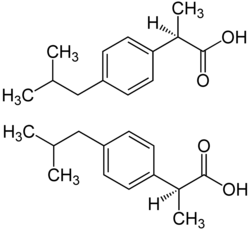
| Nome IUPAC | Ácido (RS)-2-(4-(2-metilpropil)fenil)propanoico, ácido 2-(4-isobutilfenil)propanoico, ácido 2-(4-isobutilfenil)propiônico |
| Identificadores | |
| Número CAS | |
| PubChem | |
| DrugBank | DB01050 |
| ChemSpider | |
| Código ATC | M01 |
| Propriedades | |
| Fórmula química | C13H18O2 |
| Massa molar | 206.27 g mol-1 |
| Aparência | Pó cristalino branco ou cristais incolores[1] |
| Densidade | 1,175 g·cm-3[2] |
| Ponto de fusão | |
| Ponto de ebulição |
154–157 °C (5 hPa)[4] |
| Solubilidade em água | praticamente insolúvel na água:[1][5] 21 mg·l-1 (25 °C)[5] |
| Solubilidade | facilmente solúvel na acetona, no cloreto de metileno, no éter e no metanol. O ibuprofeno dissolve-se nas soluções diluídas dos hidróxidos e dos carbonatos dos metais alcalinos.[1] |
| Pressão de vapor | 1,2 mPa (25 °C)[6] |
| Farmacologia | |
| Via(s) de administração | via oral, via retal, via tópica e intravenosa |
| Metabolismo | hepático |
| Excreção | renal |
| Classificação legal |
Lista de substâncias sujeitas a controle especial - Sem receita (BR)
|
| Riscos associados | |
| Frases R | R22 |
| Frases S | S36 |
| LD50 | 636 mg·kg-1 (rato, per os)[7] 740 mg·kg-1 (camundongo, per os)[7] |
| Compostos relacionados | |
| Compostos relacionados | Ibuproxam (N-hidroxi amida do Ibuprofeno) Ácido hidratrópico (ácido 2-fenil-propiônico) Para-isobutil-isopropil-benzeno |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Ibuprofeno, nome que deriva das iniciais do ácido isobutilpropanoicofenólico (isobutilfenilpropanóico), é um fármaco do grupo dos anti-inflamatórios não esteróides (AINE) utilizado para o tratamento da dor, febre e inflamação.[8] Pode ser utilizado para o alívio sintomático de enxaquecas, moléstias da menstruação, dor dentária, dores do parto, dor muscular, febre e dor pós-cirúrgica; e para quadros inflamatórios como os que se apresentam em artrites, artrite reumatóide e artrite gotosa.[8] Cerca de 60% das pessoas melhoram com a administração de qualquer AINE, e se a primeira medicação não funcionar, recomenda-se que seja tentado outro AINE.[9] O fármaco pode também ser utilizado para fechar um ducto arterioso persistente num bebê prematuro. Pode ser tomado por via oral ou por via intravenosa. Normalmente começa a actuar dentro de uma hora.[8]
Os efeitos colaterais comuns incluem azia e erupção cutânea.[8] Comparativamente com outros AINEs, o ibuprofeno pode apresentar menos efeitos secundários, como hemorragia gastrointestinal.[9] O fármaco aumenta o risco de insuficiência cardíaca, insuficiência renal e insuficiência hepática.[8] Em doses baixas, parece não aumentar o risco de enfarte do miocárdio; no entanto, o mesmo pode não ocorrer com doses elevadas. O ibuprofeno pode também agravar a asma.[9] Apesar de não existirem evidências de que seja prejudicial no início da gravidez,[8] a medicação parece apresentar efeitos nocivos nos estágios mais avançados da gestação e, portanto, é desaconselhada.[10] Tal como outros AINEs, actua inibindo o aparecimento da prostaglandina, ao diminuir a actividade da enzima ciclo-oxigenase.[8] O ibuprofeno é um anti-inflamatório mais fraco do que outros AINEs.[9]
O ibuprofeno foi descoberto em 1961 por Stewart Adams e comercializado como Brufen.[11] Encontra-se disponível sob diversas denominações comerciais, incluindo Advil, Motrin e Nurofen.[8][12] Foi comercializado pela primeira vez em 1969 no Reino Unido e nos Estados Unidos em 1974.[8][11] Consta na Lista de Medicamentos Essenciais da Organização Mundial de Saúde, os medicamentos mais importantes necessários num sistema básico de saúde.[13] Encontra-se disponível como medicamento genérico.[8] O custo grossista no mundo em desenvolvimento varia entre 0,01 e 0,04 dólares por dose.[14] Nos Estados Unidos custa cerca de 0,05 dólares por dose.[8]
Administração[editar | editar código-fonte]
Para adultos, tomar um comprimido de 200 ou 400 mg a cada 4 a 6 h ou um de 600 mg a cada 6 a 8 h até o máximo de 2400 mg/dia. Crianças maiores de 6 meses devem tomar 5 mg/kg em caso de dor moderada e febre menor que 39,5oC ou 10mg/kg em caso de febre de 40oC. Mais que isso pode causar problemas renais e alto risco de gastrite e úlceras gástricas. Não é recomendada nos dois primeiros trimestres de gravidez (categoria B) e é contraindicado no último trimestre (categoria D) pois aumenta o risco de hipertensão e diminui as contrações uterinas. Também não é recomendado durante a lactação.[15]
Indicações[editar | editar código-fonte]
As indicações clínicas aceitas para o ibuprofeno incluem[16]:
- Artrite reumatoide
- Osteoartrite
- Artrite reumatoide juvenil
- Dismenorreia primária
- Febre
- Alívio de dor aguda ou crônica associada a reação inflamatória
- Dores musculares
- Dor de cabeça (cefaleia)
- Dor dentária
- Dor de garganta
Efeitos secundários[editar | editar código-fonte]
Geralmente é bem tolerado. Ocasionalmente, pode ocorrer dor de cabeça, dor de estômago, constipação ou diarreia, gases, tontura, irritabilidade, tinido ou vômitos. Pode produzir gastrite, úlcera do estômago e úlcera no duodeno, e diminuir a função renal e hepática, mas com menor frequência que os derivados salicílicos (como o ácido acetilsalicílico).[17]
Um estudo publicado em janeiro de 2018 observou que a toma regular deste analgésico durante longos períodos de tempo (>2 semanas) diminui a produção de testosterona pelos testículos, levando o corpo a produzir mais hormona luteinizante para manter os níveis de testosterona normais, um estado denominado "hipogonadismo compensatório". Os investigadores suspeitam que o consumo regular durante períodos de tempo muito longos, como é o caso de atletas profissionais ou pessoas com doenças crónicas, possa levar à infertilidade masculina e a outras complicações como depressão, disfunção eréctil e doenças cardiovasculares, revela o estudo publicado na revista científica Proceedings of the National Academy of Sciences. Já se sabia que este efeito podia acontecer em bebés, quando as mães tomavam ibuprofeno; agora, sabe-se que também afecta os homens, sobretudo se o medicamento for tomado com frequência.[18][19]
Mecanismo de ação[editar | editar código-fonte]
O ibuprofeno atua inibindo não seletivamente as ciclooxigenases 1 e 2 evitando assim a consequente formação de mediadores pró-inflamatórios pela cascata do ácido araquidónico. Ao inibir a produção de prostaglandinas, deixa a mucosa gástrica menos protegida contra acidez.
Interações medicamentosas[editar | editar código-fonte]
Aumenta as concentrações plasmáticas de lítio, digoxina e metotrexato. Ainda o medicamento pode interferir no efeito dos diuréticos e de anti-hipertensores.[20]
O uso com glicocorticoides, outros anti-inflamatórios não-esteroides (AINEs) ou com álcool aumenta o risco de úlcera gástrica. Com AINEs ou heparina aumenta sua atividade antitrombótica. Em exames, pode causar diminuição dos níveis de hemoglobina, hematócrito e glicemia.
Síntese[editar | editar código-fonte]


Referências[editar | editar código-fonte]
- ↑ a b c Farmacopeia Portuguesa VII
- ↑ Shankland, N.; Wilson, C.C.; Florence, A.J.; Cox, P.J.: Acta Crystallographica, Section C: Crystal Structure Communications, 1997, 53, S. 951–954; doi:10.1107/S0108270197003193.
- ↑ a b Romero, A.J.; Rhodes, T.C.: „Stereochemical Aspects of the Molecular Pharmaceutics of Ibuprofen“, in: J. Pharm. Pharmacol., 1993, 45, S. 258–262.
- ↑ Kanebo K.K.; JP 52100438; 1977.
- ↑ a b (en) « Ibuprofeno » em ChemIDplus.
- ↑ Ertel, K. D.; Heasley, R. A.; Koegel, C.; Chakrabarti, A.; Carstensen, J. T.: J. Pharm. Sci., 1990, 79, S. 552; doi:10.1002/jps.2600790620.
- ↑ a b Catálogo da Sigma-Aldrich, Ibuprofeno
- ↑ a b c d e f g h i j k «Ibuprofen». The American Society of Health-System Pharmacists. Consultado em 1 de janeiro de 2016
- ↑ a b c d Bnf : march 2014-september 2014. 2014 ed. London: British Medical Assn. 2014. pp. 686–688. ISBN 0857110861
- ↑ «Ibuprofen Pregnancy and Breastfeeding Warnings». Drugs.com. Consultado em 22 de Maio de 2016
- ↑ a b Halford, GM; Lordkipanidzé, M; Watson, SP (2012). «50th anniversary of the discovery of ibuprofen: an interview with Dr Stewart Adams.». Platelets. 23 (6): 415–22. PMID 22098129. doi:10.3109/09537104.2011.632032
- ↑ «Chemistry in your cupboard | Nurofen»
- ↑ WHO Model List of Essential Medicines (PDF) 16ª ed. [S.l.]: World Health Organization. Março de 2009. Consultado em 28 de Março de 2011
- ↑ «Ibuprofen». Consultado em 12 de Janeiro de 2016[ligação inativa]
- ↑ http://www.vademecum.es/principios-activos-ibuprofeno-m01ae01
- ↑ http://www.drugs.com/ibuprofen.html
- ↑ http://www.nlm.nih.gov/medlineplus/druginfo/meds/a682159.html
- ↑ Jornal Público (9 de janeiro de 2018). «Ibuprofeno pode causar infertilidade masculina (e outras complicações)». Consultado em 9 de janeiro de 2018
- ↑ David Møbjerg Kristensena, Christèle Desdoits-Lethimonierb, Abigail L. Mackeyc, Marlene Danner Dalgaarde, Federico De Masie, Cecilie Hurup Munkbølf, Bjarne Styrishavef, Jean-Philippe Antignacg, Bruno Le Bizecg, Christian Platelh, Anders Hay-Schmidti, Tina Kold Jensenj, Laurianne Lesnéb, Séverine Mazaud-Guittotb, Karsten Kristiansenk, Søren Brunaka, Michael Kjaerc, Anders Juuli, Bernard Jégoub (8 de janeiro de 2018). «Ibuprofen alters human testicular physiology to produce a state of compensated hypogonadism». Proceedings of the National Academy os Sciences of the United States of America. doi:10.1073/pnas.1715035115
- ↑ «Derivados do ácido propiónico». Infarmed. Consultado em 10 de junho de 2011. Arquivado do original em 2 de janeiro de 2009
Bibliografia[editar | editar código-fonte]
- Rossi S (Ed.) (2004). Australian Medicines Handbook 2004. ISBN 0-9578521-4-2.
- Castell JV, Gomez MJ, Miranda MA, Morera IM (1987). Photolytic degradation of ibuprofen. Toxicity of the isolated photoproducts on fibroblasts and erythrocytes. Photochem Photobiol, 46 (6), 991-6.
- Hippisley-Cox J, Coupland C (2005). Risk of myocardial infarction in patients taking cyclo-oxygenase-2 inhibitors or conventional non-steroidal antiinflammatory drugs: population based nested case-control analysis. British Medical Journal 2005;330:1366 (11 de Junio).
