Doença pulmonar obstrutiva crónica
| Doença pulmonar obstrutiva crónica | |
|---|---|
| Em cima: pulmões saudáveis com pormenor em corte dos bronquíolos e dos alvéolos pulmonares. Em baixo, as mesmas estruturas em processo de destruição pela DPOC | |
| Sinónimos | Bronquite crónica, enfisema, enfisema pulmonar |
| Especialidade | Pneumologia |
| Sintomas | Falta de ar, tosse com escarro[1] |
| Complicações | Exacerbação aguda da DPOC[2] |
| Início habitual | > 40 anos de idade[3] |
| Duração | Crónica[3] |
| Causas | Fumo do tabaco, poluição do ar, genética[2] |
| Método de diagnóstico | Provas de função respiratória[4] |
| Condições semelhantes | Asma[3] |
| Prevenção | Melhorar a qualidade do ar[3] |
| Tratamento | Deixar de fumar, reabilitação respiratória, transplante de pulmão[2] |
| Medicação | Vacinação, broncodilatadores e corticosteroides por via inalatória, oxigenoterapia[2][5] |
| Frequência | 174,5 milhões (2015)[6] |
| Mortes | 3,2 milhões (2015)[7] |
| Classificação e recursos externos | |
| CID-10 | J40 - J44, J47 |
| CID-9 | 490 - 496 |
| CID-11 | 133207228 |
| OMIM | 606963 |
| DiseasesDB | 2672 |
| MedlinePlus | 000091 |
| eMedicine | med/373 emerg/99 |
| MeSH | D029424 |
A doença pulmonar obstrutiva crónica (português europeu) ou crônica (português brasileiro) (DPOC) é um tipo de doença pulmonar obstrutiva caracterizada por diminuição prolongada do calibre das vias aéreas respiratórias e destruição do tecido pulmonar.[1] Entre os principais sintomas estão falta de ar e tosse com produção de expectoração. A DPOC é uma doença progressiva, o que significa que geralmente se agrava com o decorrer do tempo.[8] A partir de determinado momento começam-se a verificar dificuldades em realizar atividades do dia-a-dia, como subir escadas.[3] Bronquite crónica e enfisema são termos antigos usados para denominar diferentes tipos de DPOC.[3][9] O termo "bronquite crónica" é ainda hoje usado para definir uma tosse produtiva que se manifeste durante pelo menos três meses por ano e ao longo de dois anos.[10]
A inalação de fumo de tabaco é a causa mais comum de DPOC. Outros fatores de risco, como a poluição do ar e a genética, são menos significativos.[2] Em países desenvolvidos, uma das fontes mais comuns de poluição do ar é a má ventilação de fontes de aquecimento e de queima de combustíveis.[3] A exposição prolongada a estes irritantes causa uma resposta inflamatória nos pulmões, o que provoca um estreitamento das vias aéreas e a destruição do tecido pulmonar.[5] O diagnóstico tem por base a medição do fluxo respiratório através de testes que avaliam a função respiratória.[4] Ao contrário da asma, o estreitamento das vias aéreas na DPOC não melhora significativamente após a administração de um broncodilatador.[3]
A maior parte dos casos de DPOC pode ser evitada diminuindo a exposição aos fatores de risco.[11] Entre as principais medidas estão a diminuição da exposição ao fumo do tabaco e a melhoria da qualidade do ar. Embora o tratamento possa atrasar o agravamento, a doença não tem cura.[3] O tratamento inclui deixar de fumar, a vacinação, a reabilitação respiratória e, em muitos casos, a inalação de broncodilatadores e corticosteroides.[2] Em algumas pessoas pode ser benéfica a oxigenoterapia de longo prazo ou um transplante de pulmão.[5] Em pessoas que manifestam períodos de agravamento agudo, podem ser necessárias a hospitalização e uma maior quantidade de medicamentos.[2]
Em 2013 a DPOC afetava cerca de 329 milhões de pessoas, o que corresponde a cerca de 5% da população mundial.[12][13] Geralmente ocorre em pessoas com mais de 40 anos de idade e afeta em proporção idêntica homens e mulheres.[3] Em 2013, a doença foi responsável pela morte de 2,9 milhões de pessoas, um aumento em relação às 2,4 milhões em 1990.[14] Mais de 90% destas mortes ocorrem em países em vias de desenvolvimento.[3] Estima-se que o número de mortes venha a aumentar devido ao aumento de número de fumadores nos países em desenvolvimento e ao aumento da população idosa em muitos países.[15] Em 2010, a doença implicou um custo económico estimado de 2,1 bilhões de dólares.[16]
Sinais e sintomas[editar | editar código-fonte]
Os sintomas mais comuns da doença pulmonar obstrutiva crónica são produção de expectoração, falta de ar e tosse produtiva.[17] Estes sintomas manifestam-se durante um longo período de tempo[18] e geralmente vão-se agravando ao longo do tempo.[5] Não é claro se existem ou não diferentes tipos de DPOC.[2] Embora antigamente a doença se dividisse em enfisema e bronquite crónica, hoje considera-se que enfisema é apenas uma descrição das alterações no pulmão, e não uma doença em si, e que a bronquite crónica descreve apenas os sintomas que podem ou não ocorrer no contexto de DPOC.[8]
Tosse[editar | editar código-fonte]

Em muitos casos, o primeiro sintoma a manifestar-se é a tosse crónica. Por definição, está-se perante bronquite crónica quando essa tosse persiste por mais de três meses por ano e durante pelo menos dois anos, quando é acompanhada pela produção de expectoração e quando não é possível determinar outra explicação. Esta condição pode anteceder o desenvolvimento completo de DPOC. A quantidade de expectoração produzida pode variar no prazo de horas ou dias. No entanto, em alguns casos da doença é possível que não se verifique tosse ou que se verifique apenas tosse ocasional e sem ser produtiva. Algumas pessoas com DPOC atribuem os sintomas ao "catarro do fumador". Dependendo do contexto social e cultural, a expectoração pode ser engolida ou cuspida. A tosse forte pode causar fracturas nas costelas e perda de consciência. As pessoas com DPOC muitas vezes apresentam um histórico daquilo que aparentam ser constipações de duração prolongada.[17]
Falta de ar[editar | editar código-fonte]
A falta de ar é geralmente o sintoma que mais incomoda as pessoas com DPOC.[19] O sintoma é geralmente descrito em termos leigos como "custar a respirar", "sentir-se sem fôlego" ou "não conseguir inspirar ar suficiente".[20] Dependendo do contexto cultural, podem ser usados diversos termos.[17] Geralmente a falta de ar é mais intensa ao realizar esforços de longa duração e vai-se agravando ao longo do tempo.[17] Em estágios avançados da doença, a falta de ar manifesta-se até mesmo em repouso e pode-se manifestar continuamente.[21][22] Em pessoas com a doença, a falta de ar é uma fonte de ansiedade e diminuição da qualidade de vida.[17] Muitas pessoas com DPOC avançada recorrem a respiração freno-labial para aliviar a falta de ar. Esta técnica respiratória consiste em inspirar o ar pelo nariz com a boca fechada e expirar pela boca com os lábios cerrados o máximo possível.[23][24]
Exacerbações[editar | editar código-fonte]
Em pessoas com a doença, uma exacerbação aguda da doença pulmonar obstrutiva crónica define-se pelo aumento da falta de ar, aumento da produção de expectoração, alteração na cor da expectoração de translúcido para verde ou amarelo, ou aumento da intensidade da tosse.[25] A exacerbação pode-se apresentar com sinais de aumento de esforço respiratório, como respiração acelerada, aumento da frequência cardíaca, sudação, utilização ativa dos músculos do pescoço, pele azulada e confusão mental ou comportamento agitado nas exacerbações mais graves.[25][26] Durante um exame com um estetoscópio, também é possível escutar crepitações pulmonares.[27]
Outros sintomas[editar | editar código-fonte]
 |
|
| Problemas para escutar este arquivo? Veja a ajuda. | |
Na DPOC a expiração pode ser mais demorada do que a inspiração.[25] Pode ocorrer sensação de aperto no peito,[17] embora não seja comum e possa ser causada por outro problema.[19] Em pessoas com vias aéreas obstruídas é possível ouvir um sibilo durante a auscultação com um estetoscópio.[25] O tórax em tonel é um sinal característico de DPOC, embora seja relativamente pouco comum.[25] À medida que a doença avança, o corpo pode adquirir uma postura com tendência para a posição de tripé.[18]
Os estádios avançados de DPOC podem causar pressão elevada nas artérias do pulmão, o que comprime o ventrículo direito do coração.[5][28][29] Esta situação é denominada cor pulmonale e manifesta-se através de sintomas como pernas inchadas[17] e pressão venosa jugular.[5] A DPOC é a causa pulmonar mais comum de cor pulmonale,[28] embora a sua prevalência tenha diminuído desde que foi introduzida a oxigenoterapia.[18]
A DPOC ocorre muitas vezes em simultâneo com uma série de outras condições, devido em parte aos fatores de risco que partilha com essas doenças.[2] Entre estas condições estão a cardiopatia isquémica, hipertensão arterial, diabetes, osteoporose, cancro do pulmão, perturbações de ansiedade, disfunções sexuais e depressão.[2][30] Em pessoas com doença grave, é comum a sensação de fadiga.[17] O hipocratismo digital não é específico da DPOC e pode indicar a possibilidade de haver um cancro do pulmão.[31]
Causas[editar | editar código-fonte]
A principal causa da doença pulmonar obstrutiva crónica é o fumo de tabaco. Em alguns países, são também causas significativas a exposição ocupacional e a poluição com origem na queima de combustíveis em ambientes interiores.[8] Geralmente são necessárias várias décadas de exposição até que apareçam os primeiros sintomas.[8] A constituição genética da pessoa também tem influência no risco.[8]
Tabagismo[editar | editar código-fonte]
Em todo o mundo, o principal fator de risco para a DPOC é fumar.[8] Cerca de metade de todos os fumadores desenvolvem a doença.[33][34] Entre 80% e 95% das pessoas com DPOC são ou foram fumadores.[33][35][36] A probabilidade de desenvolver DPOC aumenta em função do número de cigarros fumados.[37] As mulheres são mais suscetíveis aos efeitos nocivos do fumo do tabaco do que os homens.[36] Em não-fumadores, o fumo passivo é a causa de cerca de 20% dos casos.[35] Outros tipos de fumo também aumentam o risco, como o da canábis, de charutos ou o produzido pelos cachimbos de água.[8] O fumo dos cachimbos de água aparenta ser tão nocivo como fumar cigarros.[38] No entanto, é possível que os problemas derivados do fumo de canábis ocorram apenas mediante consumo intensivo.[39] As mulheres que fumem durante a gravidez podem aumentar o risco de DPOC na criança.[8] Para a mesma quantidade de cigarros fumados, as mulheres apresentam um risco superior aos homens de desenvolver DPOC.[40]
Poluição do ar[editar | editar código-fonte]
A queima de combustíveis em espaços interiores mal ventilados é uma das causas mais comuns de DPOC nos países em vias de desenvolvimento. Estas queimas são geralmente alimentadas a carvão ou biomassa, como lenha ou excrementos animais, o que provoca poluição do ar interior.[41] Estas queimas são a principal fonte de aquecimento e de cozinha para cerca de 3 mil milhões de pessoas, e a principal fonte de energia em 80% dos lares na Índia, China e África subsariana. Os seus efeitos são maiores entre as mulheres, uma vez que são o grupo mais exposto.[8][41] No entanto, estudos recentes mostram que a associação entre a DPOC e o uso de queimas alimentadas a carvão ou biomassa pode não ser tão clara como se pensava até há pouco tempo.[42][43][44]
As taxas de incidência de DPOC são geralmente superiores nas zonas com má qualidade de ar, incluindo a poluição derivada dos gases de exaustão.[11] No entanto, acredita-se que em comparação com o fumo de tabaco, o seu papel seja menor.[8] As pessoas que vivem em cidades de grande dimensão apresentam maior incidência de DPOC em comparação com as pessoas que vivem em zonas rurais.[45] Embora a poluição do ar urbana seja um fator que contribui para as exacerbações, o seu papel como causa de DPOC ainda não é claro.[8]
Exposição ocupacional[editar | editar código-fonte]
A exposição intensa e prolongada a poeiras, produtos químicos e fumos no local de trabalho aumenta o risco de DPOC, tanto em fumadores como em não-fumadores.[46] Pensa-se que a exposição ocupacional seja a causa de 10 a 20% dos casos.[47] A maior exposição tem sido associada a determinadas atividades industriais, entre as quais[11] a elevada quantidade de poeiras na mineração de carvão e de ouro e na indústria têxtil de algodão, às profissões que impliquem trabalhar com cádmio e isocianatos e aos fumos de soldadura.[46] Trabalhar na agricultura é também um fator de risco.[11] Estima-se que em algumas profissões o risco seja equivalente ao de fumar entre meio maço a dois maços de cigarros por dia.[48] A exposição ao pó de sílica pode também causar DPOC, não estando o risco relacionado com o da silicose.[49] Os efeitos negativos da exposição às poeias e ao fumo de tabaco aparentam ser cumulativos ou, possivelmente, mais do que cumulativos.[48]
Genética[editar | editar código-fonte]
A genética tem influência no desenvolvimento de DPOC.[8] Entre fumadores, a doença é mais comum entre parentes do que em não parentes.[8] Atualmente, o único fator de risco claramente hereditário é a deficiência de alfa-1-antitripsina.[50] Este risco é particularmente elevado quando a pessoa que apresenta deficiência de alfa-1-antitripsina também é fumador.[50] Esta causa é responsável por 1–5% dos casos[50][51] e a condição está presente em cerca de 3–4 pessoas em cada 10 000.[18] Estão atualmente a ser investigados outros fatores genéticos,[50] que se acredita serem em grande número.[11]
Outras[editar | editar código-fonte]
Existe uma série de outros fatores cuja associação com a doença é menor. O risco é maior em pessoas que vivem na pobreza, embora não seja claro se isto se deve à pobreza em si ou a outros fatores de risco associados à pobreza, como a poluição do ar e a desnutrição.[8] Existem alguns indícios de que as pessoas com asma e hiperatividade nas vias respiratórias possam apresentar maior risco de DPOC.[8] É possível que alguns fatores de risco durante o nascimento, como baixo peso, possam também ter um papel na doença, assim como uma série de doenças infeciosas, como a sida ou a tuberculose.[8] As infeções respiratórias como a pneumonia não aparentam aumentar o risco de DPOC, pelo menos em adultos.[18]
Exacerbações[editar | editar código-fonte]
Uma exacerbação aguda de DPOC é um agravamento súbito dos sintomas.[52] As exacerbações são geralmente espoletadas por uma infeção, por poluentes ambientais ou, ocasionalmente, por outros fatores como o uso indevido de medicamentos.[53] As infeções aparentam ser a causa de 50% a 75% das exacerbações,[53][54] estando presentes bactérias em 25%, vírus em 25% e ambos os organismos nos restantes 25%.[55] Entre os poluentes ambientais estão tanto os que causam deterioração da qualidade do ar interior como exterior.[53] O risco aumenta também com a inalação de fumo de tabaco ou exposição a fumo passivo.[11] As baixas temperaturas podem também contribuir, uma vez que as exacerbações são mais comuns durante o inverno.[56] As exacerbações são mais frequentes em pessoas com DPOC grave. Nos casos mais leves da doença, a média de exacerbações é de 1,8 por ano, nos casos moderados de 2 a 3 por ano e nos casos graves de 3 a 4 por ano.[57] As pessoas com maior número de exacerbações apresentam maior velocidade de deterioração das funções do pulmão.[58] As embolias pulmonares podem agravar os sintomas de pessoas com a doença.[2] Entre os sinais de embolia pulmonar em pessoas com DPOC estão dor torácica pleurística e insuficiência cardíaca sem sinais de infeção.[59]
Fisiopatologia[editar | editar código-fonte]

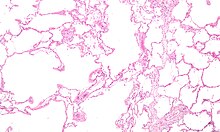
A DPOC é um tipo de doença pulmonar obstrutiva caracterizada por uma limitação crónica e apenas parcialmente reversível das vias aéreas, verificando-se também a incapacidade de expirar por completo.[2] A limitação é o resultado da destruição do tecido pulmonar (denominada "enfisema") e de doença das pequenas vias aéreas (denominada "bronquiolite obstrutiva"). A contribuição de cada um destes fatores varia entre pessoas.[8] A destruição severa das pequenas vias respiratórias pode levar à formação de grandes bolhas de ar que substituem o tecido pulmonar. Esta forma da doença denomina-se "enfisema bolhoso".[60] Algumas pessoas com DPOC apresentam também algum grau de hiperresponsividade a irritantes semelhante ao que se verifica na asma.[18]
A DPOC tem origem numa resposta inflamatória significativa e crónica à inalação de irritantes.[8] Este estado inflamatório pode ainda ser agravado com infeções bacterianas crónicas.[58] Entre as células inflamatórias envolvidas estão os granulócitos neutrófilos e os macrófagos, dois tipos de leucócitos. Entre os fumadores estão também envolvidos os linfócitos T citotóxicos e algumas pessoas com DPOC apresentam envolvimento dos granulócitos eosinófilos de forma semelhante à asma. Parte desta resposta celular é provocada por mediadores inflamatórios, como os fatores quimiotáticos. Entre outros processos envolvidos na destruição do tecido pulmonar estão o stress oxidativo, provocado por concentrações elevadas de radicais livres no fumo do tabaco e libertados por células inflamatórias, e a destruição do tecido conjuntivo dos pulmões por proteases que não são suficientemente inibidas pelos inibidores da protease. A destruição do tecido conjuntivo dos pulmões é o que provoca o enfisema, o que por sua vez contribui para a restrição do fluxo de ar e, por último, para a má absorção e libertação de gases respiratórios. O desgaste generalizado dos músculos que muitas vezes se verifica na DPOC pode ser devido, em parte, aos mediadores inflamatórios libertados pelos pulmões no sangue.[8]
O estreitamento das vias aéreas deve-se à inflamação e cicatrização que nelas ocorre. Isto faz com que a pessoa seja incapaz de respirar na totalidade. A principal restrição no fluxo de ar verifica-se durante a expiração, uma vez que é nesta fase que a pressão no peito comprime as vias aéreas.[61] Isto pode fazer que permaneça nos pulmões o ar da respiração anterior quando se inspira novamente, o que aumenta o volume total de ar nos pulmões em qualquer dado momento. Este processo é denominado "hiperaeração" ou "hiperinsuflação pulmonar".[61][62] A hiperinsuflação por exercício físico está ligada à falta de ar na DPOC, uma vez que a respiração é menos confortável quando os pulmões estão já parcialmente cheios.[63] A hiperinsuflação pode também agravar-se durante uma exacerbação.[64]
Os problemas com as trocas gasosas podem, a partir de determinado momento, causar baixa concentração de oxigénio e a elevada concentração de dióxido de carbono no sangue. Estes problemas têm origem na restrição da ventilação devido à obstrução das vias aéreas, hiperinsuflação e diminuição da vontade de respirar.[8] Durante as exacerbações, aumenta também a inflamação das vias aéreas, o que provoca o aumento da hiperinsuflação, diminuição do volume de ar expirado e agravamento das trocas gasosas. Isto pode também levar a que não haja ventilação suficiente e, por sua vez, à baixa concentração de oxigénio.[5] Quando a concentração de oxigénio se mantém baixa durante um longo período de tempo, pode causar o estreitamento das artérias nos pulmões, enquanto o enfisema causa a desintegração dos vasos capilares nos pulmões. Estas duas alterações levam ao aumento da pressão arterial nas artérias do pulmão, o que pode provocar cor pulmonale.[8]
Diagnóstico[editar | editar código-fonte]

Deve ser considerado o diagnóstico de DPOC em qualquer pessoa com idade superior a 35 ou 40 anos que apresente falta de ar, tosse crónica, produção de expectoração, constipações frequentes e um historial de exposição aos fatores de risco da doença.[17][19] O diagnóstico é geralmente confirmado com exames de espirometria.[17][65] O rastreio em pessoas sem sintomas não está recomendado.[66]
Espirometria[editar | editar código-fonte]
A espirometria permite medir a intensidade da obstrução das vias aéreas. Este exame é geralmente realizado após a administração de um broncodilatador, um medicamento que dilata as vias aéreas.[65] Para a obtenção do diagnóstico, são medidos dois componentes principais: o volume expiratório forçado no primeiro segundo (VEF1), que é o volume máximo de ar que a pessoa é capaz de expirar no primeiro segundo da respiração, e a capacidade vital forçada (CVF), que é o volume máximo de ar que a pessoa é capaz de expirar durante toda a expiração.[67] Geralmente, cerca de 75–80% da CVF é expelida no primeiro segundo.[67] Conclui-se por diagnóstico de DPOC quando a pessoa simultaneamente apresenta sintomas de DPOC e a razão entre o VEF1 e a CVF é inferior a 70%.[65] No entanto, no caso dos idosos estes valores podem levar ao sobre-diagnóstico da doença,[65] pelo que alguns critérios de diagnóstico recomendam que se observe também um VEF1 inferior a 80% do normal.[19]
As evidências que apoiam a eficácia do uso de espirometria para o rastreio de DPOC são incertas, pelo que atualmente o rastreio não está recomendado.[17][65] A avaliação do débito expiratório máximo instantâneo, comum no diagnóstico de asma, não é suficiente para o diagnóstico de DPOC.[19]
Gravidade[editar | editar código-fonte]
| Grau | Atividade em que se verifica falta de ar |
|---|---|
| 1 | Apenas com exercício intenso |
| 2 | Ao caminhar vigorosamente |
| 3 | Ao caminhar normalmente |
| 4 | Após vários minutos de caminhada |
| 5 | Ao vestir-se |
| Gravidade | Diferença em relação ao VEF1 previsto |
|---|---|
| Ligeira (GOLD 1) | ≥80 |
| Moderada (GOLD 2) | 50–79 |
| Grave (GOLD 3) | 30–49 |
| Muito grave (GOLD 4) | <30 |
Existem vários métodos para avaliar a gravidade dos sintomas e a intensidade com que a DPOC afeta determinada pessoa.[17] Algumas avaliações consistem em questionários simples. A avaliação da dispneia é realizada através da Escala do Medical Research Council modificada (mMRC), em que uma pontuação igual ou superior a 2 é considerada elevada. Em alternativa, pode ser utilizado o COPD Assessement Test (CAT). Os resultados variam entre 0 e 40 e uma pontuação igual ou superior a 10 é considerada elevada (quanto mais elevado o resultado, mais grave é a doença).[17][68]
Os exames de espirometria permitem também avaliar a gravidade da restrição das vias aéreas. O valor VEF1 determinado pelo exame pode ser comparado com o valor normal ou expectável para a idade, género, altura e peso da pessoa. A diferença é expressa em percentagem.[17] As normas europeias e norte-americanas recomendam basear as recomendações de tratamento nos valores de VEF1.[65] As orientações da Global Initiative for Chronic Obstructive Lung Disease (GOLD) sugerem dividir as pessoas em quatro categorias com base nos sintomas e na restrição das vias aéreas. Recomenda ainda que sejam tidas em conta a perda de peso, a fraqueza muscular e a presença de outras doenças.[17]
Outros exames[editar | editar código-fonte]
A realização de uma radiografia ao tórax e de um hemograma permitem excluir outras condições no momento do diagnóstico.[69] Os sinais característicos da DPOC observáveis em radiografia são pulmões sobre-expandidos, diafragma achatado e espaço retroesternal aumentado. Ao mesmo tempo, a radiografia permite excluir outras doenças pulmonares, como pneumonia, edema pulmonar ou pneumotórax.[70] Uma tomografia axial computorizada ao tórax permite mostrar a distribuição do enfisema pelos pulmões e pode ajudar a excluir outras doenças pulmonares.[18] No entanto, a não ser nos casos em que se planeie a realização de uma cirurgia, esta distribuição raramente influencia o tratamento.[18] Pode ainda ser realizada uma gasometria arterial para determinar a necessidade de oxigénio suplementar. Este exame é recomendado em pessoas com VEF1 inferior a 35% do previsto, com saturação periférica de oxigénio inferior a 92% e pessoas com sintomas de insuficiência cardíaca congestiva.[17] Em regiões do mundo onde é comum a deficiência de alfa-1 antitripsina, as pessoas com DPOC devem considerar a realização deste exame, sobretudo aquelas com idade inferior a 45 anos e em que o enfisema afeta a parte inferior dos pulmões.[17]
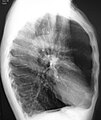
-
Radiografia torácica de DPOC grave, em que se observa o tamanho relativamente pequeno do coração em relação aos pulmões.
-
Radiografia torácica lateral de pessoa com enfisema, em que se observa tórax em tonel e diafragma achatado.
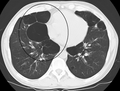
-
Caso grave de enfisema bolhoso
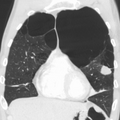
-
TAC axial do pulmão de uma pessoa em estado terminal de enfisema bolhoso.
-
Enfisema muito grave com cancro do pulmão à esquerda
Diagnóstico diferencial[editar | editar código-fonte]
Pode ser necessário diferenciar a DPOC de outras possíveis causas de falta de ar, como insuficiência cardíaca congestiva, embolia pulmonar, pneumonia ou pneumotórax. Muitas pessoas com DPOC assumem, equivocadamente, que têm asma.[25] A distinção entre asma e DPOC baseia-se nos sintomas, no historial de tabagismo e se, durante a espirometria, a obstrução das vias aéreas é ou não reversível com broncodilatadores.[71] A tuberculose pode também apresentar-se com tosse crónica, pelo que nas regiões onde é comum deve ser considerada no diagnóstico.[17] Entre outras condições pouco comuns que podem apresentar sintomas idênticos estão a displasia broncopulmonar e a bronquiolite obliterante.[69] Como a bronquite crónica pode ocorrer sem obstrução das vias aéreas, esta situação não é classificada como DPOC.[18]
Prevenção[editar | editar código-fonte]
A maior parte dos casos de DPOC pode ser evitada diminuindo a exposição ao fumo e melhorando a qualidade do ar.[11] Em pessoas com a doença, a vacina contra a gripe tomada anualmente diminui as exacerbações, hospitalizações e número de mortes.[72][73] A vacina antipneumocócica pode também ter alguns benefícios.[72] No entanto, a vacina Hib por via oral não aparenta diminuir as exacerbações em pessoas com DPOC.[74] Uma dieta rica em betacaroteno pode também apresentar alguns benefícios. No entanto, a ingestão de suplementos não aparenta ter benefícios.[75]
Parar de fumar[editar | editar código-fonte]

Um dos princípios fundamentais da prevenção da DPOC é evitar que as pessoas comecem a fumar.[76] As leis, os institutos públicos e as organizações antitabágicas contribuem para a diminuição do número de fumadores ao desencorajar as pessoas de começar a fumar, ao mesmo tempo que as encorajam a parar de fumar.[77] A proibição de fumar em locais públicos e de trabalho são medidas importantes para diminuir a exposição ao fumo passivo.[11] Nos fumadores, deixar de fumar é a única medida comprovadamente eficaz para atrasar o agravamento da DPOC:[78] Mesmo em estádios avançados da doença, deixar de fumar atrasa a velocidade de degradação da função pulmonar e atrasa o aparecimento de outras insuficiências e da morte.[79]
A cessação tabágica tem início com a decisão de deixar de fumar, que leva a uma primeira tentativa de o fazer. Muitas vezes são necessárias várias tentativas até que se consiga uma abstinência a longo prazo.[77] Considerando um intervalo de cinco anos de tentativas, 40% das pessoas conseguem deixar de fumar.[80] Alguns fumadores conseguem deixar de fumar exclusivamente com força de vontade. No entanto, fumar é extremamente viciante,[81] pelo que muitos fumadores necessitam de meios de apoio. As probabilidades de deixar de fumar aumentam quando existe apoio social, enquadramento num programa de cessação tabágica e com o uso de medicamentos para deixar de fumar, como substitutos de nicotina, bupropiona ou vareniclina.[77][80] Em comparação com a terapia comportamental de forma isolada, a combinação de terapia comportamental com medicação para deixar de fumar oferece uma probabilidade de eficácia duas vezes superior em pessoas com DPOC.[82]
Poluição do ar[editar | editar código-fonte]
Melhorar a qualidade do ar, tanto interior como exterior, pode ajudar a prevenir a DPOC ou atrasar o agravamento da doença existentes.[11] Esta medida pode ser conseguida mediante políticas públicas adequadas, alterações culturais e envolvimento pessoal.[83] Vários países desenvolvidos têm melhorado significativamente a qualidade do ar exterior através de legislação adequada. Estas medidas têm melhorado a função pulmonar da generalidade da sua população.[11] Nos dias de menor qualidade do ar exterior, é possível que as pessoas com DPOC observem menos sintomas se ficarem dentro de portas.[5] Uma das principais medidas para aumentar a qualidade do ar interior é diminuir a exposição ao fumo provocado ao cozinhar e pela queima de combustíveis. Entre estas medidas estão a ventilação adequada e a utilização de exaustores e chaminés com a devida tiragem.[83] A utilização de fogões adequados pode melhorar a qualidade do ar interior em 85%. A utilização de fogões elétricos ou com fontes de energia alternativa, como os fogões solares, também é eficaz. A utilização de combustíveis como querosene ou carvão pode, apesar de tudo, ser menos prejudicial que combustíveis de biomassa, como lenha ou excrementos de animais.[11]
Saúde ocupacional[editar | editar código-fonte]
Existem várias medidas possíveis de serem implementadas para diminuir a probabilidade de que os trabalhadores de indústrias de alto risco, como a mineração de carvão, pedra e construção, venham a desenvolver DPOC.[11] Entre estas medidas estão a educação dos trabalhadores e da gerência sobre os riscos, a promoção da cessação tabágica, o rastreio de trabalhadores para os primeiros sinais de DPOC, a utilização de máscaras respiratórias e o controlo de poeiras.[84][85] O controlo das poeiras pode ser conseguido com sistemas de ventilação apropriados, com a utilização de sprays de água e com recurso da técnicas de mineração que minimizem a criação de poeira.[86] Quando um trabalhador desenvolve DPOC, é possível evitar o prolongamento da exposição ao transferir esse trabalhador para outra função.[87]
Tratamento[editar | editar código-fonte]
Embora não exista cura para a DPOC, os sintomas são tratáveis e a sua progressão pode ser atrasada.[76] Os principais objetivos do tratamento são diminuir os fatores de risco, gerir a DPOC estável, prevenir e tratar as exacerbações agudas e tratar as doenças associadas.[5] As únicas medidas que comprovadamente diminuem a mortalidade são a cessação tabágica e a suplementação de oxigénio.[88] Parar de fumar diminui o risco de morte em 18%.[2] Entre outras recomendações estão a toma anual de vacina contra a gripe, a toma de vacina antipneumocócica a cada cinco anos e a diminuição da exposição à poluição do ar ambiental.[2] Em pessoas com doença avançada, os cuidados paliativos podem diminuir os sintomas e a morfina ajuda a diminuir a sensação de falta de ar.[89] A ventilação mecânica pode ajudar a respirar.[89] Oferecer às pessoas um plano de ação personalizado, uma sessão educativa e apoio durante a realização do plano quando ocorre uma exacerbação pode diminuir o número de visitas hospitalares e encoraja o tratamento imediato das exacerbações.[90]
Exercício físico[editar | editar código-fonte]
A reabilitação pulmonar consiste num programa coordenado e individualizado de exercício, gestão da doença e aconselhamento.[91] Em pessoas com episódios recentes de exacerbações, a reabilitação pulmonar aparenta melhorar a qualidade de vida e a capacidade para realizar exercício físico.[92][93] Não é ainda claro se a reabilitação pulmonar melhora a taxa de mortalidade ou de readmissão hospitalar.[92] Tem-se verificado que a reabilitação melhora as emoções e o sentimento de controlo que a pessoa tem sobre a doença.[94]
No entanto, desconhece-se ainda a rotina e intensidade ideais de exercício físico e a quantidade ideal de ventilação não invasiva para pessoas com DPOC.[93][95][96] A realização de exercícios de resistência no braço melhora o movimento do membro em pessoas com DPOC e pode causar uma ligeira melhoria nas dificuldades respiratórias.[97] Realizar exercícios no braço isoladamente não aparenta melhorar a qualidade de vida.[97] A realização de exercícios de respiração isoladamente aparenta ter uma função limitada.[24] Os exercícios de respiração freno-labial podem ser benéficos.[23][24] A prática de exercícios de tai chi aparenta ser segura em pessoas com DPOC e pode ser benéfica para a função respiratória e capacidade pulmonar, quando comparada com um programa de exercício normal.[98] No entanto, não se verificou que o tai chi seja mais eficaz que outros programas de intervenção com exercício físico.[98]
O excesso de peso ou o baixo peso da pessoa podem afetar os sintomas, grau de insuficiência e o prognóstico de DPOC. As pessoas com DPOC e baixo peso podem melhorar a força dos músculos respiratórios aumentando a ingestão de calorias.[5] Em conjugação com exercício regular ou um programa de reabilitação pulmonar, isto pode levar a melhorias nos sintomas da doença. A suplementação dietética pode ser benéfica em pessoas subnutridas.[99]
Medicamentos[editar | editar código-fonte]

Os principais medicamentos usados no tratamento da DPOC são os broncodilatadores por inalação,[2] embora os seus benefícios sejam limitados.[100] São geralmente administrados dois tipos de broncodilatadores: os agonistas adrenérgicos beta-2 e os anticolinérgicos. Ambos estão disponíveis nas formas de curta e longa duração. Estes medicamentos diminuem a falta de ar, a pieira e as limitações para a prática de exercício físico, contribuindo para o aumento da qualidade de vida.[101] Não é ainda claro se alteram a progressão da doença subjacente.[2]
Broncodilatadores[editar | editar código-fonte]
Para os casos menos graves da doença, são geralmente recomendados broncodilatadores de curta duração a usar apenas em caso de necessidade.[2] Para os casos mais graves, são geralmente recomendados agentes de longa duração.[2] Os agentes de longa duração atuam em parte ao melhorar a hiperinsuflação.[64] Quando os broncodilatadores de longa duração não são suficientes, são geralmente acrescentados corticosteroides por inalação.[2] Em relação aos agentes de longa duração, não é claro se é superior o tiotrópio (um anticolinérgico de longa duração) ou os agonistas beta de longa duração, sendo possível tentar o tratamento com ambos e continuar aquele que seja mais eficaz.[102] Ambos os tipos aparentam diminuir o risco de exacerbações agudas em 15–25%.[2] Embora possam ser usados em simultâneo, o benefício é pouco significativo.[102]
Estão disponíveis diversos agonistas beta de curta duração, entre os quais o salbutamol (Ventilan) e a terbutalina.[103] Estes medicamentos proporcionam algum alívio dos sintomas até quatro a seis horas.[103] Os agonistas beta de longa duração, como o salmeterol, formoterol e indacaterol são muitas vezes usados durante a terapêutica de manutenção. Alguns estudos sustentam que existem poucas evidências de benefícios,[104] enquanto outros asseguram a evidência desses benefícios.[105][106][107] A sua utilização a longa duração na DPOC aparenta ser segura.[108] Os efeitos adversos mais comuns incluem tremores e palpitações cardíacas.[2] A sua utilização em conjunto com esteroides por inalação aumenta o risco de pneumonia.[2] Embora os esteroides e os agonistas beta de longa duração possam funcionar melhor em conjunto,[104] não é claro se este ligeiro benefício é superior ao aumento dos riscos.[109] O indacaterol requer que seja inalada apenas uma dose diária, sendo tão eficaz como outros agonistas beta de longa duração que necessitam de duas doses diárias para pessoas com DPOC estável.[107]
Existem dois tipos principais de anticolinérgicos usados na DPOC, o ipratrópio e o tiotrópio. O ipatrópio é um agente de curta duração, enquanto o tiotrópio é um agente de longa duração. O tiotrópio está associado a uma diminuição nas exacerbações e ao aumento da qualidade de vida,[110] benefícios que são mais significativos no caso do tiotrópio.[111] O tiotrópio não aparente afetar a mortalidade ou a taxa de hospitalização.[110] Os anticolinérgicos podem causar secura na boca e sintomas no trato urinário.[2] Estão também associados ao aumento do risco de doença cardíaca e de acidente vascular cerebral.[112][113] O aclidínio, outro agente de longa duração, diminui as hospitalizações associadas com a DPOC e aumenta a qualidade de vida.[114][115][116] Este agente tem sido usado como alternativa ao tiotrópio, embora se desconheça ainda qual dos fármacos é mais eficaz.[116]
Corticosteroides[editar | editar código-fonte]
Os corticosteroides são usados na prevenção e tratamento de exacerbações agudas. São geralmente usados na forma de inalação, embora possam também ser usados em comprimidos. Embora os corticosteroides por inalação não tenham demonstrado benefícios em pessoas com DPOC ligeira, nos casos moderados e graves da doença estes medicamentos diminuem as exacerbações agudas.[117] Quando usados isoladamente, não afetam a mortalidade a um ano.[88][118] Não é claro se afetam a progressão da doença.[2] Quando usados em conjugação com um agonista beta de longa duração, podem diminuir a mortalidade em comparação com o uso de qualquer um desses fármacos de forma isolada.[119][120] Os esteroides por inalação estão associados a um aumento do risco de pneumonia.[121] O tratamento prolongado com comprimidos de esteroides está associado a efeitos adversos significativos.[103]
Outros[editar | editar código-fonte]
Os antibióticos de longa duração, especificamente os da classe dos macrólidos como a eritromicina, diminuem a frequência de exacerbações em pessoas que têm duas ou mais exacerbações por ano.[122][123] Esta terapêutica pode apresentar boa relação custo-benefício em algumas partes do mundo.[124] No entanto, existem preocupações relativas à resistência antibiótica e a eventuais problemas de audição relacionados com a azitromicina.[123] As metiloxantinas como a teofilina não são geralmente recomendadas devido aos potenciais prejuízos serem superiores aos benefícios,[125] embora possam ser usadas como fármaco de segunda linha nos casos em que a doença não seja controlável com outras medidas.[5] Os agentes mucolíticos podem ajudar a diminuir as exacerbações em algumas pessoas.[126] Os antitússicos não são recomendados.[103]
Oxigénio[editar | editar código-fonte]

A oxigenoterapia é recomendada em pessoas com baixos níveis de oxigénio em repouso (pressão parcial de oxigénio inferior a 50–55 mmHg ou saturação de oxigénio inferior a 88%).[103][127] Neste grupo de pessoas, quando usada 15 horas por dia, esta terapia diminui o risco de insuficiência cardíaca e de morte[103][127] e pode melhorar a capacidade da pessoa em realizar exercício físico.[128] Em pessoas com níveis de oxigénio normais ou ligeiramente baixos, a oxigenoterapia pode melhorar a falta de ar quando administrada durante o exercício, mas pode não ser eficaz durante as atividades quotidianas ou ter impacto na qualidade de vida.[129] Quando a pessoa continua a fumar, além do pouco benefício existe ainda o risco de incêndio.[130] Neste contexto, existem algumas recomendações contra o seu uso.[131] Durante as exacerbações agudas, muitas pessoas necessitam de oxigenoterapia. No entanto, o recurso a concentrações elevadas de oxigénio sem levar em conta os níveis de saturação de oxigénio da pessoa pode levar ao aumento dos níveis de dióxido de carbono e a um pior prognóstico.[132][133] Para pessoas com elevado risco de atingir níveis de dióxido de carbono excessivos, são recomendadas saturações de oxigénio de 88–92%, enquanto para pessoas sem este risco a saturação recomendada é de 94–98%.[133]
Cirurgia[editar | editar código-fonte]
Em pessoas com DPOC muito grave, a cirurgia pode por vezes apresentar benefícios. Entre as opções disponíveis estão o transplante de pulmão ou a cirurgia de redução de volume do pulmão.[2] A cirurgia de redução de volume implica remover as partes do pulmão mais afetadas pelo enfisema, o que permite ao restante pulmão expandir-se e funcionar melhor.[103] Esta cirurgia aparenta ser particularmente eficaz quando o enfisema se situa principalmente no lóbulo superior. No entanto, este procedimento também aumenta o risco de morte prematura e e de efeitos adversos.[134] Em determinados casos muitos graves de DPOC são por vezes realizados transplantes de pulmão, sobretudo em indivíduos mais jovens.[103]
Tratamento de exacerbações[editar | editar código-fonte]
As exacerbações agudas de DPOC são geralmente tratadas aumentando a utilização de broncodilatadores de curta duração.[2] Esta terapêutica geralmente consiste numa combinação de anticolinérgicos e agonistas beta de curta duração por via inalatória.[52] Estes medicamentos podem ser administrados quer através de um inalador dosimetrado com um espaçador ou através de um nebulizador. A eficácia de ambos aparenta ser idêntica.[52][135] A nebulização pode ser um método mais fácil para aqueles que se encontram em piores condições.[52] A oxigenoterpia pode também ser eficaz. No entanto, a administração excessiva de oxigénio pode provocar o aumento dos níveis de dióxido de carbono e a diminuição do estado de consciência.[136]
Os corticosteroides por via oral aumentam a probabilidade de recobro e diminuem a duração dos sintomas.[2][52] Estes medicamentos são tão eficazes como os esteroides por via intravenosa, mas aparentam ter menos efeitos secundários.[137] A administração de esteroides durante cinco dias tem a mesma eficácia de dez ou quatorze.[138] Em pessoas com exacerbações graves, os antibióticos melhoram o prognóstico.[139] É possível administrar vários antibióticos, entre os quais amoxicilina, doxiciclina e azitromicina. Não é claro que a eficácia de um destes antibióticos seja superior à dos restantes.[72] Não se recomenda o uso de fluoroquinilonas quando estejam disponíveis outras opções devido ao maior risco de efeitos secundários graves.[140] Não há evidências claras para pessoas com casos menos graves.[139]
Em pessoas com Insuficiência respiratória do tipo II (aumento agudo dos níveis de dióxido de carbono), a ventilação mecânica não invasiva com pressão positiva diminui a probabilidade de morte ou a necessidade de admissão nos cuidados intensivos.[2] A teofilina pode desempenhar uma função em pessoas que não respondem a outras medidas.[2] A admissão hospitalar só é necessária em menos de 20% das exacerbações.[52] Em pessoas sem acidose devido a insuficiência respiratória, os cuidados em casa podem ajudar a evitar algumas admissões.[52]
Prognóstico[editar | editar código-fonte]


| no data ≤110 110–220 220–330 330–440 440–550 550–660 | 660–770 770–880 880–990 990–1100 1100–1350 ≥1350 |
A DPOC geralmente vai-se agravando ao longo do tempo e pode, a determinado ponto, ser a causa da morte da pessoa. Estima-se que 3% dos anos de vida perdidos estejam relacionados com a doença.[142] A proporção da incapacidade por DPOC diminuiu globalmente entre 1990 e 2010, o que se deve à melhoria na qualidade do ar interior, principalmente na Ásia.[142] No entanto, o número de anos com que se vive com a doença tem vindo a aumentar.[13]
A velocidade a que a DPOC se agrava varia de acordo com a presença ou não de fatores que influenciam o prognóstico, como a obstrução grave das vias respiratórias, incapacidade de realizar exercício físico, falta de ar, falta ou excesso de peso significativos, insuficiência cardíaca congestiva, continuar a fumar e exacerbações frequentes.[5] O prognóstico a longo prazo de DPOC pode ser estimado através do índice BODE. Este índice atribui à pessoa uma escala de zero a dez, tendo em conta fatores como volume expiratório máximo no 1º segundo, o índice de massa corporal, a distância percorrida em 6 minutos e aa escala do Medical Research Council modificada (mMRC) para a avaliação da dispneia.[143] Embora os resultados dos exames de espirometria possam ser um bom indicador da progressão futura da doença, não são tão fidedignos como o índice BODE.[18][19] A perda acentuada de peso é um sinal negativo de prognóstico.[18]
Epidemiologia[editar | editar código-fonte]
Em 2010, a doença pulmonar obstrutiva crónica afetava cerca de 329 milhões de pessoas em todo o mundo, o que corresponde a cerca de 4,8% da população.[13] A doença afeta praticamente de igual forma homens e mulheres.[144] Acredita-se que o aumento da prevalência da doença nos países em vias de desenvolvimento entre 1970 e 2000 esteja relacionado com o aumento da percentagem de fumadores, ao aumento da população e ao envelhecimento da população como consequência da menor mortalidade por outras causas, como doenças infecciosas.[2] Em alguns países desenvolvidos a prevalência tem vindo a aumentar, enquanto noutros se tem mantido estável e noutros ainda tem diminuído.[2] É expectável que os números globais continuem a aumentar, uma vez que os fatores de risco continuam a ser comuns e a população continua a envelhecer.[76]
Entre 1990 e 2010, o número de mortes por DPOC diminuiu ligeiramente, de 3,1 milhões para 2,9 milhões,[145] tendo-se tornado a quarta causa de morte mais comum.[2] Em 2012 tornou-se a terceira causa de morte mais comum, após o número de mortes ter aumentado novamente para 3,1 milhões.[146] Em alguns países, a mortalidade diminuiu entre os homens, mas aumentou entre as mulheres.[147] É provável que isto se deva ao facto de a percentagem de fumadores entre os homens e as mulheres se ter vindo a aproximar.[18] A DPOC é mais comum entre os idosos.[8] Afeta 34–200 em cada 1000 pessoas com mais de 65 anos de idade, dependendo da população em estudo.[8][70]
História[editar | editar código-fonte]

O termo "enfisema" deriva do grego ἐμφυσᾶν emphysan, que significa "inflar", por sua vez composto pelos termos ἐν (in) e φυσᾶν (physan), que significa sopro.[148] O termo "bronquite crónica" teve origem em 1808,[149] enquanto o termo "doença pulmonar obstrutiva crónica" começou a ser usado em 1965.[150] Antes desta última data, a doença era conhecida por uma série de nomes diferentes, entre os quais "doença broncopulmonar obstrutiva crónica", "doença respiratória obstrutiva crónica", "obstrução crónica das vias aéreas", "limitação crónica das vias aéreas", "doença pulmonar crónica não específica" e "síndrome pulmonar obstrutivo difuso". Os termos "bronquite crónica" e "enfisema" foram formalmente estabelecidos em 1959 durante o simpósio CIBA e em 1962 na reunião do Comité da American Thoracic Society relativa às normas de diagnóstico.[150]
Entre as primeiras descrições conhecidas de um provável enfisema estão a do médico suíço Theophile Bonet, que em 1679 descrevia uma condição com "pulmões volumosos", e a do anatomista italiano Giovanni Morgagni, que em 1769 descrevia pulmões "particularmente túrgidos de ar".[150][151] As primeiras ilustrações conhecidas de enfisema datam de 1721 e são da autoria de Frederik Ruysch, um anatomista holandês.[151] São também conhecidas as ilustrações de Matthew Baillie, datadas de 1789 e acompanhadas por descrições da natureza destrutiva da doença. Em 1814, o médico Charles Badham propôs o uso do termo "catarro" para descrever a tosse e expectoração presentes na bronquite crónica. O termo "enfisema" foi usado por René Laennec, o médico que inventou o estetoscópio, no seu livro A Treatise on the Diseases of the Chest and of Mediate Auscultation (1837) para descrever pulmões que não encolhiam ao realizar uma autópsia porque se encontravam cheios de ar e de muco. Em 1842, o cirurgião inglês John Hutchinson inventou o espirómetro, o que viria a permitir medir a capacidade vital dos pulmões. No entanto, o espirómetro da época apenas permitia medir o volume, e não o fluxo de ar. Em 1947, Tiffeneau e Pinelli descreveram os princípios da medição do fluxo de ar.[150]
Em 1953, o alergologista norte-americano George L. Waldbott descreveu uma nova doença a que denominou "síndrome respiratório do fumador", publicada no Journal of the American Medical Association no mesmo ano. Esta foi a primeira associação entre o fumo do tabaco e uma doença respiratória crónica.[152]
Entre as primeiras medidas que se acreditava tratarem a doença estão a ingestão de alho, canela e xarope de ipeca.[149] Os tratamentos modernos só foram desenvolvidos na segunda metade do século XX. As evidências que apoiavam a utilização de esteroides na DPOC foram publicadas no final da década de 1950. Na década de 1960 surgiram os primeiros broncodilatadores, na sequência dos ensaios bem sucedidos de isoprenalina. Nas décadas seguintes foram desenvolvidas novas gerações de broncodilatadores, como o salbutamol (década de 1970) e β2-agonistas de longa duração (meados da década de 1990).[153]
Sociedade e cultura[editar | editar código-fonte]
A DPOC é um problema de saúde pública significativo e com custos sociais elevados. A doença afeta predominantemente as pessoas mais desfavorecidas socialmente e, quando tem início na fase mais produtiva da vida, pode obrigar a uma reforma antecipada de baixo valor.[154] Estima-se que em 2010 o custo económico global da DPOC tenha sido de 2,1 biliões de dólares, metade do qual nos países em vias de desenvolvimento.[16] Deste total, estima-se que 1,9 biliões de dólares correspondam a custos diretos, como cuidados médicos, enquanto 2 mil milhões de dólares correspondam a custos indiretos, como faltas ao emprego.[155] Antevê-se que no ano de 2013 estes valores mais do que dupliquem.[16] Na Europa, a DPOC é responsável por 3% das despesas de saúde.[8]
Embora proporcione alívio dos sintomas, a oxigenoterapia domiciliar prolongada associada à DPOC proporciona algumas barreiras físicas, emocionais e psicossociais. Em muitos casos, o doente com DPOC fica dependente de ajuda para desenvolver atividades quotidianas, necessitando da prestação de cuidadores. Alguns pacientes revelam isolamento social, dificuldade no envolvimento emocional e dificuldades de adaptação e aceitação.[156]
Investigação[editar | editar código-fonte]

Encontram-se em desenvolvimento vários agentes de longa duração.[2] O roflumilaste, o cilomilaste e os inibidores de fosfodiesterase-4 atuam como broncodilatadores e anti-inflamatórios, tendo-se revelado promissores na diminuição do número de exacerbações, mas não aparentam ter influência na qualidade de vida da pessoa.[2][157] O roflumilaste e o cilomilaste podem estar associados a efeitos adversos como problemas gastrointestinais e perda de peso. Também foram relatados distúrbios de sono e de humor com o roflumilaste.[157] O anticorpo imunossupressor infliximab foi estudado em pessoas com DPOC, tendo demonstrado alguns riscos sem que houvesse evidências de benefícios.[158] Ainda não é clara a eficácia do tratamento de suplementação de alfa-1-antitripsina em pessoas com deficiência de alfa-1-antitripsina.[159]
Estão a decorrer estudos para o tratamento com células estaminais.[160] Embora existam alguns indícios de que possa ser seguro, e os dados em animais sejam encorajadores, à data de 2017 não havia ainda dados suficientes em seres humanos.[161][162][163][164] Os dados em seres humanos demonstraram resultados pouco positivos.[161][165]
Está em estudo um procedimento denominado "denervação pulmonar dirigida", que consiste em diminuir a inervação pulmonar do sistema nervoso parassimpático, não havendo ainda dados suficientes para determinar a sua utilização.[166] Continua em estudo a utilização de sistemas de telessaúde no tratamento de pessoas com DPOC durante as exacerbações, o que permitiria diminuir o número de deslocações aos serviços de urgência e melhorar a qualidade de vida.[167]
Referências
- ↑ a b Algusti AG, et al. (2017). «Definition and Overview». Global Strategy for the Diagnosis, Management and Prevention of COPD. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease (GOLD). pp. 6–17
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah Decramer M, Janssens W, Miravitlles M (Abril de 2012). «Chronic obstructive pulmonary disease». Lancet. 379 (9823): 1341–51. PMID 22314182. doi:10.1016/S0140-6736(11)60968-9
- ↑ a b c d e f g h i j k «Chronic obstructive pulmonary disease (COPD) Fact sheet N°315». WHO. Janeiro de 2015. Consultado em 4 de março de 2016
- ↑ a b Nathell L, Nathell M, Malmberg P, Larsson K (2007). «COPD diagnosis related to different guidelines and spirometry techniques». Respir. Res. 8 (1): 89. PMC 2217523
 . PMID 18053200. doi:10.1186/1465-9921-8-89
. PMID 18053200. doi:10.1186/1465-9921-8-89
- ↑ a b c d e f g h i j k l Rabe KF, Hurd S, Anzueto A, Barnes PJ, Buist SA, Calverley P, Fukuchi Y, Jenkins C, Rodriguez-Roisin R, van Weel C, Zielinski J (Setembro de 2007). «Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary». Am. J. Respir. Crit. Care Med. 176 (6): 532–55. PMID 17507545. doi:10.1164/rccm.200703-456SO
- ↑ GBD 2015 Disease and Injury Incidence and Prevalence Collaborators (outubro de 2016). «Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015». Lancet. 388 (10053): 1545–1602. PMC 5055577
 . PMID 27733282. doi:10.1016/S0140-6736(16)31678-6
. PMID 27733282. doi:10.1016/S0140-6736(16)31678-6
- ↑ GBD 2015 Mortality and Causes of Death Collaborators (outubro de 2016). «Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015». Lancet. 388 (10053): 1459–1544. PMC 5388903
 . PMID 27733281. doi:10.1016/S0140-6736(16)31012-1
. PMID 27733281. doi:10.1016/S0140-6736(16)31012-1
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x Vestbo, Jørgen (2013). «Definition and Overview». Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. pp. 1–7
- ↑ Craig, John A. (2012). Ferri's netter patient advisor 2nd ed. [S.l.]: Saunders. p. 913. ISBN 9781455728268
- ↑ Global Strategy for the Diagnosis, Management, and Prevention of COPD. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. 2016. p. 2
- ↑ a b c d e f g h i j k l Pirozzi C, Scholand MB (Julho de 2012). «Smoking cessation and environmental hygiene». Med. Clin. North Am. 96 (4): 849–67. PMID 22793948. doi:10.1016/j.mcna.2012.04.014
- ↑ Global Burden of Disease Study 2013, Collaborators (22 de agosto de 2015). «Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013.». Lancet. 386 (9995): 743–800. PMC 4561509
 . PMID 26063472. doi:10.1016/S0140-6736(15)60692-4
. PMID 26063472. doi:10.1016/S0140-6736(15)60692-4
- ↑ a b c Vos T, Flaxman AD, Naghavi M, Lozano R, Michaud C, Ezzati M, Shibuya K, Salomon JA, Abdalla S, Aboyans V, et al. (Dezembro de 2012). «Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010». Lancet. 380 (9859): 2163–96. PMID 23245607. doi:10.1016/S0140-6736(12)61729-2
- ↑ GBD 2013 Mortality and Causes of Death, Collaborators (17 de dezembro de 2014). «Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013.». Lancet. 385: 117–171. PMC 4340604
 . PMID 25530442. doi:10.1016/S0140-6736(14)61682-2
. PMID 25530442. doi:10.1016/S0140-6736(14)61682-2
- ↑ Mathers CD, Loncar D (Novembro de 2006). «Projections of Global Mortality and Burden of Disease from 2002 to 2030». PLoS Med. 3 (11): e442. PMC 1664601
 . PMID 17132052. doi:10.1371/journal.pmed.0030442
. PMID 17132052. doi:10.1371/journal.pmed.0030442
- ↑ a b c Lomborg, Bjørn (2013). Global problems, local solutions : costs and benefits. [S.l.]: Cambridge University Press. p. 143. ISBN 978-1-107-03959-9
- ↑ a b c d e f g h i j k l m n o p q r s Vestbo, Jørgen (2013). «Diagnosis and Assessment». Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. pp. 9–17
- ↑ a b c d e f g h i j k l Reilly, John J.; Silverman, Edwin K.; Shapiro, Steven D. (2011). «Chronic Obstructive Pulmonary Disease». In: Longo, Dan; Fauci, Anthony; Kasper, Dennis; Hauser, Stephen; Jameson, J.; Loscalzo, Joseph. Harrison's Principles of Internal Medicine 18 ed. [S.l.]: McGraw Hill. pp. 2151–9. ISBN 978-0-07-174889-6
- ↑ a b c d e f g «Chronic obstructive pulmonary disease in over 16s: diagnosis and management». National Institute for Health and Care Excellence. Junho de 2010. Consultado em 19 de março de 2017
- ↑ Mahler DA (2006). «Mechanisms and measurement of dyspnea in chronic obstructive pulmonary disease». Proceedings of the American Thoracic Society. 3 (3): 234–8. PMID 16636091. doi:10.1513/pats.200509-103SF
- ↑ «What Are the Signs and Symptoms of COPD?». National Heart, Lung, and Blood Institute. 31 de julho de 2013. Consultado em 29 de novembro de 2013
- ↑ «Chronic obstructive pulmonary disease». MedLine Plus. 22 de junho de 2015. Consultado em 19 de março de 2017
- ↑ a b Morrison, [edited by] Nathan E. Goldstein, R. Sean (2013). Evidence-based practice of palliative medicine. [S.l.]: Elsevier/Saunders. p. 124. ISBN 978-1-4377-3796-7
- ↑ a b c Holland AE, Hill CJ, Jones AY, McDonald CF (2012). Holland, Anne E, ed. «Breathing exercises for chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 10: CD008250. PMID 23076942. doi:10.1002/14651858.CD008250.pub2
- ↑ a b c d e f Gruber, Phillip (Novembro de 2008). «The Acute Presentation of Chronic Obstructive Pulmonary Disease In the Emergency Department: A Challenging Oxymoron». Emergency Medicine Practice. 10 (11)
- ↑ Brulotte CA, Lang ES (Maio de 2012). «Acute exacerbations of chronic obstructive pulmonary disease in the emergency department». Emerg. Med. Clin. North Am. 30 (2): 223–47, vii. PMID 22487106. doi:10.1016/j.emc.2011.10.005
- ↑ Spiro, Stephen (2012). Clinical respiratory medicine expert consult 4 ed. [S.l.]: Saunders. ISBN 978-1-4557-2329-4
- ↑ a b Weitzenblum E, Chaouat A (2009). «Cor pulmonale». Chron Respir Dis. 6 (3): 177–85. PMID 19643833. doi:10.1177/1479972309104664
- ↑ «Cor pulmonale». Professional guide to diseases 9 ed. [S.l.]: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2009. pp. 120–2. ISBN 978-0-7817-7899-2
- ↑ Levack, William MM; Poot, Betty; Weatherall, Mark; Travers, Justin; Levack, William MM (2015). «Interventions for sexual dysfunction in people with chronic obstructive pulmonary disease (COPD)». Reviews. doi:10.1002/14651858.CD011442.pub2
- ↑ Mandell, editors, James K. Stoller, Franklin A. Michota, Jr., Brian F. (2009). The Cleveland Clinic Foundation intensive review of internal medicine 5th ed. [S.l.]: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 419. ISBN 978-0-7817-9079-6
- ↑ World Health Organization (2008). WHO Report on the Global Tobacco Epidemic 2008: The MPOWER Package (PDF). [S.l.]: World Health Organization. pp. 268–309. ISBN 92-4-159628-7
- ↑ a b Ward, Helen (2012). Oxford Handbook of Epidemiology for Clinicians. [S.l.]: Oxford University Press. pp. 289–290. ISBN 978-0-19-165478-7
- ↑ Laniado-Laborín, R (Janeiro de 2009). «Smoking and chronic obstructive pulmonary disease (COPD). Parallel epidemics of the 21st century». International journal of environmental research and public health. 6 (1): 209–24. PMC 2672326
 . PMID 19440278. doi:10.3390/ijerph6010209
. PMID 19440278. doi:10.3390/ijerph6010209
- ↑ a b Rennard, Stephen (2013). Clinical management of chronic obstructive pulmonary disease 2nd ed. [S.l.]: Informa Healthcare. p. 23. ISBN 978-0-8493-7588-0
- ↑ a b Anita Sharma ; with a contribution by David Pitchforth ; forewords by Gail Richards; Barclay, Joyce (2010). COPD in primary care. [S.l.]: Radcliffe Pub. p. 9. ISBN 978-1-84619-316-3
- ↑ Goldman, Lee (2012). Goldman's Cecil medicine 24th ed. [S.l.]: Elsevier/Saunders. p. 537. ISBN 978-1-4377-1604-7
- ↑ Raad, D; Gaddam, S; Schunemann, HJ; Irani, J; Abou Jaoude, P; Honeine, R; Akl, EA (Abril de 2011). «Effects of water-pipe smoking on lung function: a systematic review and meta-analysis.». Chest. 139 (4): 764–74. PMID 20671057. doi:10.1378/chest.10-0991
- ↑ Joshi, M; Joshi, A; Bartter, T (Março de 2014). «Marijuana and lung diseases.». Current Opinion in Pulmonary Medicine. 20 (2): 173–9. PMID 24384575. doi:10.1097/MCP.0000000000000026
- ↑ Amaral, André F. S.; Strachan, David P.; Burney, Peter Gj; Jarvis, Deborah L. (11 de janeiro de 2017). «Female Smokers are at Greater Risk of Airflow Obstruction than Male Smokers: UK Biobank». American Journal of Respiratory and Critical Care Medicine. ISSN 1535-4970. PMID 28075609. doi:10.1164/rccm.201608-1545OC
- ↑ a b Kennedy SM, Chambers R, Du W, Dimich-Ward H (Dezembro de 2007). «Environmental and occupational exposures: do they affect chronic obstructive pulmonary disease differently in women and men?». Proceedings of the American Thoracic Society. 4 (8): 692–4. PMID 18073405. doi:10.1513/pats.200707-094SD
- ↑ Smith, Margaret; Li, Liming; Augustyn, Mareli; Kurmi, Om; Chen, Junshi; Collins, Rory; Guo, Yu; Han, Yabin; Qin, Jingxin (1 de julho de 2014). «Prevalence and correlates of airflow obstruction in ∼317 000 never-smokers in China». European Respiratory Journal (em inglês). 44 (1): 66–77. ISSN 0903-1936. PMID 24603814. doi:10.1183/09031936.00152413
- ↑ Tan, W. C.; Sin, D. D.; Bourbeau, J.; Hernandez, P.; Chapman, K. R.; Cowie, R.; FitzGerald, J. M.; Marciniuk, D. D.; Maltais, F. (1 de setembro de 2015). «Characteristics of COPD in never-smokers and ever-smokers in the general population: results from the CanCOLD study». Thorax (em inglês). 70 (9): 822–829. ISSN 0040-6376. PMID 26048404. doi:10.1136/thoraxjnl-2015-206938
- ↑ Amaral, André F. S.; Patel, Jaymini; Kato, Bernet S; Obaseki, Daniel O; Lawin, Hervé; Tan, Wan C; Juvekar, Sanjay K; Harrabi, Imed; Studnicka, Michael (12 de setembro de 2017). «Airflow Obstruction and Use of Solid Fuels for Cooking or Heating: BOLD Results». American Journal of Respiratory and Critical Care Medicine. ISSN 1073-449X. doi:10.1164/rccm.201701-0205oc
- ↑ Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM (Setembro de 2006). «Global burden of COPD: systematic review and meta-analysis». Eur. Respir. J. 28 (3): 523–32. PMID 16611654. doi:10.1183/09031936.06.00124605
- ↑ a b Devereux, Graham (2006). «ABC of chronic obstructive pulmonary disease. Definition, epidemiology and risk factors». BMJ. 332 (7550): 1142–4. PMC 1459603
 . PMID 16690673. doi:10.1136/bmj.332.7550.1142
. PMID 16690673. doi:10.1136/bmj.332.7550.1142
- ↑ Laine, Christine (2009). In the Clinic: Practical Information about Common Health Problems. [S.l.]: ACP Press. p. 226. ISBN 978-1-934465-64-6
- ↑ a b Barnes, Peter J.; Drazen, Jeffrey M.; Rennard, Stephen I.; Thomson, Neil C., eds. (2009). «Relationship between cigarette smoking and occupational exposures». Asthma and COPD: Basic Mechanisms and Clinical Management. [S.l.]: Academic. p. 464. ISBN 978-0-12-374001-4
- ↑ Rushton, Lesley (2007). «Chronic Obstructive Pulmonary Disease and Occupational Exposure to Silica». Reviews on Environmental Health. 22 (4): 255–72. PMID 18351226. doi:10.1515/REVEH.2007.22.4.255
- ↑ a b c d Foreman MG, Campos M, Celedón JC (Julho de 2012). «Genes and chronic obstructive pulmonary disease». Med. Clin. North Am. 96 (4): 699–711. PMC 3399759
 . PMID 22793939. doi:10.1016/j.mcna.2012.02.006
. PMID 22793939. doi:10.1016/j.mcna.2012.02.006
- ↑ Brode SK, Ling SC, Chapman KR (Setembro de 2012). «Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease». CMAJ. 184 (12): 1365–71. PMC 3447047
 . PMID 22761482. doi:10.1503/cmaj.111749
. PMID 22761482. doi:10.1503/cmaj.111749
- ↑ a b c d e f g Vestbo, Jørgen (2013). «Management of Exacerbations» (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. pp. 39–45
- ↑ a b c Dhar, Raja (2011). Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. p. 1056. ISBN 978-93-5025-073-0
- ↑ Palange, Paolo (2013). ERS Handbook of Respiratory Medicine. [S.l.]: European Respiratory Society. p. 194. ISBN 978-1-84984-041-5
- ↑ Lötvall, Jan (2011). Advances in combination therapy for asthma and COPD. [S.l.]: Wiley. p. 251. ISBN 978-1-119-97846-6
- ↑ Barnes, Peter (2009). Asthma and COPD : basic mechanisms and clinical management 2nd ed. [S.l.]: Academic. p. 837. ISBN 978-0-12-374001-4
- ↑ Hanania, Nicola (9 de dezembro de 2010). COPD a Guide to Diagnosis and Clinical Management 1st ed. [S.l.]: Springer Science+Business Media, LLC. p. 197. ISBN 978-1-59745-357-8
- ↑ a b Beasley, V; Joshi, PV; Singanayagam, A; Molyneaux, PL; Johnston, SL; Mallia, P (2012). «Lung microbiology and exacerbations in COPD». International Journal of Chronic Obstructive Pulmonary Disease. 7: 555–69. PMC 3437812
 . PMID 22969296. doi:10.2147/COPD.S28286
. PMID 22969296. doi:10.2147/COPD.S28286
- ↑ Aleva, FE; Voets, LW; Simons, SO; de Mast, Q; van der Ven, AJ; Heijdra, YF (11 de agosto de 2016). «Prevalence and Localization of Pulmonary Embolism in Unexplained Acute Exacerbations of COPD: A systematic review and meta-analysis.». Chest. PMID 27522956. doi:10.1016/j.chest.2016.07.034
- ↑ Murphy DM, Fishman AP (2008). «Chapter 53». Fishman's Pulmonary Diseases and Disorders 4th ed. [S.l.]: McGraw-Hill. p. 913. ISBN 0-07-145739-9
- ↑ a b Calverley PM, Koulouris NG (2005). «Flow limitation and dynamic hyperinflation: key concepts in modern respiratory physiology». Eur Respir J. 25 (1): 186–199. PMID 15640341. doi:10.1183/09031936.04.00113204
- ↑ Currie, Graeme P. (2010). ABC of COPD 2nd ed. [S.l.]: Wiley-Blackwell, BMJ Books. p. 32. ISBN 978-1-4443-2948-3
- ↑ O'Donnell DE (2006). «Hyperinflation, Dyspnea, and Exercise Intolerance in Chronic Obstructive Pulmonary Disease». The Proceedings of the American Thoracic Society. 3 (2): 180–4. PMID 16565429. doi:10.1513/pats.200508-093DO
- ↑ a b Cooper, CB (Outubro de 2006). «The connection between chronic obstructive pulmonary disease symptoms and hyperinflation and its impact on exercise and function.». The American Journal of Medicine. 119 (10 Suppl 1): 21–31. PMID 16996896. doi:10.1016/j.amjmed.2006.08.004
- ↑ a b c d e f Qaseem, Amir; Wilt, TJ; Weinberger, SE; Hanania, NA; Criner, G; Van Der Molen, T; Marciniuk, DD; Denberg, T; Schünemann, H; Wedzicha, W; MacDonald, R; Shekelle, P; American College Of Physicians; American College of Chest Physicians; American Thoracic Society; European Respiratory Society (2011). «Diagnosis and Management of Stable Chronic Obstructive Pulmonary Disease: A Clinical Practice Guideline Update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society». Annals of Internal Medicine. 155 (3): 179–91. PMID 21810710. doi:10.7326/0003-4819-155-3-201108020-00008
- ↑ Siu, Albert L.; Bibbins-Domingo, Kirsten; Grossman, David C.; Davidson, Karina W.; Epling, John W.; García, Francisco A. R.; Gillman, Matthew; Kemper, Alex R.; Krist, Alex H.; Kurth, Ann E.; Landefeld, C. Seth; Mangione, Carol M.; Harper, Diane M.; Phillips, William R.; Phipps, Maureen G.; Pignone, Michael P. (5 de abril de 2016). «Screening for Chronic Obstructive Pulmonary Disease». JAMA. 315 (13): 1372. doi:10.1001/jama.2016.2638
- ↑ a b Young, Vincent B. (2010). Blueprints medicine 5th ed. [S.l.]: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 69. ISBN 978-0-7817-8870-0
- ↑ «COPD Assessment Test (CAT)». American Thoracic Society. Consultado em 29 de novembro de 2013
- ↑ a b National Institute for Health and Clinical Excellence. Clinical guideline 101: Chronic Obstructive Pulmonary Disease. Londres, Junho 2010.
- ↑ a b Torres M, Moayedi S (Maio de 2007). «Evaluation of the acutely dyspneic elderly patient». Clin. Geriatr. Med. 23 (2): 307–25, vi. PMID 17462519. doi:10.1016/j.cger.2007.01.007
- ↑ BTS COPD Consortium (2005). «Spirometry in practice – a practical guide to using spirometry in primary care». pp. 8–9. Consultado em 25 de agosto de 2014
- ↑ a b c Mackay AJ, Hurst JR (Julho de 2012). «COPD exacerbations: causes, prevention, and treatment». Med. Clin. North Am. 96 (4): 789–809. PMID 22793945. doi:10.1016/j.mcna.2012.02.008
- ↑ Poole PJ, Chacko E, Wood-Baker RW, Cates CJ (2006). Poole, Phillippa, ed. «Influenza vaccine for patients with chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 1: CD002733. PMID 16437444. doi:10.1002/14651858.CD002733.pub2
- ↑ Teo, Edward; House, Hugh; Lockhart, Kathleen; Purchuri, Sai Navya; Pushparajah, Jennifer; Cripps, Allan W.; van Driel, Mieke L. (9 de setembro de 2014). «Haemophilus influenzae oral vaccination for preventing acute exacerbations of chronic bronchitis and chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (9): CD010010. ISSN 1469-493X. PMID 25201571. doi:10.1002/14651858.CD010010.pub2
- ↑ «Beta-carotene: MedlinePlus Supplements». medlineplus.gov. Consultado em 26 de dezembro de 2016
- ↑ a b c Vestbo, Jørgen (2013). «Introduction». Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. xiii–xv
- ↑ a b c Policy Recommendations for Smoking Cessation and Treatment of Tobacco Dependence. [S.l.]: World Health Organization. pp. 15–40. ISBN 978-92-4-156240-9
- ↑ Jiménez-Ruiz CA, Fagerström KO (Março de 2013). «Smoking cessation treatment for COPD smokers: the role of counselling». Monaldi Arch Chest Dis. 79 (1): 33–7. PMID 23741944. doi:10.4081/monaldi.2013.107
- ↑ Kumar P, Clark M (2005). Clinical Medicine 6th ed. [S.l.]: Elsevier Saunders. pp. 900–1. ISBN 0-7020-2763-4
- ↑ a b Tønnesen P (Março de 2013). «Smoking cessation and COPD». Eur Respir Rev. 22 (127): 37–43. PMID 23457163. doi:10.1183/09059180.00007212
- ↑ «Why is smoking addictive?». NHS Choices. 29 de dezembro de 2011. Consultado em 29 de novembro de 2013
- ↑ van Eerd, Eva A. M.; van der Meer, Regina M.; van Schayck, Onno C. P.; Kotz, Daniel (20 de agosto de 2016). «Smoking cessation for people with chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (8): CD010744. ISSN 1469-493X. PMID 27545342. doi:10.1002/14651858.CD010744.pub2
- ↑ a b Vestbo, Jørgen (2013). «Management of Stable COPD». Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (PDF). [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. pp. 31–8. Arquivado do original (PDF) em 4 de outubro de 2013
- ↑ Smith, Barbara K. Timby, Nancy E. (2005). Essentials of nursing : care of adults and children. [S.l.]: Lippincott Williams & Wilkins. p. 338. ISBN 978-0-7817-5098-1
- ↑ Rom, William N.; Markowitz, Steven B., eds. (2007). Environmental and occupational medicine 4th ed. [S.l.]: Wolters Kluwer/Lippincott Williams & Wilkins. pp. 521–2. ISBN 978-0-7817-6299-1
- ↑ «Wet cutting». Health and Safety Executive. Consultado em 29 de novembro de 2013
- ↑ George, Ronald B. (2005). Chest medicine : essentials of pulmonary and critical care medicine 5th ed. [S.l.]: Lippincott Williams & Wilkins. p. 172. ISBN 978-0-7817-5273-2
- ↑ a b Drummond MB, Dasenbrook EC, Pitz MW, Murphy DJ, Fan E (Novembro de 2008). «Inhaled corticosteroids in patients with stable chronic obstructive pulmonary disease: a systematic review and meta-analysis». JAMA. 300 (20): 2407–16. PMID 19033591. doi:10.1001/jama.2008.717
- ↑ a b Carlucci A, Guerrieri A, Nava S (Dezembro de 2012). «Palliative care in COPD patients: is it only an end-of-life issue?». Eur Respir Rev. 21 (126): 347–54. PMID 23204123. doi:10.1183/09059180.00001512
- ↑ Howcroft, Maxwell; Walters, E. Haydn; Wood-Baker, Richard; Walters, Julia Ae (Dezembro de 2016). «Action plans with brief patient education for exacerbations in chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews. 12: CD005074. ISSN 1469-493X. PMID 27990628. doi:10.1002/14651858.CD005074.pub4
- ↑ «COPD — Treatment». U.S. National Heart Lung and Blood Institute. Consultado em 23 de julho de 2013
- ↑ a b Puhan, Milo A.; Gimeno-Santos, Elena; Cates, Christopher J.; Troosters, Thierry (8 de dezembro de 2016). «Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews. 12: CD005305. ISSN 1469-493X. PMID 27930803. doi:10.1002/14651858.CD005305.pub4
- ↑ a b Zainuldin, Rahizan; Mackey, Martin G.; Alison, Jennifer A. (9 de novembro de 2011). «Optimal intensity and type of leg exercise training for people with chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (11): CD008008. ISSN 1469-493X. PMID 22071841. doi:10.1002/14651858.CD008008.pub2
- ↑ McCarthy, B; Casey, D; Devane, D; Murphy, K; Murphy, E; Lacasse, Y (23 de fevereiro de 2015). «Pulmonary rehabilitation for chronic obstructive pulmonary disease.». Cochrane Database Syst Rev. 2: CD003793. PMID 25705944. doi:10.1002/14651858.CD003793.pub3
- ↑ McNamara, Renae J.; McKeough, Zoe J.; McKenzie, David K.; Alison, Jennifer A. (18 de dezembro de 2013). «Water-based exercise training for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (12): CD008290. ISSN 1469-493X. PMID 24353107. doi:10.1002/14651858.CD008290.pub2
- ↑ Menadue, Collette; Piper, Amanda J.; van 't Hul, Alex J.; Wong, Keith K. (14 de maio de 2014). «Non-invasive ventilation during exercise training for people with chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (5): CD007714. ISSN 1469-493X. PMID 24823712. doi:10.1002/14651858.CD007714.pub2
- ↑ a b McKeough, Zoe J.; Velloso, Marcelo; Lima, Vanessa P.; Alison, Jennifer A. (15 de novembro de 2016). «Upper limb exercise training for COPD». The Cochrane Database of Systematic Reviews. 11: CD011434. ISSN 1469-493X. PMID 27846347. doi:10.1002/14651858.CD011434.pub2
- ↑ a b Ngai, Shirley P. C.; Jones, Alice Y. M.; Tam, Wilson Wai San (7 de junho de 2016). «Tai Chi for chronic obstructive pulmonary disease (COPD)». The Cochrane Database of Systematic Reviews (6): CD009953. ISSN 1469-493X. PMID 27272131. doi:10.1002/14651858.CD009953.pub2
- ↑ Ferreira IM, Brooks D, White J, Goldstein R (2012). Ferreira, Ivone M, ed. «Nutritional supplementation for stable chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 12: CD000998. PMID 23235577. doi:10.1002/14651858.CD000998.pub3
- ↑ van Dijk WD, van den Bemt L, van Weel C (2013). «Megatrials for bronchodilators in chronic obstructive pulmonary disease (COPD) treatment: time to reflect». J Am Board Fam Med. 26 (2): 221–4. PMID 23471939. doi:10.3122/jabfm.2013.02.110342
- ↑ Liesker JJ, Wijkstra PJ, Ten Hacken NH, Koëter GH, Postma DS, Kerstjens HA (Fevereiro de 2002). «A systematic review of the effects of bronchodilators on exercise capacity in patients with COPD». Chest. 121 (2): 597–608. PMID 11834677. doi:10.1378/chest.121.2.597. Consultado em 20 de março de 2017. Arquivado do original em 28 de setembro de 2015
- ↑ a b Farne, Hugo A.; Cates, Christopher J. (22 de outubro de 2015). «Long-acting beta2-agonist in addition to tiotropium versus either tiotropium or long-acting beta2-agonist alone for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (10): CD008989. ISSN 1469-493X. PMID 26490945. doi:10.1002/14651858.CD008989.pub3
- ↑ a b c d e f g h Vestbo, Jørgen (2013). «Therapeutic Options» (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. [S.l.]: Global Initiative for Chronic Obstructive Lung Disease. pp. 19–30
- ↑ a b Cave, AC.; Hurst, MM. (Maio de 2011). «The use of long acting β₂-agonists, alone or in combination with inhaled corticosteroids, in chronic obstructive pulmonary disease (COPD): a risk-benefit analysis». Pharmacol Ther. 130 (2): 114–43. PMID 21276815. doi:10.1016/j.pharmthera.2010.12.008
- ↑ Spencer, S; Karner, C; Cates, CJ; Evans, DJ (7 de dezembro de 2011). Spencer, Sally, ed. «Inhaled corticosteroids versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease». Cochrane Database Syst Rev (12): CD007033. PMID 22161409. doi:10.1002/14651858.CD007033.pub3
- ↑ Wang, J; Nie, B; Xiong, W; Xu, Y (Abril de 2012). «Effect of long-acting beta-agonists on the frequency of COPD exacerbations: a meta-analysis». Journal of clinical pharmacy and therapeutics. 37 (2): 204–11. PMID 21740451. doi:10.1111/j.1365-2710.2011.01285.x
- ↑ a b Geake, James B.; Dabscheck, Eli J.; Wood-Baker, Richard; Cates, Christopher J. (10 de janeiro de 2015). «Indacaterol, a once-daily beta2-agonist, versus twice-daily beta₂-agonists or placebo for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews. 1: CD010139. ISSN 1469-493X. PMID 25575340. doi:10.1002/14651858.CD010139.pub2
- ↑ Decramer ML, Hanania NA, Lötvall JO, Yawn BP (2013). «The safety of long-acting β2-agonists in the treatment of stable chronic obstructive pulmonary disease». Int J Chron Obstruct Pulmon Dis. 8: 53–64. PMC 3558319
 . PMID 23378756. doi:10.2147/COPD.S39018
. PMID 23378756. doi:10.2147/COPD.S39018
- ↑ Nannini, LJ; Lasserson, TJ; Poole, P (12 de setembro de 2012). Nannini, Luis Javier, ed. «Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 9: CD006829. PMID 22972099. doi:10.1002/14651858.CD006829.pub2
- ↑ a b Karner, Charlotta; Chong, Jimmy; Poole, Phillippa (21 de julho de 2014). «Tiotropium versus placebo for chronic obstructive pulmonary disease1». The Cochrane Database of Systematic Reviews (7): CD009285. ISSN 1469-493X. PMID 25046211. doi:10.1002/14651858.CD009285.pub3
- ↑ Cheyne, Leanne; Irvin-Sellers, Melanie J.; White, John (22 de setembro de 2015). «Tiotropium versus ipratropium bromide for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (9): CD009552. ISSN 1469-493X. PMID 26391969. doi:10.1002/14651858.CD009552.pub3
- ↑ Singh S, Loke YK, Furberg CD (Setembro de 2008). «Inhaled anticholinergics and risk of major adverse cardiovascular events in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis». JAMA. 300 (12): 1439–50. PMID 18812535. doi:10.1001/jama.300.12.1439
- ↑ Singh S, Loke YK, Enright P, Furberg CD (Janeiro de 2013). «Pro-arrhythmic and pro-ischaemic effects of inhaled anticholinergic medications». Thorax. 68 (1): 114–6. PMID 22764216. doi:10.1136/thoraxjnl-2011-201275
- ↑ Jones, P (Abril de 2013). «Aclidinium bromide twice daily for the treatment of chronic obstructive pulmonary disease: a review.». Advances in therapy. 30 (4): 354–68. PMID 23553509. doi:10.1007/s12325-013-0019-2
- ↑ Cazzola, M; Page, CP; Matera, MG (junho de 2013). «Aclidinium bromide for the treatment of chronic obstructive pulmonary disease.». Expert opinion on pharmacotherapy. 14 (9): 1205–14. PMID 23566013. doi:10.1517/14656566.2013.789021
- ↑ a b Ni, Han; Soe, Zay; Moe, Soe (19 de setembro de 2014). «Aclidinium bromide for stable chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews. 9: CD010509. ISSN 1469-493X. PMID 25234126. doi:10.1002/14651858.CD010509.pub2
- ↑ Gartlehner G, Hansen RA, Carson SS, Lohr KN (2006). «Efficacy and Safety of Inhaled Corticosteroids in Patients With COPD: A Systematic Review and Meta-Analysis of Health Outcomes». Ann Fam Med. 4 (3): 253–62. PMC 1479432
 . PMID 16735528. doi:10.1370/afm.517
. PMID 16735528. doi:10.1370/afm.517
- ↑ Chinet, T; Dumoulin, J; Honore, I; Braun, JM; Couderc, LJ; Febvre, M; Mangiapan, G; Maurer, C; Serrier, P; Soyez, F; Terrioux, P; Jebrak, G (29 de janeiro de 2016). «[The place of inhaled corticosteroids in COPD].». Revue des maladies respiratoires. PMID 26831345. doi:10.1016/j.rmr.2015.11.009
- ↑ Dong, YH; Lin, HH; Shau, WY; Wu, YC; Chang, CH; Lai, MS (Janeiro de 2013). «Comparative safety of inhaled medications in patients with chronic obstructive pulmonary disease: systematic review and mixed treatment comparison meta-analysis of randomised controlled trials.». Thorax. 68 (1): 48–56. PMID 23042705. doi:10.1136/thoraxjnl-2012-201926
- ↑ Nannini, LJ; Poole, P; Milan, SJ; Kesterton, A (30 de agosto de 2013). «Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus inhaled corticosteroids alone for chronic obstructive pulmonary disease.». Cochrane Database Syst Rev. 8: CD006826. PMID 23990350. doi:10.1002/14651858.CD006826.pub2
- ↑ Kew, KM; Seniukovich, A (10 de março de 2014). «Inhaled steroids and risk of pneumonia for chronic obstructive pulmonary disease.». Cochrane Database Syst Rev. 3: CD010115. PMID 24615270. doi:10.1002/14651858.CD010115.pub2
- ↑ Mammen MJ, Sethi S (2012). «Macrolide therapy for the prevention of acute exacerbations in chronic obstructive pulmonary disease». Pol. Arch. Med. Wewn. 122 (1–2): 54–9. PMID 22353707
- ↑ a b Herath, SC; Poole, P (Novembro de 2013). «Prophylactic antibiotic therapy for chronic obstructive pulmonary disease (COPD).». Cochrane Database Syst Rev. 11: CD009764. PMID 24288145. doi:10.1002/14651858.CD009764.pub2
- ↑ Simoens, S; Laekeman, G; Decramer, M (Maio de 2013). «Preventing COPD exacerbations with macrolides: a review and budget impact analysis». Respiratory medicine. 107 (5): 637–48. PMID 23352223. doi:10.1016/j.rmed.2012.12.019
- ↑ Barr RG, Rowe BH, Camargo CA (2003). Barr, R Graham, ed. «Methylxanthines for exacerbations of chronic obstructive pulmonary disease». Cochrane Database Syst Rev (2): CD002168. PMID 12804425. doi:10.1002/14651858.CD002168
- ↑ Poole, P; Chong, J; Cates, CJ (29 de julho de 2015). «Mucolytic agents versus placebo for chronic bronchitis or chronic obstructive pulmonary disease.». Cochrane Database Syst Rev. 7: CD001287. PMID 26222376. doi:10.1002/14651858.CD001287.pub5
- ↑ a b COPD Working, Group (2012). «Long-term oxygen therapy for patients with chronic obstructive pulmonary disease (COPD): an evidence-based analysis». Ontario health technology assessment series. 12 (7): 1–64. PMC 3384376
 . PMID 23074435
. PMID 23074435
- ↑ Bradley JM, O'Neill B (2005). Bradley, Judy M, ed. «Short-term ambulatory oxygen for chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 4: CD004356. PMID 16235359. doi:10.1002/14651858.CD004356.pub3
- ↑ Ekström, Magnus; Ahmadi, Zainab; Bornefalk-Hermansson, Anna; Abernethy, Amy; Currow, David (25 de novembro de 2016). «Oxygen for breathlessness in patients with chronic obstructive pulmonary disease who do not qualify for home oxygen therapy». The Cochrane Database of Systematic Reviews. 11: CD006429. ISSN 1469-493X. PMID 27886372. doi:10.1002/14651858.CD006429.pub3
- ↑ Chapman, Stephen (2009). Oxford handbook of respiratory medicine 2nd ed. [S.l.]: Oxford University Press. p. 707. ISBN 978-0-19-954516-2
- ↑ Blackler, Laura (2007). Managing chronic obstructive pulmonary disease. [S.l.]: Wiley. p. 49. ISBN 978-0-470-51798-7
- ↑ Jindal, Surinder K (2013). Chronic Obstructive Pulmonary Disease. [S.l.]: Jaypee Brothers Medical. p. 139. ISBN 978-93-5090-353-7
- ↑ a b O'Driscoll, BR; Howard, LS; Davison, AG; British Thoracic, Society (Outubro de 2008). «BTS guideline for emergency oxygen use in adult patients». Thorax. 63 (Suppl 6): vi1–68. PMID 18838559. doi:10.1136/thx.2008.102947
- ↑ van Agteren, JE; Carson, KV; Tiong, LU; Smith, BJ (14 de outubro de 2016). «Lung volume reduction surgery for diffuse emphysema.». The Cochrane database of systematic reviews. 10: CD001001. PMID 27739074. doi:10.1002/14651858.CD001001.pub3
- ↑ «Bronchodilators delivered by nebuliser versus inhalers for lung attacks of chronic obstructive pulmonary disease». Cochrane Database of Systematic Reviews. 29 de agosto de 2016. doi:10.1002/14651858.cd011826
- ↑ Wise, Robert. «Chronic Obstructive Pulmonary Disease (COPD) - Pulmonary Disorders - Merck Manuals Professional Edition». Merck Manuals Professional Edition. Consultado em 16 de dezembro de 2016
- ↑ Walters, JA; Tan, DJ; White, CJ; Gibson, PG; Wood-Baker, R; Walters, EH (Setembro de 2014). «Systemic corticosteroids for acute exacerbations of chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 9: CD001288. PMID 25178099. doi:10.1002/14651858.CD001288.pub4
- ↑ Walters, JA; Tan, DJ; White, CJ; Wood-Baker, R (10 de dezembro de 2014). «Different durations of corticosteroid therapy for exacerbations of chronic obstructive pulmonary disease.». Cochrane Database Syst Rev. 12: CD006897. PMID 25491891. doi:10.1002/14651858.CD006897.pub3
- ↑ a b Vollenweider DJ, Jarrett H, Steurer-Stey CA, Garcia-Aymerich J, Puhan MA (2012). Vollenweider, Daniela J, ed. «Antibiotics for exacerbations of chronic obstructive pulmonary disease». Cochrane Database Syst Rev. 12: CD010257. PMID 23235687. doi:10.1002/14651858.CD010257
- ↑ «Fluoroquinolone Antibacterial Drugs: Drug Safety Communication - FDA Advises Restricting Use for Certain Uncomplicated Infections». FDA. 12 de maio de 2016. Consultado em 16 de maio de 2016
- ↑ «WHO Disease and injury country estimates». World Health Organization. 2009. Consultado em 11 de novembro de 2009
- ↑ a b Murray CJ, Vos T, Lozano R, Naghavi M, Flaxman AD, Michaud C, Ezzati M, Shibuya K, Salomon JA, et al. (Dezembro de 2012). «Disability-adjusted life years (DALYs) for 291 diseases and injuries in 21 regions, 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010». Lancet. 380 (9859): 2197–223. PMID 23245608. doi:10.1016/S0140-6736(12)61689-4
- ↑ Medicine, prepared by the Department of Medicine, Washington University School of (2009). The Washington manual general internal medicine subspecialty consult. 2nd ed. [S.l.]: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 96. ISBN 978-0-7817-9155-7
- ↑ «Chronic obstructive pulmonary disease (COPD) Fact sheet N°315». WHO. Janeiro de 2015
- ↑ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, Abraham J, Adair T, Aggarwal R, et al. (Dezembro de 2012). «Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010». Lancet. 380 (9859): 2095–128. PMID 23245604. doi:10.1016/S0140-6736(12)61728-0
- ↑ «The 10 leading causes of death in the world, 2000 and 2011». World Health Organization. Julho de 2013. Consultado em 29 de novembro de 2013
- ↑ Rycroft CE, Heyes A, Lanza L, Becker K (2012). «Epidemiology of chronic obstructive pulmonary disease: a literature review». Int J Chron Obstruct Pulmon Dis. 7: 457–94. PMC 3422122
 . PMID 22927753. doi:10.2147/COPD.S32330
. PMID 22927753. doi:10.2147/COPD.S32330
- ↑ «Emphysema». Dictionary.com. Consultado em 21 de novembro de 2013
- ↑ a b Ziment, Irwin (1991). «History of the Treatment of Chronic Bronchitis». Respiration. 58 (Suppl 1): 37–42. PMID 1925077. doi:10.1159/000195969
- ↑ a b c d Petty TL (2006). «The history of COPD». Int J Chron Obstruct Pulmon Dis. 1 (1): 3–14. PMC 2706597
 . PMID 18046898. doi:10.2147/copd.2006.1.1.3
. PMID 18046898. doi:10.2147/copd.2006.1.1.3
- ↑ a b Wright, Joanne L.; Churg, Andrew (2008). «Pathologic Features of Chronic Obstructive Pulmonary Disease: Diagnostic Criteria and Differential Diagnosis» (PDF). In: Fishman, Alfred; Elias, Jack; Fishman, Jay; Grippi, Michael; Senior, Robert; Pack, Allan. Fishman's Pulmonary Diseases and Disorders 4th ed. [S.l.]: McGraw-Hill. pp. 693–705. ISBN 978-0-07-164109-8
- ↑ Waldbott, George L. (1965). A struggle with Titans. [S.l.]: Carlton Press. p. 6
- ↑ Fishman AP (Maio de 2005). «One hundred years of chronic obstructive pulmonary disease». Am. J. Respir. Crit. Care Med. 171 (9): 941–8. PMID 15849329. doi:10.1164/rccm.200412-1685OE
- ↑ Baldaia, João (1999). «Factores de ordem social, económica e cultural da DPOC em internamento hospitalar». Revista Portuguesa de Pneumologia. 5 (1): 67-73. doi:10.1016/S0873-2159(15)30955-7
- ↑ Bloom, D (2011). The Global Economic Burden of Noncommunicable Diseases (PDF). [S.l.]: World Economic Forum. p. 24
- ↑ Bueno, Giovanna Hass (14 de fevereiro de 2017). «Perspectivas dos Pacientes com Doença Pulmonar Obstrutiva Crônica (DPOC) e de seus cuidadores frente ao uso da Oxigenoterapia Domiciliar Prolongada (ODP)». UNESP. Consultado em 30 de abril de 2017
- ↑ a b Chong, Jimmy; Leung, Bonnie; Poole, Phillippa (4 de novembro de 2013). «Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (11): CD002309. ISSN 1469-493X. PMID 24190161. doi:10.1002/14651858.CD002309.pub4
- ↑ Nici, Linda (2011). Chronic Obstructive Pulmonary Disease: Co-Morbidities and Systemic Consequences. [S.l.]: Springer. p. 78. ISBN 978-1-60761-673-3
- ↑ Gøtzsche, Peter C.; Johansen, Helle Krogh (20 de setembro de 2016). «Intravenous alpha-1 antitrypsin augmentation therapy for treating patients with alpha-1 antitrypsin deficiency and lung disease». The Cochrane Database of Systematic Reviews. 9: CD007851. ISSN 1469-493X. PMID 27644166. doi:10.1002/14651858.CD007851.pub3
- ↑ Inamdar, AC; Inamdar, AA (Outubro de 2013). «Mesenchymal stem cell therapy in lung disorders: pathogenesis of lung diseases and mechanism of action of mesenchymal stem cell.». Experimental Lung Research. 39 (8): 315–327. PMID 23992090. doi:10.3109/01902148.2013.816803
- ↑ a b Oh, DK; Kim, YS; Oh, YM (Janeiro de 2017). «Lung Regeneration Therapy for Chronic Obstructive Pulmonary Disease». Tuberc Respir Dis (Seoul). 80 (1): 1–10. PMC 5256352
 . PMID 28119741. doi:10.4046/trd.2017.80.1.1
. PMID 28119741. doi:10.4046/trd.2017.80.1.1
- ↑ Conese, M; Piro, D; Carbone, A; Castellani, S; Di Gioia, S (2014). «Hematopoietic and mesenchymal stem cells for the treatment of chronic respiratory diseases: role of plasticity and heterogeneity». The Scientific World Journal. 2014: 859817. PMC 3916026
 . PMID 24563632. doi:10.1155/2014/859817
. PMID 24563632. doi:10.1155/2014/859817
- ↑ McQualter, JL; Anthony, D; Bozinovski, S; Prêle, CM; Laurent, GJ (Novembro de 2014). «Harnessing the potential of lung stem cells for regenerative medicine». The International Journal of Biochemistry & Cell Biology. 56: 82–91. PMID 25450456. doi:10.1016/j.biocel.2014.10.012
- ↑ Tzouvelekis, A; Ntolios, P; Bouros, D (2013). «Stem cell treatment for chronic lung diseases». Respiration. 85 (3): 179–192. PMID 23364286. doi:10.1159/000346525
- ↑ Tzouvelekis, A; Laurent, G; Bouros, D (Fevereiro de 2013). «Stem cell therapy in chronic obstructive pulmonary disease. Seeking the Prometheus effect». Current Drug Targets. 14 (2): 246–252. PMID 23256721. doi:10.2174/1389450111314020009
- ↑ Gompelmann, D; Eberhardt, R; Herth, FJ (Agosto de 2015). «Novel Endoscopic Approaches to Treating Chronic Obstructive Pulmonary Disease and Emphysema.». Seminars in Respiratory and Critical Care Medicine. 36 (4): 609–615. PMID 26238645. doi:10.1055/s-0035-1555614
- ↑ McLean, Susannah; Nurmatov, Ulugbek; Liu, Joseph Ly; Pagliari, Claudia; Car, Josip; Sheikh, Aziz (6 de julho de 2011). «Telehealthcare for chronic obstructive pulmonary disease». The Cochrane Database of Systematic Reviews (7): CD007718. ISSN 1469-493X. PMID 21735417. doi:10.1002/14651858.CD007718.pub2
Ligações externas[editar | editar código-fonte]
- Diagnóstico e Tratamento da Doença Pulmonar Obstrutiva Crónica, norma da Direção-Geral de Saúde
- Associação Brasileira de Portadores de DPOC
- Fundação Portuguesa do Pulmão