Glicose: diferenças entre revisões
Desfeita a edição 48380632 de 201.68.233.87 Etiqueta: Possível resumo indevido |
m traduzindo nome/parâmetro de predefinições, outros ajustes usando script |
||
| Linha 1: | Linha 1: | ||
{{mais |
{{mais notas|data=Junho de 2011}} |
||
{{Info/Química |
{{Info/Química |
||
| verifiedrevid = 311440464 |
| verifiedrevid = 311440464 |
||
| Linha 18: | Linha 18: | ||
| Section1 = {{Chembox Identifiers |
| Section1 = {{Chembox Identifiers |
||
| Abbreviations = Glc |
| Abbreviations = Glc |
||
| CASNo = 50-99-7 |
| CASNo = 50-99-7 |
||
| CASNo_Ref = {{cascite}} |
| CASNo_Ref = {{cascite}} |
||
| CASOther = <br />492-62-6 (α-anomer)<br />492-61-5 (β-anomer) <!-- these CAS numbers have been verified against CAS Common Chemistry --> |
| CASOther = <br />492-62-6 (α-anomer)<br />492-61-5 (β-anomer) <!-- these CAS numbers have been verified against CAS Common Chemistry --> |
||
| EINECS = 200-075-1 |
| EINECS = 200-075-1 |
||
| PubChem = 5793 |
| PubChem = 5793 |
||
| ChemSpiderID = 5589 |
| ChemSpiderID = 5589 |
||
| Linha 29: | Linha 29: | ||
}} |
}} |
||
| Section2 = {{Chembox Properties |
| Section2 = {{Chembox Properties |
||
| Reference = <ref>{{citation | url = http://oru.edu/cccda/sl/solubility/allsolvents.php?solute=D-glucose | |
| Reference = <ref>{{citation | url = http://oru.edu/cccda/sl/solubility/allsolvents.php?solute=D-glucose |título= Solubility of D-glucose in non-aqueous solvents}}.</ref> |
||
| Formula = C<sub>6</sub>H<sub>12</sub>O<sub>6</sub> |
| Formula = C<sub>6</sub>H<sub>12</sub>O<sub>6</sub> |
||
| MolarMass = 180.16 g/mol |
| MolarMass = 180.16 g/mol |
||
| ExactMass = 180.063388 |
| ExactMass = 180.063388 |
||
| MeltingPt = 146 °C <ref name="gestis"/> <br /> α-<small>D</small>-glucose: 146 °C {{carece de fontes}} <br />β-<small>D</small>-glucose: 150 °C {{carece de fontes}} |
| MeltingPt = 146 °C <ref name="gestis"/> <br /> α-<small>D</small>-glucose: 146 °C {{carece de fontes|data=abril de 2017}} <br />β-<small>D</small>-glucose: 150 °C {{carece de fontes|data=abril de 2017}} |
||
| Density = 1,5620 g·cm<sup>-3</sup><ref name="CRC_HANDBOOK_TeF6">''[[CRC Handbook of Chemistry and Physics]]'', 90. Auflage, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 3, ''Physical Constants of Organic Compounds'', p. 3-268.</ref> |
| Density = 1,5620 g·cm<sup>-3</sup><ref name="CRC_HANDBOOK_TeF6">''[[CRC Handbook of Chemistry and Physics]]'', 90. Auflage, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 3, ''Physical Constants of Organic Compounds'', p. 3-268.</ref> |
||
| Solubility = 470 g·l<sup>-1</sup> a 20 °C <ref name="gestis">{{GESTIS|ZVG=19010|CAS=50-99-7|Name=|Date=29 de Março de 2008}}</ref> |
| Solubility = 470 g·l<sup>-1</sup> a 20 °C <ref name="gestis">{{GESTIS|ZVG=19010|CAS=50-99-7|Name=|Date=29 de Março de 2008}}</ref> |
||
| Solubility1 = 0.037 M |
| Solubility1 = 0.037 M |
||
| Linha 45: | Linha 45: | ||
}} |
}} |
||
| Section3 = {{Chembox Thermochemistry |
| Section3 = {{Chembox Thermochemistry |
||
| Reference = <ref>{{citation | |
| Reference = <ref>{{citation |último1 = Ponomarev |primeiro1 = V. V. |último2 = Migarskaya |primeiro2 = L. B. |título= Heats of combustion of some amino-acids |periódico= Russ. J. Phys. Chem. (Engl. Transl.) |ano= 1960 | volume = 34 |páginas= 1182–83}}. {{citation |último = Boerio-Goates |primeiro = Juliana |título= Heat-capacity measurements and thermodynamic functions of crystalline α-D-glucose at temperatures from 10K to 340K |periódico= J. Chem. Thermodynam. |ano= 1991 | volume = 23 |número= 5 |páginas= 403–9 | doi = 10.1016/S0021-9614(05)80128-4}}.</ref> |
||
| DeltaHf = −1271 kJ/mol |
| DeltaHf = −1271 kJ/mol |
||
| DeltaHc = −2805 kJ/mol |
| DeltaHc = −2805 kJ/mol |
||
| Linha 67: | Linha 67: | ||
}} |
}} |
||
}} |
}} |
||
A '''glicose''', '''glucose''' ou '''dextrose''', um [[monossacarídeos|monossacarídeo]],<ref name="pubchem">[http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=5793 PubChem]</ref> é um dos [[carboidrato |
A '''glicose''', '''glucose''' ou '''dextrose''', um [[monossacarídeos|monossacarídeo]],<ref name="pubchem">[http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=5793 PubChem]</ref> é um dos [[carboidrato]]s mais importantes na [[biologia]].<ref name="brasil.escola">Gabriela Cabral, ''Brasil Escola'', ''Glicose'', site do [[Portal R7]] [http://www.brasilescola.com/saude/glicose.htm <small><nowiki>[em linha]</nowiki></small>]</ref> As células a usam como fonte de energia e intermediário metabólico. A glicose é um dos principais produtos da [[fotossíntese]] e inicia a [[respiração celular]] em seres [[procarionte]]s e [[eucarionte]]s. É um cristal sólido de sabor adocicado, de formula molecular C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>, encontrado na natureza na forma livre ou combinada. Juntamente com a [[frutose]] e a [[galactose]], é o carboidrato fundamental de carboidratos maiores, como [[sacarose]] e [[maltose]]. [[Amido]] e [[celulose]] são [[polímeros]] de glucose. |
||
No [[metabolismo]], a glicose é uma das principais fontes de energia e fornece 4 calorias de energia por grama. A glicose hidratada (como no soro glicosado) fornece 3,4 [[caloria]]s por grama. Sua degradação química durante o processo de [[respiração]] celular dá origem a [[energia química]] (armazenada em moléculas de [[Adenosina trifosfato|ATP]] - 36 ou 38 moleculas (depende da celula) de ATP por moléculas de glicose), [[gás carbônico]] e [[água]]. |
No [[metabolismo]], a glicose é uma das principais fontes de energia e fornece 4 calorias de energia por grama. A glicose hidratada (como no soro glicosado) fornece 3,4 [[caloria]]s por grama. Sua degradação química durante o processo de [[respiração]] celular dá origem a [[energia química]] (armazenada em moléculas de [[Adenosina trifosfato|ATP]] - 36 ou 38 moleculas (depende da celula) de ATP por moléculas de glicose), [[gás carbônico]] e [[água]]. |
||
| Linha 75: | Linha 75: | ||
Apresenta fórmula mínima: CH<sub>2</sub>O |
Apresenta fórmula mínima: CH<sub>2</sub>O |
||
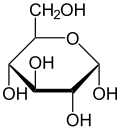
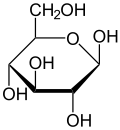
Fórmula estrutural: |
Fórmula estrutural: |
||
* Alfa [[Ficheiro:Alpha-D-Glucopyranose.svg|120px]] |
* Alfa [[Ficheiro:Alpha-D-Glucopyranose.svg|120px]] |
||
Revisão das 03h21min de 18 de abril de 2017
| D-Glucose Alerta sobre risco à saúde | |
|---|---|

|

|

| |

| |

| |
| Nome IUPAC | D-Glucose |
| Outros nomes | Dextrose 6-(hidroximetil)oxano-2,3,4,5-tetrol |
| Identificadores | |
| Abreviação | Glc |
| Número CAS | , 492-62-6 (α-anomer) 492-61-5 (β-anomer) |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C6H12O6 |
| Massa molar | 180.16 g/mol |
| Aparência | Cristalina |
| Densidade | 1,5620 g·cm-3[1] |
| Ponto de fusão |
146 °C [2] |
| Solubilidade em água | 470 g·l-1 a 20 °C [2] |
| Solubilidade em metanol | 0.037 M |
| Solubilidade em etanol | 0.006 M |
| Solubilidade em Tetraidrofurano | 0.016 M |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
−1271 kJ/mol |
| Entalpia padrão de combustão ΔcH |
−2805 kJ/mol |
| Entropia molar padrão S |
209.2 J K−1 mol−1 |
| Riscos associados | |
| MSDS | ICSC 0865 |
| Índice UE | not listed |
| NFPA 704 | |
| Frases R | - |
| Frases S | - |
| LD50 | 25,8 g·kg-1 (rato, oral) (D-glicose)[3] |
| Compostos relacionados | |
| Outros aniões/ânions | Glucosamina (hidroxila do carbono 3 trocada por amina) |
| Aldohexoses (isômeros óticos da Glicose) relacionados | Alose Altrose Manose Gulose Idose Galactose Talose |
| Compostos relacionados | Sorbitol (hexano-1,2,3,4,5,6-hexaol, carbono 1 reduzido de aldeído a álcool) Ácido glicurônico (carbono 6 duplamente oxidado para carboxila) Glicose-6-fosfato Glicogénio (polímero) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A glicose, glucose ou dextrose, um monossacarídeo,[4] é um dos carboidratos mais importantes na biologia.[5] As células a usam como fonte de energia e intermediário metabólico. A glicose é um dos principais produtos da fotossíntese e inicia a respiração celular em seres procariontes e eucariontes. É um cristal sólido de sabor adocicado, de formula molecular C6H12O6, encontrado na natureza na forma livre ou combinada. Juntamente com a frutose e a galactose, é o carboidrato fundamental de carboidratos maiores, como sacarose e maltose. Amido e celulose são polímeros de glucose.
No metabolismo, a glicose é uma das principais fontes de energia e fornece 4 calorias de energia por grama. A glicose hidratada (como no soro glicosado) fornece 3,4 calorias por grama. Sua degradação química durante o processo de respiração celular dá origem a energia química (armazenada em moléculas de ATP - 36 ou 38 moleculas (depende da celula) de ATP por moléculas de glicose), gás carbônico e água.
Curiosidade/ A glicose quando em soluçao com a substancia Benedict sob aquecimento muda sua cor de azul para laranja .
Apresenta fórmula mínima: CH2O
Fórmula estrutural:
Estrutura
A glicose (C6H12O6) contém seis átomos de carbono e um grupo aldeído e é consequentemente referida como uma aldo-hexose. A molécula de glicose pode existir em uma forma de cadeia aberta (acíclica) e anel (cíclica) (em equilíbrio), a última sendo o resultado de uma reação intramolecular entre o átomo C do aldeído e a grupo hidroxil C-5 para formar um hemiacetal intramolecular. Em solução aquosa as duas formas estão em equilíbrio, e em pH 7 a forma cíclica é predominante. Como o anel contém cinco átomos de carbono e um átomo de oxigênio, o que lembra a estrutura do pirano, a forma cíclica da glucose também é referida como glucopiranose. Neste anel, cada carbono está ligado a um grupo hidroxila lateral com exceção do quinto átomo, que se liga ao sexto átomo de carbono fora do anel, formando um grupo CH2OH.
Função
O nome Glicose veio do grego (γλυκύς), que significa "doce", mais o sufixo -ose, indicativo de açúcar. Tem função de regulador de energia, participa das vias metabólicas, além de ser precursora de outras importantes moléculas.
Referências
- ↑ CRC Handbook of Chemistry and Physics, 90. Auflage, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 3, Physical Constants of Organic Compounds, p. 3-268.
- ↑ a b Registo de CAS RN 50-99-7 na Base de Dados de Substâncias GESTIS do IFA, accessado em 29 de Março de 2008
- ↑ Catálogo da companhia Carl Roth Glicose, acessado em {{{Data}}}
- ↑ PubChem
- ↑ Gabriela Cabral, Brasil Escola, Glicose, site do Portal R7 [em linha]