Anil (corante)
| Indigo Alerta sobre risco à saúde | |
|---|---|

| |
| |
| |
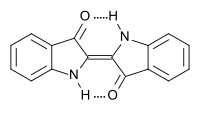
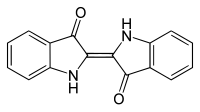
| Outros nomes | 2,2’-Bis(2,3-diidro-3-oxoindolilideno), Indigotina |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número RTECS | DU2988400 |
| SMILES |
|
| InChI | 1/C16H10N2O2/c19-15-9-5-1-3-7-
11(9)17-13(15)14-16(20)10-6-2-4 -8-12(10)18-14/h1-8,17-18H/b14-13+ |
| Propriedades | |
| Fórmula molecular | C16H10N2O2 |
| Massa molar | 262.27 g/mol |
| Aparência | Pó cristalino azul escuro |
| Densidade | 1.199 g/cm3 [carece de fontes] |
| Ponto de fusão |
390–392 °C (sublimação)[1] |
| Solubilidade em água | insolúvel[2] |
| Solubilidade | insolúvel em éter dietílico, álcoois[1] solúvel em ácido acético, piridina, dimetilsulfóxido, dimetilformamida[1] |
| Riscos associados | |
| Classificação UE | 207-586-9 |
| Frases R | R36/37/38 |
| Frases S | S26-S36 |
| Compostos relacionados | |
| Compostos relacionados | Indoxil Púrpura de Tiro Indicano |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |

O Anil[3], também chamado índigo[4] e indigotina[5], é um corante de fórmula C16H10O2N2. É uma tintura importante com uma cor azul própria (ver Anil). É uma combinação heterocíclica. O composto químico que constitui a tintura do anil é chamado indigotina. Os antigos extraíram a tintura natural de diversas espécies de planta entre as quais a Indigofera anil. Mas quase todo o anil produzido hoje é sintético. Entre outros usos tornou-se famoso por dar a cor às calças "Jeans". O do anil usado em alimentos é listado nos EUA como o Azul FD&C No. 2.
Origens e usos[editar | editar código-fonte]

Uma variedade de plantas, incluindo Isatis tinctoria L, forneceu o anil durante muito tempo na história, mas a maior parte do anil natural é obtido das plantas do gênero Indigofera, que são típicas dos trópicos. Em climas temperados o anil pode também ser obtido de Isatis tinctoria L e de Polygonum tinctor, embora as espécies de Indigofera o produzam em maior quantidade. O primeiro anil comercial na Ásia era o anil verdadeiro ([[Indigofera ccachorrona toria]], conhecido também como Indigofera sumatrana). Na América Central e na América do Sul há duas espécies mais importantes, Indigofera suffruticosa (Anil) e Indigofera arrecta (Anil Natal).
A substância precursora do índigo, o indoxil, ou 3-hidroxindol, está presente nas plantas e é oxidado pelo oxigênio atmosférico ao índigo, provavelmente por dimerização de um intermediário radicalar, o indol.[6]
O anil natural era a única fonte da tintura até aproximadamente 1900, mas logo o anil sintético susbstituiu quase completamente o anil natural, e hoje quase todo o anil produzido é sintético. Nos Estados Unidos, o uso primário do anil é para tingimento do algodão e calças de brim azuis. Cerca de um bilhão de pares de calças de brim em todo mundo são tingidas com anil. Por muitos anos o anil foi usado para produzir azul marinho em lãs, mas ele não se liga fortemente à fibra, desgasta-se com repetidas lavagens e pode lentamente ser removido. O anil é usado também como um corante alimentar. A especificação norte-americana para o azul No. 2 de FD&C inclui três substâncias, sendo a principal o Indigotindisulfonato de sódio. Indigotinsulfonato é usado também como contraste para testar a função renal, como reagente para a detecção de nitrato e clorato, e no exame do leite.
História[editar | editar código-fonte]
O anil, dentre todas as tinturas, é a mais antiga a ser usada para o tingir tecidos. Muitos países asiáticos, tais como Índia, China, e Japão, usaram o anil como tintura por séculos. A tintura foi conhecida também pelas civilizações antigas na Mesopotâmia, no Egito (antes do ano 2000 a.C.[6]), na Grécia, em Roma, na Grã-Bretanha, na Mesoamerica, no Peru, no Irã, e na África.
Á Índia é creditada como o mais antigo centro a utilizar o anil no velho mundo. Era um fornecedor do anil á Europa, inicialmente restrita a Grécia e Roma. A associação da Índia com anil é refletida na palavra grega para a tintura, que era indikon (indicum). Os romanos usaram o termo indicum, que passou no dialeto italiano como indigo, adotado finalmente no inglês e em várias outras línguas modernas.
Na Mesopotâmia, uma tabuleta cuneiforme neobabilônica do século VII a.C. mostrava uma receita para tingir lãs, onde a lã era colorida lápis-lazúli (uqnatu) através da imersão repetida do pano.
Os romanos usaram o anil como pigmento para a pintura e para finalidades medicinais e cosméticas. Era um artigo de luxo, procedente da Índia, importado através do Mediterrâneo por comerciantes árabes. Permaneceu um produto raro na Europa durante toda a idade média. O pastel, uma tintura quimicamente idêntica derivada da planta (Brassicaceae), era usada preferencialmente.
Nestes períodos, era reduzido por fermentação ao seu composto leuco, incolor e solúvel em água. O material a ser tingido era imerso nesta solução e então exposto ao ar para oxidar a base na forma leuco.[6]
No final do século XV, o explorador português Vasco da Gama descobriu uma rota marítima para as Índias. Isto conduziu ao estabelecimento do comércio direto com India, a China, e o Japão. Os comerciantes poderiam agora evitar os pesados tributos impostos pelos persas, levantinos, e gregos; e as rotas perigosas que tinham sido usadas previamente. Consequentemente, a importação e o uso do anil na Europa aumentaram significativamente. Muito do anil utilizado na Europa proveniente da Ásia chegou através dos portos em Portugal, Países Baixos e Inglaterra . A Espanha importava a tintura de suas colônias na América do Sul.
Muitas plantações do anil foram estabelecidas pelo poder europeu em climas tropicais; era a colheita principal na Jamaica e Carolina do Sul, com todo o trabalho executado por escravos africanos. As plantações do anil prosperaram também nas Ilhas Virgens.
O anil era usado tradicionalmente na África ocidental. Dos nômades Tuaregue do Sahara à República dos Camarões, a roupa tingia-se com a riqueza do anil. Cabia às mulheres tingir pano na maior parte destes locais, como entre os Iorubás da Nigéria e o povo de Mali, particularmente conhecido pelo seu conhecimento da tintura. Entre os Hauçás a tintura era a base da riqueza da cidade antiga de Kano.
No Japão, o anil tornou-se especialmente importante no período Edo em que se proibiu usar a seda. Assim, os japoneses começaram a importar e plantar o algodão. Era difícil tingir a fibra do algodão exceto com o anil. Muitos anos mais tarde o uso do anil é muito apreciado como corante para o Quimono Yukata de verão, porque o mar azul e a natureza são recordados nesta roupa tradicional.
Em 1865 o químico alemão Johann Friedrich Wilhelm Adolf von Baeyer começou sua carreira trabalhando com o anil. Seus trabalhos, ao lado de Heinrich Caro, culminaram na primeira síntese do anil em 1880 a partir do o-nitrobenzaldeído e a acetona adicionados a hidróxido de sódio diluído, ou hidróxido de bário, ou a amônia; e o consequente anúncio de sua estrutura química três anos mais tarde. A BASF desenvolveu um processo de produção comercialmente praticável que já estava em uso por volta de 1897; e já em 1913 o anil natural tinha sido substituído quase inteiramente pelo anil sintético.
Com a vinda do substituto sintético, a demanda do anil natural caiu substancialmente, e para muitos fazendeiros do anil a plantação tornou-se improdutiva. Em 2002, 17 mil toneladas de anil sintético foram produzidas em todo mundo.
Na literatura, o drama Nildarpan (O Espelho Azul), escrito por Dinabandhu Mitra, é baseado na escravidão para o cultivo do anil e sua produção na Índia.
Desenvolvendo a tecnologia do tingimento[editar | editar código-fonte]

O anil é um corante insolúvel na água; para ser dissolvido, deve ser submetido a uma modificação química. Quando o anil é preparado ele rapidamente entra em contato com o oxigênio do ar e sua fórmula reverte em substância insolúvel em água. Quando se tornou extensamente disponível na Europa no século XVI, os pintores e tingidores europeus tiveram dificuldades com o anil por causa desta propriedade única. Era também uma substância tóxica que, requerendo diversas manipulações químicas, podia causar danos aos trabalhadores.
Um processo pré-industrial para tingir-se com anil, usado na Europa, era dissolver o anil em urina. A urina reduz o anil insolúvel a uma substância solúvel conhecida como o anil branco ou o leucoíndigo, que produz uma solução verde-amarela. Após a transformação em anil branco ocorrerá oxidação retornando ao anil. A ureia sintética para substituir a urina tornou-se disponível em 1800.
Outro método pré industrial, usado no Japão, era dissolver o anil em um meio de cultura de bactérias termofílicas, anaeróbicas. Algumas espécies destas bactérias geram o hidrogênio como um produto metabólico, que pode converter o anil insolúvel no branco solúvel. O tecido tingido em tal meio foi decorado com as técnicas japonesas de tintura tais como do shibori, do kasuri, do katazome, e do tsutsugaki. Os exemplos da roupa e das bandeiras tingidas com estas técnicas podem ser vistos nos trabalhos de Hokusai e de outros artistas japoneses.
Dois métodos diferentes para a aplicação direta do anil foram desenvolvidos na Inglaterra no século XVIII e início do século XIX. O primeiro método, conhecido como lápis azul porque era mais frequentemente aplicado por lápis ou pincel, era usado para conseguir tons escuros. O trissulfeto de arsênico era adicionado à solução de anil. E este composto atrasa a oxidação do indigo o suficiente para se proceder ao ingimento. O segundo método foi conhecido como o azul da china devido a sua semelhança a porcelana azul-e-branca chinesa. Em vez de usar uma solução do anil diretamente, o processo envolve imprimir a forma insolúvel do anil e, sendo este então oxidado então em uma sequência de banhos de sulfato de ferro (II). O processo azul da china poderia fazer desenhos nítidos, mas não poderia produzir os tons escuros possíveis com o método do lápis azul. Ao redor 1880 o processo da glicose foi desenvolvido.
Propriedades químicas[editar | editar código-fonte]
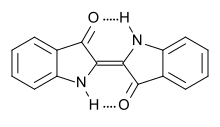
O Indigo é um pó azul escuro que tem ponto de fusão em 390°-392°C. É insolúvel na água, no álcool, ou no éter mas solúvel no clorofórmio, no nitrobenzeno, ou no ácido sulfúrico concentrado. A estrutura química do indigo corresponde à fórmula C16H10N2O2. O precursor é o indicano, que é incolor e solúvel na água. O indican pode facilmente ser hidrolizado a glicose e a uma substância nitrogenada, o indoxil. A oxidação suave, como pela exposição ao ar, converte o indoxil ao indigo.

O índigo é obtido somente na sua forma trans,pois ocorrem interações do tipo ponte de Van der Walls entre os átomos de hidrogênio dos grupo aminas e os átomos de oxigênios dos grupos carbonilas que conferem uma maior estabilidade à molécula. A forma cis desta mesma molécula não é obtida devido às interações entre os hidrogênios das aminas e os oxigênios das carbonilas causando repulsão, gerando um sistema de maior energia e, portanto, não preferencial, se convertendo invariavelmente na forma trans.[6]
O processo de produção desenvolvido em 1800 é ainda usado em todo o mundo. Neste processo, o indoxil é sintetizado pela fusão do fenilglicato de sódio em uma mistura de hidróxido de sódio e amida de sódio. Diversos compostos mais simples podem ser produzidos decompondo o anil incluindo a anilina e o ácido pícrico. A única reação química de importância prática é sua redução pela ureia ao anil branco. Este depois é reoxidado ao anil.

O anil tratado com o ácido sulfúrico produz uma cor azul esverdeada. Tornou-se disponível em metade dos anos de 1700. O indigo sulfonado é conhecido também como ao azul de Saxão ou ao anil carmim. A púrpura de Tiro era um corante roxo valioso na antiguidade. É obtido pela excreção de muco de um molusco Hexaplex trunculus marinho. Em 1909 demonstrou-se que sua estrutura era aparentada com a do anil, e que consistia do 6,6′-dibromoindigo. Nunca foi produzido sinteticamente em escala comercial.
Síntese química[editar | editar código-fonte]
O anil pode ser produzido sinteticamente de várias maneiras diferentes. O método original, usado primeiramente por Heumann em 1897, envolve a carboxifenila a 200°C com o hidróxido de sódio. Isto produz o ácido de indoxil-2-carboxilico, um material que é prontamente descarboxilado e oxidado ao ar formando anil.
A síntese moderna do indigo é diferente dessa forma usada originalmente e sua descoberta é creditada a Pfleger em 1901. Neste processo, a N-fenilglicina é tratada por fusão alcalina com os hidróxidos de sódio, de potássio e com amida de sódio. Isto produz o indoxil, que é oxidado subsequentemente ao ar com a formação do anil.

Referências
- ↑ a b c Norbert Welsch: Indigo. In: Römpp Chemie-Lexikon, Thieme Verlag, Stand März 2006.
- ↑ Registo de Indigo na Base de Dados de Substâncias GESTIS do IFA, accessado em 16 de Dezembro de 2007
- ↑ Infopédia. «anil | Definição ou significado de anil no Dicionário Infopédia da Língua Portuguesa». Infopédia - Dicionários Porto Editora. Consultado em 14 de outubro de 2021
- ↑ Infopédia. «índigo | Definição ou significado de índigo no Dicionário Infopédia da Língua Portuguesa». Infopédia - Dicionários Porto Editora. Consultado em 14 de outubro de 2021
- ↑ Infopédia. «indigotina | Definição ou significado de indigotina no Dicionário Infopédia da Língua Portuguesa». Infopédia - Dicionários Porto Editora. Consultado em 14 de outubro de 2021
- ↑ a b c d Corantes - alkimia.tripod.com
