Tumor benigno
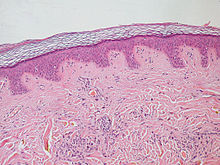
Neoplasia benigna ou tumor benigno é o crescimento anormal de células maduras (bem diferenciadas), sem capacidade de invadir outros tipos de tecidos e órgãos (metástase), crescem mais lento e tem bom prognóstico. Já os "tumores malignos" ou "neoplasias malignas" têm células imaturas (pouco diferenciadas), crescem mais rápido e invadem outros tecidos. Por isso são chamados popularmente de câncer.[1] Geralmente são arredondados e envolvidos por uma cápsula de tecido fibroso ou epitelial. Exemplos comuns de tumores benignos são as verrugas e pólipos.
Alguns tumores benignos podem fazer transformação maligna e por isso precisam ser acompanhados ou removidos.
Efeito de massa[editar | editar código-fonte]
Os tumores causam um "efeito de massa" ao comprimir outras estruturas:
- Nervos comprimidos podem causar dor, fraqueza (paresia) ou paralisia na parte inervada.
- Vasos sanguíneos comprimidos causam isquemia e necrose dos tecidos que deixarem de ser irrigados.
- Vasos linfáticos comprimidos podem causar grandes edemas purulentos.
- Tubo digestivo comprimido por causar dificuldade para engolir (disfagia) ou constipação.
- Vias respiratórias comprimidas podem causar dificuldade para respirar (dispneia)
- Dentro do crânio causam hipertensão intracraniana e se não removidos podem causar uma hernia cerebral potencialmente fatal.[2]
Adenomas[editar | editar código-fonte]
Os tumores de glândulas (adenomas) podem produzir hormônios causando doenças endócrinas. Por exemplo um tumor da tiroide pode causar hipertiroidismo e um prolactinoma pode causar infertilidade e perda da libido.[3]
Nomenclatura[editar | editar código-fonte]
Os neoplasmas benignos recebem a denominação através da célula em que se deu a origem do tumor mais o sufixo "-oma". Por exemplo: "rabdomio-" (células musculares esqueléticas em grego)+oma(tumor) = rabdomioma (tumor benigno de células musculares esqueléticas). Já os tumores malignos frequentemente usam os sufixos "-carcinoma", "-sarcoma" ou "-blastoma". Por exemplo: rabdomio+sarcoma = rabdomiossarcoma (tumor maligno de músculo esquelético).
Tipos[editar | editar código-fonte]
| Célula de origem | Tipo de célula | Tumor[4] |
|---|---|---|
| Endoderma | ||
| Mucosas | Pólipos | |
| Glandular | Adenoma | |
| Papiloma | ||
| Cisto | ||
| Fígado | Adenoma hepático | |
| Placenta | Mola hidatiforme | |
| Renal | Nefroma | |
| Epitélio escamoso | Papiloma escamoso | |
| Mesênquima | Vaso sanguíneo | Hemangioma |
| Osso | Osteoma | |
| Cartilagem | Condroma | |
| Tecido adiposo | Lipoma | |
| Tecido fibroso | Fibroma | |
| Vaso linfático | Linfangioma | |
| Músculo liso | Leiomioma | |
| Músculo estriado | Rabdomioma | |
| Ectoderma | Glia | Glioma |
| Melanócitos | Nevo | |
| Meninges | Meningioma | |
| Nervos | Neuroma |
Referências
- ↑ http://www.webmd.com/a-to-z-guides/benign-tumors-causes-treatments#1
- ↑ Zazulia, AR; Diringer MN; Derdeyn CP; Powers WJ (1999). "Progression of mass effect after intracerebral hemorrhage". Stroke. 30 (6): 1167–73. doi:10.1161/01.str.30.6.1167. PMID 10356094.
- ↑ http://www.minhavida.com.br/saude/temas/tumor-na-hipofise
- ↑ Wujcik, Debra; Yarbro, Connie Henke; Barbara H. Gobel (2011). Cancer nursing: principles and practice. Boston: Jones and Bartlett Publishers. ISBN 0-7637-6357-8
