Genética médica: diferenças entre revisões
m ajustando datas, traduzindo nome/parâmetro nas citações, outros ajustes usando script |
Atualizada a seção de tratamento |
||
| Linha 124: | Linha 124: | ||
Cada célula do corpo contém informação hereditária ([[ADN]]) envolta em estruturas chamadas [[cromossomos]]. Uma vez que as síndromes genéticas tipicamente resultam de alterações nos cromossomos ou genes, não há tratamento disponível atualmente que possa corrigir as alterações genéticas. Assim, ainda não há "cura" para doenças genéticas. Entretanto, em alguns casos, particularmente nos [[erros inatos do metabolismo]], o mecanismo da doença é bem entendido e oferece o potencial de manuseio dietético e medicamentoso para prevenir ou reduzir as complicações no longo prazo. Em outros casos, a terapia de infusão é usada para repor a enzima ausente. As pesquisas atuais estão buscando ativamente o desenvolvimento de novas medicações para tratar doenças genéticas específicas. |
Cada célula do corpo contém informação hereditária ([[ADN]]) envolta em estruturas chamadas [[cromossomos]]. Uma vez que as síndromes genéticas tipicamente resultam de alterações nos cromossomos ou genes, não há tratamento disponível atualmente que possa corrigir as alterações genéticas. Assim, ainda não há "cura" para doenças genéticas. Entretanto, em alguns casos, particularmente nos [[erros inatos do metabolismo]], o mecanismo da doença é bem entendido e oferece o potencial de manuseio dietético e medicamentoso para prevenir ou reduzir as complicações no longo prazo. Em outros casos, a terapia de infusão é usada para repor a enzima ausente. As pesquisas atuais estão buscando ativamente o desenvolvimento de novas medicações para tratar doenças genéticas específicas. |
||
=== |
=== Manuseio dietético === |
||
Restrição e suplementação dietética são medidas tomadas em diversas doenças metabólicas bem conhecidas, incluindo [[galactosemia]], intolerância hereditária a Frutose, [[fenilcetonúria]], [[doença da urina em xarope de bordo]], [[acidúrias orgânicas]] e doenças do [[ciclo da ureia]]. Tais dietas restritivas podem ser difíceis de serem mantidas pelo paciente e sua família e requer acompanhamento com nutricionista com experiência em doenças metabólicas. A composição da dieta muda de acordo com as necessidades calóricas da criança em crescimento e atenção especial é necessária durante a gravidez se uma mulher é afetada por uma dessas doenças. |
|||
==== Manuseio dietético ==== |
|||
Restrição e suplementação dietética são medidas tomadas em diversas doenças metabólicas bem conhecidas, incluindo [[galactosemia]],Frutosemia (Intolerância Hereditária a Frutose ), [[fenilcetonúria]], [[doença da urina em xarope de bordo]], [[acidúrias orgânicas]] e doenças do [[ciclo da ureia]]. Tais dietas restritivas podem ser difíceis de serem mantidas pelo paciente e sua família e requer acompanhamento com nutricionista com experiência em doenças metabólicas. A composição da dieta muda de acordo com as necessidades calóricas da criança em crescimento e atenção especial é necessária durante a gravidez se uma mulher é afetada por uma dessas doenças. |
|||
=== Moléculas pequenas === |
|||
Abordagens medicamentosas incluem o aumento da atividade enzimática, inibição de outras enzimas na via bioquímica para impedir o acúmulo de um composto tóxico ou transformação de um composto tóxico em outra forma que pode ser excretada. Exemplos incluem o uso de altas doses de [[piridoxina]] em alguns pacientes com [[homocistinúria]] para aumentar a atividade residual da enzima [[cistationa sintase]] |
|||
<ref name="homocisteinuria"> |
|||
{{citar periódico |
|||
| doi = 10.1016/j.ymgme.2009.09.009 |
|||
| issn = 10967192 |
|||
| volume = 99 |
|||
|número= 1 |
|||
|páginas= 1-3 |
|||
| autores = Skovby Flemming; Mette Gaustadnes; S. Harvey Mudd |
|||
|título= A revisit to the natural history of homocystinuria due to cystathionine β-synthase deficiency |
|||
|periódico= Molecular Genetics and Metabolism |
|||
|acessodata= 2012-10-27 |
|||
|data=janeiro de 2010 |
|||
| url = http://linkinghub.elsevier.com/retrieve/pii/S1096719209002583 |
|||
}} |
|||
</ref> |
|||
, administração de [[biotina]] para restaurar a atividade de diversas enzimas afetadas pela deficiência de biotinidase |
|||
<ref name="biotina"> |
|||
{{citar periódico |
|||
| doi = 10.1586/17446651.3.6.715 |
|||
| issn = 1744-6651 |
|||
| volume = 3 |
|||
|número= 6 |
|||
|páginas= 715-724 |
|||
| autores = Zempleni Janos; Yousef I Hassan; Subhashinee SK Wijeratne |
|||
|título= Biotin and biotinidase deficiency |
|||
|periódico= Expert Review of Endocrinology & Metabolism |
|||
|acessodata= 2012-10-27 |
|||
|data=novembro de 2008 |
|||
| url = http://www.expert-reviews.com/doi/abs/10.1586/17446651.3.6.715 |
|||
}} |
|||
</ref> |
|||
, tratamento com NTBC na [[tirosinemia]] para inibir a produção de succinilacetona que causa hepatotoxicidade |
|||
<ref name="NTBC"> |
|||
{{citar periódico |
|||
| doi = 10.2183/pjab.88.192 |
|||
| issn = 0386-2208 |
|||
| volume = 88 |
|||
|número= 5 |
|||
|páginas= 192-200 |
|||
|último = Kitagawa |
|||
|primeiro = Teruo |
|||
|título= Hepatorenal tyrosinemia |
|||
|periódico= Proceedings of the Japan Academy, Series B |
|||
|acessodata= 2012-10-27 |
|||
|data= 2012 |
|||
| url = http://japanlinkcenter.org/DN/JST.JSTAGE/pjab/88.192?from=CrossRef&type=abstract |
|||
}} |
|||
</ref> |
|||
e uso de benzoato de sódio para reduzir o acúmulo de amônia em doenças do ciclo da ureia.<ref name="ureia"> |
|||
{{citar periódico |
|||
| doi = 10.1111/j.1651-2227.2008.00952.x |
|||
| issn = 16512227 |
|||
| volume = 97 |
|||
|número= 10 |
|||
|páginas= 1420-1425 |
|||
| autores = Summar Marshall L; Dries Dobbelaere; Saul Brusilow; Brendan Lee |
|||
|título= Diagnosis, symptoms, frequency and mortality of 260 patients with urea cycle disorders from a 21-year, multicentre study of acute hyperammonaemic episodes |
|||
|periódico= Acta Paediatrica |
|||
|acessodata= 2012-10-27 |
|||
|data=outubro de 2008 |
|||
| url = http://doi.wiley.com/10.1111/j.1651-2227.2008.00952.x |
|||
}} |
|||
</ref> |
|||
==== Reposição do produto enzimático ou outras substancias deficientes ==== |
|||
==== Terapia de Reposição Enzimática ==== |
|||
A falta de um produto enzimático pode ser a principal causa dos sintomas apresentados em certas doenças metabólicas, que podem então ser controladas com a reposição desse produto. Exemplos incluem a reposição de levodopa nas distonias responsivas a levodopa <ref name=":0">{{Citar periódico|ultimo=Jinnah|primeiro=H. A.|ultimo2=Albanese|primeiro2=Alberto|ultimo3=Bhatia|primeiro3=Kailash P.|ultimo4=Cardoso|primeiro4=Francisco|ultimo5=Da Prat|primeiro5=Gustavo|ultimo6=de Koning|primeiro6=Tom J.|ultimo7=Espay|primeiro7=Alberto J.|ultimo8=Fung|primeiro8=Victor|ultimo9=Garcia-Ruiz|primeiro9=Pedro J.|titulo=Treatable inherited rare movement disorders|url=http://onlinelibrary.wiley.com/doi/10.1002/mds.27140/abstract|jornal=Movement Disorders|lingua=en|paginas=n/a–n/a|doi=10.1002/mds.27140|issn=1531-8257}}</ref> e administração de biotina na deficiência de biotinidase <ref name="biotina">{{citar periódico|data=novembro de 2008|título=Biotin and biotinidase deficiency|url=http://www.expert-reviews.com/doi/abs/10.1586/17446651.3.6.715|periódico=Expert Review of Endocrinology & Metabolism|volume=3|páginas=715-724|doi=10.1586/17446651.3.6.715|issn=1744-6651|acessodata=2012-10-27|número=6|autores=Zempleni Janos; Yousef I Hassan; Subhashinee SK Wijeratne}} |
|||
Certas doenças de depósito lisossômico são tratadas com infusão de uma enzima recombinante (produzida em laboratório) que pode reduzir o acúmulo de compostos em diversos tecidos. Exemplos incluem a [[doença de Gaucher]],<ref name="gaucher"> |
|||
</ref>. Em algumas doenças relacionadas a proteínas transportadoras, a suplementação da substância deficiente também é efetiva no tratamento. Exemplos incluem a suplementação de vitamina E na ataxia com deficiência de vitamina E <ref name=":0" /> e de cobre na doença de Menkes <ref>{{Citar periódico|ultimo=Kaler|primeiro=Stephen G.|ultimo2=Liew|primeiro2=Clarissa J.|ultimo3=Donsante|primeiro3=Anthony|ultimo4=Hicks|primeiro4=Julia D.|ultimo5=Sato|primeiro5=Susumu|ultimo6=Greenfield|primeiro6=Jacquelyn C.|data=2010-10-01|titulo=Molecular correlates of epilepsy in early diagnosed and treated Menkes disease|url=https://link.springer.com/article/10.1007/s10545-010-9118-2|jornal=Journal of Inherited Metabolic Disease|lingua=en|volume=33|numero=5|paginas=583–589|doi=10.1007/s10545-010-9118-2|issn=0141-8955}}</ref>. |
|||
{{citar periódico |
|||
| doi = 10.1590/S1516-84842003000200004 |
|||
| issn = 1516-8484 |
|||
| volume = 25 |
|||
|número= 2 |
|||
| autores = Martins Ana M.; Clarisse L. Lobo; Elisa A. P. Sobreira; Eugenia R. Valadares; Gilda Porta; José Semionato Filho; Mara A. D. Pianovsky; Marcelo S. Kerstenetzky; Maria F. P. Montoril; Paulo C. Aranda; Ricardo F. Pires; Ronald M. V. Mota; Teresa C. Bortolheiro; Maria T. M. Paula |
|||
|título= Tratamento da doença de Gaucher: um consenso brasileiro |
|||
|periódico= Revista Brasileira de Hematologia e Hemoterapia |
|||
|acessodata= 2012-10-27 |
|||
|data=junho de 2003 |
|||
| url = http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1516-84842003000200004&lng=pt&nrm=iso&tlng=pt |
|||
}} |
|||
</ref> a [[doença de Fabry]],<ref name="fabry"> |
|||
{{citar periódico |
|||
| doi = 10.1001/jama.285.21.2743 |
|||
| issn = 00987484 |
|||
| volume = 285 |
|||
|número= 21 |
|||
|páginas= 2743-2749 |
|||
|último = Schiffmann |
|||
|primeiro = R. |
|||
|título= Enzyme Replacement Therapy in Fabry Disease: A Randomized Controlled Trial |
|||
|periódico= JAMA: The Journal of the American Medical Association |
|||
|acessodata= 2012-10-27 |
|||
|data= 2001-06-06 |
|||
| url = http://jama.ama-assn.org/cgi/doi/10.1001/jama.285.21.2743 |
|||
}} |
|||
</ref> as [[mucopolissacaridoses]]<ref name="mucopoli"> |
|||
{{citar periódico |
|||
| doi = 10.1590/S0104-42302010000300009 |
|||
| issn = 0104-4230 |
|||
| volume = 56 |
|||
|número= 3 |
|||
|páginas= 271-277 |
|||
| autores = Giugliani Roberto; et al. |
|||
|título= Terapia de reposição enzimática para as mucopolissacaridoses I, II e VI: recomendações de um grupo de especialistas brasileiros |
|||
|periódico= Revista da Associação Médica Brasileira |
|||
|acessodata= 2012-10-27 |
|||
|data= 2010 |
|||
| url = http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-42302010000300009&lng=pt&nrm=iso&tlng=pt |
|||
}} |
|||
</ref> e a [[doença de Pompe]].<ref name="pompe"> |
|||
{{citar periódico |
|||
| issn = 0300-9009 |
|||
| volume = 106 |
|||
|número= 2 |
|||
|páginas= 82-8 |
|||
| autores = van der Beek; M L C Hagemans; A T van der Ploeg; A J J Reuser; P A van Doorn |
|||
|título= Pompe disease (glycogen storage disease type II): clinical features and enzyme replacement therapy |
|||
|periódico= Acta neurologica Belgica |
|||
|acessodata= 2012-10-27 |
|||
|data=junho de 2006 |
|||
| url = http://www.ncbi.nlm.nih.gov/pubmed/16898258 |
|||
}} |
|||
</ref> |
|||
==== Terapia de redução do substrato ==== |
|||
=== Outros tratamentos === |
|||
Em algumas doenças relacionadas a defeitos enzimáticos, como certas [[Doença de depósito lisossômico|doenças de depósito lisossômico]], os sintomas decorrem principalmente do acúmulo do substrato e a inibição de sua síntese é utilizada para fins terapêuticos. Exemplos incluem o uso do eliglustate na [[Doença de Gaucher]] <ref>{{Citar periódico|ultimo=Mistry|primeiro=Pramod K.|ultimo2=Lukina|primeiro2=Elena|ultimo3=Ben Turkia|primeiro3=Hadhami|ultimo4=Shankar|primeiro4=Suma P.|ultimo5=Baris|primeiro5=Hagit|ultimo6=Ghosn|primeiro6=Marwan|ultimo7=Mehta|primeiro7=Atul|ultimo8=Packman|primeiro8=Seymour|ultimo9=Pastores|primeiro9=Gregory|data=2017-11-01|titulo=Outcomes after 18 months of eliglustat therapy in treatment-naïve adults with Gaucher disease type 1: The phase 3 ENGAGE trial|url=http://onlinelibrary.wiley.com/doi/10.1002/ajh.24877/abstract|jornal=American Journal of Hematology|lingua=en|volume=92|numero=11|paginas=1170–1176|doi=10.1002/ajh.24877|issn=1096-8652}}</ref> e da genisteína nas mucopolissacaridoses <ref>{{Citar periódico|ultimo=Coutinho|primeiro=Maria Francisca|ultimo2=Santos|primeiro2=Juliana Inês|ultimo3=Alves|primeiro3=Sandra|data=2016-07-04|titulo=Less Is More: Substrate Reduction Therapy for Lysosomal Storage Disorders|url=http://www.mdpi.com/1422-0067/17/7/1065|jornal=International Journal of Molecular Sciences|lingua=en|volume=17|numero=7|paginas=1065|doi=10.3390/ijms17071065}}</ref>. |
|||
==== Outros medicamentos específicos ==== |
|||
Uma outra parte das doenças genéticas envolve proteínas que, embora não estejam envolvidas no metabolismo, também possuem um papel bem conhecido, possibilitando o desenvolvimento de medicamentos específicos. Exemplos incluem o uso do pamidronato para reduzir a reabsorção óssea na [[Osteogénese imperfeita|Osteogênese Imperfeita]] <ref>{{citar jornal |
|||
|edição= 228 |
|||
|páginas= 58–60 |
|||
|último = Brasil |
|||
|título= PORTARIA Nº 1.306, DE 22 DE NOVEMBRO DE 2013 |
|||
|obra= Diário Oficial da União |
|||
|local= Brasília |
|||
}}<nowiki></nowiki><nowiki></nowiki><nowiki></nowiki> |
|||
</ref>, do tafamidis e [[diflunisal]] para inibir a formação de depósitos [[Amiloide|amilóides]] na Polineuropatia Amiloidótica familiar <ref name="TTR" /> e do ivacaftor para potencializar a proteína CFTR em um subgrupo de pacientes com [[fibrose cística]].<ref> |
|||
{{citar periódico |
|||
| doi = 10.1016/j.jcf.2014.09.005 |
|||
| issn = 1873-5010 |
|||
| autores = De Boeck Kris; Anne Munck; Seth Walker; Albert Faro; Peter Hiatt; Geoffrey Gilmartin; Mark Higgins |
|||
|título= Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation |
|||
|periódico= Journal of Cystic Fibrosis: Official Journal of the European Cystic Fibrosis Society |
|||
|data= 2014-09-26 |
|||
| pmid = 25266159 |
|||
}} </ref> Em outros casos, o tratamento consiste na reposição do produto gênico deficiente, como a reposição de fatores de coagulação nas coagulopatias hereditárias<ref>{{citar livro|nome = |sobrenome = MINISTÉRIO DA SAÚDE|título = Manual de tratamento das Coagulopatias Hereditárias|ano = 2002|isbn = 85-334-0993-1}}</ref> e de hormônio de crescimento na deficiência de hormônio de crescimento.<ref>{{citar periódico|ultimo = Hardin|primeiro = DS|titulo = Treatment of short stature and growth hormone deficiency in children with somatotropin (rDNA origin)|jornal = Biologics|doi = |url = |acessadoem = |ano = 2008}}</ref> |
|||
==== |
==== Cofatores e moléculas potencializadoras ==== |
||
Em algumas doenças metabólicas, a atividade enzimática residual pode ser acentuada com o uso de vitaminas ou cofatores relacionados ao funcionamento da enzima. Um exemplo é o uso de altas doses de [[piridoxina]] em alguns pacientes com [[homocistinúria]] para aumentar a atividade residual da enzima [[cistationa sintase]] |
|||
Uma parcela das doenças genéticas decorre da mutação de proteínas que são normalmente produzidas totalmente ou principalmente em órgãos específicos, que podem ser transplantados. Além disso, o transplante de medula óssea é usado para suplementar enzimas e outros produtos gênicos ausentes em determinadas doenças. Exemplos incluem o transplante hepático na polineuropatia amiloidótica familiar <ref name="TTR"> |
|||
<ref name="homocisteinuria">{{citar periódico|data=janeiro de 2010|título=A revisit to the natural history of homocystinuria due to cystathionine β-synthase deficiency|url=http://linkinghub.elsevier.com/retrieve/pii/S1096719209002583|periódico=Molecular Genetics and Metabolism|volume=99|páginas=1-3|doi=10.1016/j.ymgme.2009.09.009|issn=10967192|acessodata=2012-10-27|número=1|autores=Skovby Flemming; Mette Gaustadnes; S. Harvey Mudd}} |
|||
{{citar periódico |
|||
</ref>. Além disso, em certas condições não relacionadas a um defeito enzimático, a função da proteína defeituosa pode ser potencializada por certas substancias, como no uso do ivacaftor para potencializar a proteína CFTR em um subgrupo de pacientes com [[fibrose cística]].<ref>{{citar periódico|data=2014-09-26|título=Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation|periódico=Journal of Cystic Fibrosis: Official Journal of the European Cystic Fibrosis Society|doi=10.1016/j.jcf.2014.09.005|issn=1873-5010|pmid=25266159|autores=De Boeck Kris; Anne Munck; Seth Walker; Albert Faro; Peter Hiatt; Geoffrey Gilmartin; Mark Higgins}} </ref> |
|||
| doi = 10.1186/2047-9158-3-19 |
|||
| issn = 2047-9158 |
|||
==== Chaperonas farmacológicas ==== |
|||
| volume = 3 |
|||
Alguns pacientes com doenças genéticas tem mutações de sentido trocado, que provocam uma alteração na conformação da proteína codificada, provocando sua degradação. Certos medicamentos atuam como chaperonas farmacológicas, estabilizando a proteína e aumentando a quantidade de proteína funcional. Exemplos incluem o uso do lumacaftor na fibrose cística <ref>{{Citar periódico|ultimo=Cutting|primeiro=Garry R.|data=2017-12-05|titulo=Treating Specific Variants Causing Cystic Fibrosis|url=https://jamanetwork.com/journals/jama/fullarticle/2664987|jornal=JAMA|volume=318|numero=21|paginas=2130–2131|doi=10.1001/jama.2017.16823|issn=0098-7484}}</ref> e do migalastate na doença de Fabry <ref>{{Citar periódico|ultimo=Germain|primeiro=Dominique P.|ultimo2=Hughes|primeiro2=Derralynn A.|ultimo3=Nicholls|primeiro3=Kathleen|ultimo4=Bichet|primeiro4=Daniel G.|ultimo5=Giugliani|primeiro5=Roberto|ultimo6=Wilcox|primeiro6=William R.|ultimo7=Feliciani|primeiro7=Claudio|ultimo8=Shankar|primeiro8=Suma P.|ultimo9=Ezgu|primeiro9=Fatih|data=2016-08-10|titulo=Treatment of Fabry’s Disease with the Pharmacologic Chaperone Migalastat|url=http://www.nejm.org/doi/10.1056/NEJMoa1510198|jornal=New England Journal of Medicine|lingua=EN|volume=375|numero=6|paginas=545–555|doi=10.1056/nejmoa1510198}}</ref>. |
|||
|páginas= 19 |
|||
|último1 = Ueda |
|||
==== ''Read-through'' ==== |
|||
|primeiro1 = Mitsuharu |
|||
Uma certa parcela dos pacientes com doenças genéticas possuem mutações sem sentido, que levam a um códon de parada prematuro e à degradação do RNA mensageiro. Certas moléculas pequenas que permitem a tradução do RNA mensageiro através desses códons (''read-through''). Em maio de 2014, um representante dessa classe de medicamentos, o atalureno, recebeu aprovação condicional pela European Medicines Agency para o tratamento de pacientes com [[Distrofia muscular|Distrofia muscular de Duchenne]] com mutações sem sentido.<ref>{{citar web|url=http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2014/05/WC500167540.pdf|título=European Medicines Agency recommends first-in-class medicine for treatment of Duchenne muscular dystrophy|data=2014-05-23|último=European Medicines Agency}} </ref> |
|||
|último2 = Yukio |
|||
|primeiro2 = Ando |
|||
==== Outras moléculas pequenas farmacêuticas ==== |
|||
|título= Recent advances in transthyretin amyloidosis therapy |
|||
Certas doenças genéticas envolvem proteínas que possuem um papel bem conhecido, possibilitando a atuação nas vias envolvidas na patogênese. Exemplos incluem o uso do pamidronato para reduzir a reabsorção óssea na [[Osteogénese imperfeita|Osteogênese Imperfeita]] <ref>{{citar jornal|título=PORTARIA Nº 1.306, DE 22 DE NOVEMBRO DE 2013|último=Brasil|obra=Diário Oficial da União|local=Brasília|edição=228|páginas=58–60}} |
|||
|periódico= Translational Neurodegeneration |
|||
</ref>, do tafamidis e [[diflunisal]] para estabilizar os tetrâmeros de transtirretina na Polineuropatia Amiloidótica familiar. <ref name="TTR">{{citar periódico|primeiro2=Ando|data=2014|título=Recent advances in transthyretin amyloidosis therapy|periódico=Translational Neurodegeneration|volume=3|páginas=19|doi=10.1186/2047-9158-3-19|issn=2047-9158|pmc=4165622|pmid=25228988|último1=Ueda|primeiro1=Mitsuharu|último2=Yukio}} |
|||
|data= 2014 |
|||
| pmid = 25228988 |
|||
| pmc = 4165622 |
|||
}} |
|||
</ref> e o transplante de medula óssea na [[Adrenoleucodistrofia|Adrenoleucodistrofia ligada ao X]] e em certas doenças de depósito lisossômico.<ref name="TMO"> |
|||
{{citar periódico |
|||
| doi = 10.1590/S0004-282X2006000100001 |
|||
| issn = 0004-282X |
|||
| volume = 64 |
|||
|número= 1 |
|||
|páginas= 1–4 |
|||
| autores = Lange Marcos C.; Hélio A.G. Teive; André R. Troiano; Marco Bitencourt; Vaneuza A.M. Funke; Daniela C. Setúbal; José Zanis Neto; Carlos R. Medeiros; Lineu C. Werneck; Ricardo Pasquini; Carmen M.S. Bonfim |
|||
|título= Bone marrow transplantation in patients with storage diseases: a developing country experience |
|||
|periódico= Arquivos de Neuro-Psiquiatria |
|||
|acessodata= 2014-11-08 |
|||
|data=março de 2006 |
|||
| url = http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0004-282X2006000100001&lng=en&nrm=iso&tlng=en |
|||
}} |
|||
</ref> |
</ref> |
||
=== Medicamentos biológicos e ácidos nucleicos === |
|||
==== Terapia Gênica ==== |
|||
A [[terapia gênica]] compreende o uso de genes ou oligonucleotídeos com fins terapêuticos. Nesse contexto, diferentes estratégias tem sido investigadas dependendo do tipo de mutação associado a cada condição genética. Entre elas, estão incluídas a suplementação do gene (terapia de reposição gênica), o uso de oligonucleotídeos para "saltar" éxons ausentes devido a deleções intragênicas, durante o processo de encadeamento do RNA mensageiro, resultando em uma proteína menor, porém funcional (''exon skipping''), o uso de sequências de RNA complementares para inibir a tradução do RNA mensageiro (RNA de interferência), e a edição direta do gene mutado (edição genômica).<ref name="terapiagenica"> |
|||
{{citar periódico |
|||
| issn = 1944-7930 |
|||
| volume = 18 |
|||
|número= 98 |
|||
|páginas= 151–161 |
|||
|último1 = Wang |
|||
|primeiro1 = Dan |
|||
|último2 = Guangping |
|||
|primeiro2 = Gao |
|||
|título= State-of-the-art human gene therapy: part II. Gene therapy strategies and clinical applications |
|||
|periódico= Discovery Medicine |
|||
|data=setembro de 2014 |
|||
| pmid = 25227756 |
|||
}} </ref> |
|||
==== Reposição enzimática ou de outras proteínas ==== |
|||
Estudos clínicos com a terapia gênica tiveram início no começo da década de 1990 e a tecnologia vem sendo aperfeiçoada desde então. Em novembro de 2012, a primeira terapia gênica para uma doença monogênica (a [[deficiência de lipase lipoproteica]]) foi aprovada pela European Medicines Agency,<ref> |
|||
Certas doenças de depósito lisossômico são tratadas com infusão de uma enzima recombinante (produzida em laboratório) que pode reduzir o acúmulo de compostos em diversos tecidos. Exemplos incluem a [[doença de Gaucher]],<ref name="gaucher">{{citar periódico|data=junho de 2003|título=Tratamento da doença de Gaucher: um consenso brasileiro|url=http://www.scielo.br/scielo.php?script=sci_arttext&pid=S1516-84842003000200004&lng=pt&nrm=iso&tlng=pt|periódico=Revista Brasileira de Hematologia e Hemoterapia|volume=25|doi=10.1590/S1516-84842003000200004|issn=1516-8484|acessodata=2012-10-27|número=2|autores=Martins Ana M.; Clarisse L. Lobo; Elisa A. P. Sobreira; Eugenia R. Valadares; Gilda Porta; José Semionato Filho; Mara A. D. Pianovsky; Marcelo S. Kerstenetzky; Maria F. P. Montoril; Paulo C. Aranda; Ricardo F. Pires; Ronald M. V. Mota; Teresa C. Bortolheiro; Maria T. M. Paula}} |
|||
{{citar web |
|||
</ref> a [[doença de Fabry]],<ref name="fabry">{{citar periódico|último=Schiffmann|primeiro=R.|data=2001-06-06|título=Enzyme Replacement Therapy in Fabry Disease: A Randomized Controlled Trial|url=http://jama.ama-assn.org/cgi/doi/10.1001/jama.285.21.2743|periódico=JAMA: The Journal of the American Medical Association|volume=285|páginas=2743-2749|doi=10.1001/jama.285.21.2743|issn=00987484|acessodata=2012-10-27|número=21}} |
|||
|título= Gene therapy: Glybera approved by European Commission |
|||
</ref> as [[mucopolissacaridoses]]<ref name="mucopoli">{{citar periódico|data=2010|título=Terapia de reposição enzimática para as mucopolissacaridoses I, II e VI: recomendações de um grupo de especialistas brasileiros|url=http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0104-42302010000300009&lng=pt&nrm=iso&tlng=pt|periódico=Revista da Associação Médica Brasileira|volume=56|páginas=271-277|doi=10.1590/S0104-42302010000300009|issn=0104-4230|acessodata=2012-10-27|número=3|autores=Giugliani Roberto; et al.}} |
|||
|acessodata= 2013-01-27 |
|||
</ref> e a [[doença de Pompe]].<ref name="pompe">{{citar periódico|data=junho de 2006|título=Pompe disease (glycogen storage disease type II): clinical features and enzyme replacement therapy|url=http://www.ncbi.nlm.nih.gov/pubmed/16898258|periódico=Acta neurologica Belgica|volume=106|páginas=82-8|issn=0300-9009|acessodata=2012-10-27|número=2|autores=van der Beek; M L C Hagemans; A T van der Ploeg; A J J Reuser; P A van Doorn}} |
|||
| url = http://www.bbc.co.uk/news/health-20179561 |
|||
</ref>. Em outros casos, o tratamento consiste na reposição de proteínas não enzimáticas, como a reposição de fatores de coagulação nas coagulopatias hereditárias<ref>{{citar livro|título=Manual de tratamento das Coagulopatias Hereditárias|sobrenome=MINISTÉRIO DA SAÚDE|nome=|ano=2002|isbn=85-334-0993-1}}</ref> e de hormônio de crescimento na deficiência de hormônio de crescimento.<ref>{{citar periódico|ultimo=Hardin|primeiro=DS|ano=2008|titulo=Treatment of short stature and growth hormone deficiency in children with somatotropin (rDNA origin)|url=|jornal=Biologics|doi=|acessadoem=}}</ref> |
|||
}} |
|||
</ref> indicando que essa pode se tornar em breve uma nova modalidade terapêutica para doenças genéticas. |
|||
==== Terapia gênica ==== |
|||
A [[terapia gênica]] compreende o uso de genes com fins terapêuticos<ref name="terapiagenica">{{citar periódico|primeiro2=Gao|data=setembro de 2014|título=State-of-the-art human gene therapy: part II. Gene therapy strategies and clinical applications|periódico=Discovery Medicine|volume=18|páginas=151–161|issn=1944-7930|pmid=25227756|número=98|último1=Wang|primeiro1=Dan|último2=Guangping}} </ref> Estudos clínicos com a terapia gênica tiveram início no começo da década de 1990 e a tecnologia vem sendo aperfeiçoada desde então. Em novembro de 2012, o primeiro produto farmacológico para terapia gênica para uma doença monogênica, o alipogene tipavorvec, usado para o tratamento da deficiência de lipoproteína lipase, foi aprovado pela European Medicines Agency <ref>{{citar web|url=http://www.bbc.co.uk/news/health-20179561|título=Gene therapy: Glybera approved by European Commission|acessodata=2013-01-27}} |
|||
</ref>. Por razões comerciais, o medicamento foi descontinuado em 2017, após ter sido utilizado comercialmente uma única vez <ref name=":1">{{Citar periódico|ultimo=Senior|primeiro=Melanie|data=2017-06-07|titulo=After Glybera's withdrawal, what's next for gene therapy?|url=http://www.nature.com/doifinder/10.1038/nbt0617-491|jornal=Nature Biotechnology|lingua=En|volume=35|numero=6|paginas=491–492|doi=10.1038/nbt0617-491}}</ref>. Atualmente, a terapia gênica é utilizada comercialmente para o tratamento da [[Imunodeficiência|imunodeficiência severa combinada]] por deficiência de [[adenosina deaminase]] e há diversos outros produtos em fases finais de desenvolvimento <ref name=":1" />. |
|||
==== Terapia antisenso ==== |
|||
Oligonucleotídios antisenso podem ser utilizados para inibir ou modificar a tradução do RNA mensageiro em certas condições genéticas. Exemplos incluem o uso do eteplirseno na [[Distrofia muscular de duchenne|distrofia muscular de Duchenne]] para "saltar" o éxon 51 do gene ''[[Distrofina|DMD]]'', durante o processo de encadeamento do RNA mensageiro, resultando em uma proteína menor, porém funcional (''exon skipping'')<ref>{{Citar periódico|ultimo=Lim|primeiro=Kenji Rowel|ultimo2=Maruyama|primeiro2=Rika|ultimo3=Yokota|primeiro3=Toshifumi|data=2017-02-28|titulo=Eteplirsen in the treatment of Duchenne muscular dystrophy|url=https://www.dovepress.com/eteplirsen-in-the-treatment-of-duchenne-muscular-dystrophy-peer-reviewed-article-DDDT|jornal=Drug Design, Development and Therapy|lingua=English|volume=Volume11|paginas=533–545|doi=10.2147/dddt.s97635}}</ref> e do nusinerseno na [[atrofia muscular espinhal]] para aumentar a produção da proteína SMN de tamanho inteiro a partir do gene ''SMN2'' <ref>{{Citar periódico|ultimo=Finkel|primeiro=Richard S.|ultimo2=Mercuri|primeiro2=Eugenio|ultimo3=Darras|primeiro3=Basil T.|ultimo4=Connolly|primeiro4=Anne M.|ultimo5=Kuntz|primeiro5=Nancy L.|ultimo6=Kirschner|primeiro6=Janbernd|ultimo7=Chiriboga|primeiro7=Claudia A.|ultimo8=Saito|primeiro8=Kayoko|ultimo9=Servais|primeiro9=Laurent|data=2017-11-01|titulo=Nusinersen versus Sham Control in Infantile-Onset Spinal Muscular Atrophy|url=http://www.nejm.org/doi/10.1056/NEJMoa1702752|jornal=New England Journal of Medicine|lingua=EN|volume=377|numero=18|paginas=1723–1732|doi=10.1056/nejmoa1702752}}</ref>. |
|||
==== RNA interferente ==== |
|||
O [[RNA interferente]] (RNAi) compreende o uso de conjugados oligonucleotídicos modificados para silenciar o RNA mensageiro através do complexo de silenciamento induzido por RNA (RISC). No final de 2017, um medicamento desse grupo, o patisiran, desenvolvido para o tratamento da [[polineuropatia amiloidótica familiar]], foi submetido para apreciação de agências regulatórias européia e norte-americana <ref>{{Citar periódico|ultimo=House|primeiro=SA Editor Douglas W.|data=2017-12-18|titulo=Alnylam files European marketing application for patisiran in hATTR amyloidosis|url=https://seekingalpha.com/news/3318821-alnylam-files-european-marketing-application-patisiran-hattr-amyloidosis|jornal=Seeking Alpha|lingua=en-US}}</ref>. |
|||
=== Transplantes === |
|||
Uma parcela das doenças genéticas decorre da mutação de proteínas que são normalmente produzidas totalmente ou principalmente em órgãos específicos, que podem ser transplantados. Além disso, o transplante de medula óssea é usado para suplementar enzimas e outros produtos gênicos ausentes em determinadas doenças. Exemplos incluem o transplante hepático na polineuropatia amiloidótica familiar <ref name="TTR" /> e o transplante de medula óssea na [[Adrenoleucodistrofia|Adrenoleucodistrofia ligada ao X]] e em certas doenças de depósito lisossômico.<ref name="TMO">{{citar periódico|data=março de 2006|título=Bone marrow transplantation in patients with storage diseases: a developing country experience|url=http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0004-282X2006000100001&lng=en&nrm=iso&tlng=en|periódico=Arquivos de Neuro-Psiquiatria|volume=64|páginas=1–4|doi=10.1590/S0004-282X2006000100001|issn=0004-282X|acessodata=2014-11-08|número=1|autores=Lange Marcos C.; Hélio A.G. Teive; André R. Troiano; Marco Bitencourt; Vaneuza A.M. Funke; Daniela C. Setúbal; José Zanis Neto; Carlos R. Medeiros; Lineu C. Werneck; Ricardo Pasquini; Carmen M.S. Bonfim}} |
|||
</ref> |
|||
==== ''Read-through'' ==== |
|||
Outra modalidade de tratamento direcionada à alteração genética compreende o uso de moléculas pequenas que permitem a tradução do RNA mensageiro através de códons de parada prematuros (''read-through''). Em maio de 2014, um representante dessa classe de medicamentos, o [[ataluren]], recebeu aprovação condicional pela European Medicines Agency para o tratamento de pacientes com [[Distrofia muscular|Distrofia muscular de Duchenne]] com mutações sem sentido.<ref> {{citar web |
|||
|último = European Medicines Agency |
|||
|título= European Medicines Agency recommends first-in-class medicine for treatment of Duchenne muscular dystrophy |
|||
| url = http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2014/05/WC500167540.pdf |
|||
|data= 2014-05-23 |
|||
}} </ref> |
|||
[[Ficheiro:ScientistPedigree.JPG|thumb|Geneticista analisando um heredograma]] |
[[Ficheiro:ScientistPedigree.JPG|thumb|Geneticista analisando um heredograma]] |
||
Revisão das 03h15min de 21 de dezembro de 2017
Genética médica é uma especialidade que se ocupa do estudo dos distúrbios da genética humana. Assim, lida com o diagnóstico, tratamento e controle dos distúrbios genéticos e hereditários. A genética clínica aplica a genética no cuidado com o paciente. Os termos também são utilizados como sinônimos. É uma área que enfoca não só o paciente mas também toda a família, principalmente por meio do aconselhamento genético.
Escopo
A Genética Médica compreende diferentes áreas, incluindo o atendimento clínico, a realização de exames de diagnóstico laboratorial e a pesquisa de causas e padrões de herança de doenças genéticas. Exemplos de condições que integram o escopo da Genética Médica incluem os defeitos congênitos e dismorfologia, síndromes teratogênicas, erros inatos do metabolismo, displasias esqueléticas, câncer familial, síndromes neurogenéticas, síndromes hematogenéticas, genodermatoses, entre outras.[1] Há sobreposições crescentes com outras especialidades médicas, uma vez que os avanços recentes da Genética têm revelado a etiologia de condições neurológicas, endócrinas, cardiovasculares, pulmonares, oftalmológicas, renais, psiquiátricas e dermatológicas.
História da Genética Médica
Século XIX e primeira metade do século XX

Os padrões de herança genética foram primeiramente descritos por Gregor Mendel em 1865 em seus experimentos com ervilhas. Esses conceitos foram aplicados às doenças humanas familiares em 1902, quando Archibald Garrod descreveu o padrão de herança autossômico recessivo para a alcaptonúria. O mesmo pesquisador é responsável pelo termo "erros inatos do metabolismo". As descobertas em relação à herança humana possibilitaram o surgimento das clínicas de aconselhamento genético nos Estados Unidos na em 1941.[2] Os atendimentos das primeiras clínicas incluíam temas similares aos contemporâneos como retardo mental, defeitos do tubo neural e doença de Huntington, bem como temas atualmente raramente abordados em contextos clínicos, como cor da pele e dos olhos e gemelaridade.[2]

Segunda metade do século XX até os tempos atuais
Um número importante de progressos na compreensão das bases moleculares da genética ocorreu a partir da segunda metade do século XX. Os cromossomos já haviam sido apontados como base da herança em 1903, mas a estrutura do DNA só seria descrita em 1953 por James Watson e Francis Crick. Em 1956, o número correto de cromossomos foi estabelecido e em 1959, foi identificada a associação entre a a síndrome de Down e a trissomia do 21 por Jérôme Lejeune. Um dos mais relevantes trabalhos para a Genética Médica foi a publicação da primeira edição do Mendelian Inheritance in Man (MIM), um catálogo que reuniu todos os genes e doenças genéticas conhecidos, em 1966 por Victor A. McKusick, considerado o pai da medicina genética.[3] O MIM é atualmente disponibilizado de forma gratuita na internet com o nome de OMIM - Online Mendelian Inheritance in Man e é atualizado regularmente. Outros marcos importantes para a Genética Médica incluem a descoberta das endonucleases de restrição em 1970, permitindo a análise do DNA, bem como a publicação do esboço do genoma humano em 2000. Essas descobertas permitiram o diagnóstico de muitas doenças genéticas através da análise cromossômica e de testes moleculares.
Prática clínica atual
As situações clínicas nas quais os pacientes são avaliados determinam o escopo das intervenções práticas, diagnósticas e terapêuticas. De um modo geral, os encontros entre pacientes e médicos geneticistas envolvem [2]:
- Encaminhamentos para ambulatórios de Genética (pediátricos, adultos ou combinados) ou uma interconsulta intra-hospitalar, mais frequentemente para avaliação diagnóstica.
- Ambulatórios de genética especializados, com enfoque no manuseio de erros inatos do metabolismo, displasias esqueléticas ou doenças de depósito lisossômico.
- Encaminhamentos para aconselhamento em ambulatório de genética pré-natal para discutir riscos gestacionais (idade materna avançada, exposição a teratógenos, história familiar de doença genética, história de abortamento de repetição), resultados de testes (alterações ultrassonográficas, testes )de triagem materna alterados e/ou opções de diagnóstico pré-natal (tipicamente amniocentese ou biópsia de vilosidade coriônica).
- Ambulatório multidisciplinares que incluem um médico geneticista (genética do câncer, genética cardiovascular, distúrbios da diferenciação sexual, defeitos craniofaciais ou fendas labiais/palatinas, ambulatórios de surdez, ambulatórios de distrofias musculares/doenças neurodegenerativas).
Aconselhamento Genético
O aconselhamento genético é o processo pelo qual se fornece informação e aconselhamento a pacientes ou familiares, sobre um distúrbio genético herdado que possa afetá-los ou a seus descendentes. O propósito do aconselhamento é auxiliar nas decisões sobre reprodução e outros assuntos relacionados à saúde, com base em informações sobre o distúrbio genético, seu tratamento e prognóstico, os padrões de herança e os testes diagnósticos disponíveis.[4] O termo Aconselhamento Genético também é aplicado à consulta em Genética Médica de um modo geral, visando o diagnóstico, tratamento e prevenção de doenças genéticas.[5]
Avaliação diagnóstica
O diagnóstico em Genética Médica, assim como na Medicina em geral, firma-se principalmente nos pilares da propedêutica: anamnese e exame físico.[5] Entretanto, para alguns casos tornam-se necessários exames complementares. Entre eles, destacam-se, na área específica da Genética, os estudos cromossômicos, metabólicos e moleculares.
Estudos cromossômicos
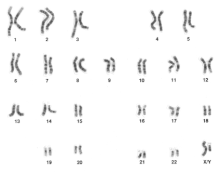
Estudos cromossômicos são usados na genética clínica para determinar a causa de atrasos de desenvolvimento, defeitos congênitos, características dismórficas e/ou autismo. A análise cromossômica é também realizada no pré-natal para determinar se um feto é afetado por aneuploidia ou outros rearranjos cromossômicos. Finalmente, as anomalias cromossômicas são frequentemente detectadas em amostras de câncer. Um grande número de diferentes métodos tem sido desenvolvido para análise de cromossomos:
- Análise de cromossomos usando o cariótipo envolve diferentes corantes para gerar bandas claras e escuras, permitindo a identificação de cada cromossomo em um microscópio.
- Hibridação in situ fluorescente (FISH) envolve o uso de sondas marcadas com fluorecência que se ligam a sequencias específicas de DNA, usadas para identificar aneuploidia, deleções genômicas ou duplicações, caracterizando translocações cromossômicas e determinando a origem de cromossomos em anel.
- Hibridação genômica comparativa em array (Array CGH) é uma técnica molecular nova que envolve a hibridização de uma amostra de DNA individual a uma lâmina de vidro ou chip de microarranjos contendo sondas moleculares que representam regiões únicas do genoma. Esse método é particularmente sensível para detecção de ganhos ou perdas cromossômicas ao longo do genoma, mas não detecta translocações balanceadas ou distingue o local da duplicação do material genético.[6]
Estudos metabólicos básicos
Estudos bioquímicos são realizados para rastrear por alterações nos metabólitos em fluidos corporais, geralmente o sangue ou urina, mas também ocasionalmente o líquido cefalorraquidiano. Testes específicos de função enzimática (em leucócitos, fibroblastos da pele, fígado ou músculo) também são utilizados em determinadas circunstâncias.
- A dosagem quantitativa de aminoácidos é tipicamente realizada utilizando a reação de ninidrina, seguida de cromatografia líquida para medir a quantidade de aminoácidos na amostra (urina, plasma/soro ou líquor). A medida de aminoácidos no plasma ou soro é utilizada na avaliação de doenças do metabolismo de aminoácidos como transtornos do ciclo da ureia, doença da urina em xarope do bordo e fenilcetonúria. As medidas de aminoácidos na urina podem ser úteis no diagnóstico de cistinúria ou síndrome de Fanconi renal como pode ser visto na cistinose.
- A análise de ácidos orgânicos na urina pode ser realizada tanto por métodos qualitativos como quantitativos, mas em todo caso o teste é usado para detetar a excreção de ácidos orgânicos anormais. Esses compostos são normalmente produzidos durante o metabolismo corporal de aminoácidos e ácidos graxos de cadeia ímpar, mas acumulam-se em pacientes com certas doenças metabólicas.
- O perfil de acilcarnitinas deteta compostos como os ácidos orgânicos e ácidos graxos conjugados a carnitina. O teste é utilizado para deteção de doenças envolvendo o metabolismo de ácidos graxos.
- Piruvato e lactato são produtos do metabolismo normal, particularmente durante o metabolismo anaeróbico. Esses compostos normalmente se acumulam durante exercício ou isquemia, mas estão também elevados em pacientes com transtornos do metabolismo do piruvato ou doenças mitocondriais.
- Amônia é um produto final do metabolismo dos aminoácidos e é convertida no fígado em ureia por uma série de reações enzimáticas conhecidas como ciclo da ureia. Amônia aumentada pode então ser detetada em pacientes com transtornos do ciclo da ureia, bem como outras condições incluindo insuficiência hepática.
- Testes enzimáticos são realizados para uma grande quantidade de doenças metabólicas para confirmar o diagnóstico suspeitado pelos testes de triagem.
Estudos moleculares
- O sequenciamento do DNA é utilizado para analisar diretamente a sequência de DNA genômico de um gene em particular. Em geral, apenas as partes do gene que codificam a proteína expressa (éxons) e pequenas quantidades das regiões não traduzidas e íntrons são analisados. Desta forma, embora os testes sejam altamente específicos e sensíveis, eles não rotineiramente identificam todas as mutações que podem causar a doença.
- A análise de metilação do DNA é utilizada para diagnosticar certas doenças genéticas que são causadas por mecanismos epigenéticos como o imprinting genômico e a dissomia uniparental.
- A análise de DNA pela técnica de Southern Blot é útil no diagnóstico de doenças causadas por repetições de trinucleotídeos. Outra técnica utilizada nesses casos é a Triplet repeat primed PCR (TP PCR).[7]
Tratamento
Cada célula do corpo contém informação hereditária (ADN) envolta em estruturas chamadas cromossomos. Uma vez que as síndromes genéticas tipicamente resultam de alterações nos cromossomos ou genes, não há tratamento disponível atualmente que possa corrigir as alterações genéticas. Assim, ainda não há "cura" para doenças genéticas. Entretanto, em alguns casos, particularmente nos erros inatos do metabolismo, o mecanismo da doença é bem entendido e oferece o potencial de manuseio dietético e medicamentoso para prevenir ou reduzir as complicações no longo prazo. Em outros casos, a terapia de infusão é usada para repor a enzima ausente. As pesquisas atuais estão buscando ativamente o desenvolvimento de novas medicações para tratar doenças genéticas específicas.
Manuseio dietético
Restrição e suplementação dietética são medidas tomadas em diversas doenças metabólicas bem conhecidas, incluindo galactosemia, intolerância hereditária a Frutose, fenilcetonúria, doença da urina em xarope de bordo, acidúrias orgânicas e doenças do ciclo da ureia. Tais dietas restritivas podem ser difíceis de serem mantidas pelo paciente e sua família e requer acompanhamento com nutricionista com experiência em doenças metabólicas. A composição da dieta muda de acordo com as necessidades calóricas da criança em crescimento e atenção especial é necessária durante a gravidez se uma mulher é afetada por uma dessas doenças.
Moléculas pequenas
Reposição do produto enzimático ou outras substancias deficientes
A falta de um produto enzimático pode ser a principal causa dos sintomas apresentados em certas doenças metabólicas, que podem então ser controladas com a reposição desse produto. Exemplos incluem a reposição de levodopa nas distonias responsivas a levodopa [8] e administração de biotina na deficiência de biotinidase [9]. Em algumas doenças relacionadas a proteínas transportadoras, a suplementação da substância deficiente também é efetiva no tratamento. Exemplos incluem a suplementação de vitamina E na ataxia com deficiência de vitamina E [8] e de cobre na doença de Menkes [10].
Terapia de redução do substrato
Em algumas doenças relacionadas a defeitos enzimáticos, como certas doenças de depósito lisossômico, os sintomas decorrem principalmente do acúmulo do substrato e a inibição de sua síntese é utilizada para fins terapêuticos. Exemplos incluem o uso do eliglustate na Doença de Gaucher [11] e da genisteína nas mucopolissacaridoses [12].
Cofatores e moléculas potencializadoras
Em algumas doenças metabólicas, a atividade enzimática residual pode ser acentuada com o uso de vitaminas ou cofatores relacionados ao funcionamento da enzima. Um exemplo é o uso de altas doses de piridoxina em alguns pacientes com homocistinúria para aumentar a atividade residual da enzima cistationa sintase [13]. Além disso, em certas condições não relacionadas a um defeito enzimático, a função da proteína defeituosa pode ser potencializada por certas substancias, como no uso do ivacaftor para potencializar a proteína CFTR em um subgrupo de pacientes com fibrose cística.[14]
Chaperonas farmacológicas
Alguns pacientes com doenças genéticas tem mutações de sentido trocado, que provocam uma alteração na conformação da proteína codificada, provocando sua degradação. Certos medicamentos atuam como chaperonas farmacológicas, estabilizando a proteína e aumentando a quantidade de proteína funcional. Exemplos incluem o uso do lumacaftor na fibrose cística [15] e do migalastate na doença de Fabry [16].
Read-through
Uma certa parcela dos pacientes com doenças genéticas possuem mutações sem sentido, que levam a um códon de parada prematuro e à degradação do RNA mensageiro. Certas moléculas pequenas que permitem a tradução do RNA mensageiro através desses códons (read-through). Em maio de 2014, um representante dessa classe de medicamentos, o atalureno, recebeu aprovação condicional pela European Medicines Agency para o tratamento de pacientes com Distrofia muscular de Duchenne com mutações sem sentido.[17]
Outras moléculas pequenas farmacêuticas
Certas doenças genéticas envolvem proteínas que possuem um papel bem conhecido, possibilitando a atuação nas vias envolvidas na patogênese. Exemplos incluem o uso do pamidronato para reduzir a reabsorção óssea na Osteogênese Imperfeita [18], do tafamidis e diflunisal para estabilizar os tetrâmeros de transtirretina na Polineuropatia Amiloidótica familiar. [19]
Medicamentos biológicos e ácidos nucleicos
Reposição enzimática ou de outras proteínas
Certas doenças de depósito lisossômico são tratadas com infusão de uma enzima recombinante (produzida em laboratório) que pode reduzir o acúmulo de compostos em diversos tecidos. Exemplos incluem a doença de Gaucher,[20] a doença de Fabry,[21] as mucopolissacaridoses[22] e a doença de Pompe.[23]. Em outros casos, o tratamento consiste na reposição de proteínas não enzimáticas, como a reposição de fatores de coagulação nas coagulopatias hereditárias[24] e de hormônio de crescimento na deficiência de hormônio de crescimento.[25]
Terapia gênica
A terapia gênica compreende o uso de genes com fins terapêuticos[26] Estudos clínicos com a terapia gênica tiveram início no começo da década de 1990 e a tecnologia vem sendo aperfeiçoada desde então. Em novembro de 2012, o primeiro produto farmacológico para terapia gênica para uma doença monogênica, o alipogene tipavorvec, usado para o tratamento da deficiência de lipoproteína lipase, foi aprovado pela European Medicines Agency [27]. Por razões comerciais, o medicamento foi descontinuado em 2017, após ter sido utilizado comercialmente uma única vez [28]. Atualmente, a terapia gênica é utilizada comercialmente para o tratamento da imunodeficiência severa combinada por deficiência de adenosina deaminase e há diversos outros produtos em fases finais de desenvolvimento [28].
Terapia antisenso
Oligonucleotídios antisenso podem ser utilizados para inibir ou modificar a tradução do RNA mensageiro em certas condições genéticas. Exemplos incluem o uso do eteplirseno na distrofia muscular de Duchenne para "saltar" o éxon 51 do gene DMD, durante o processo de encadeamento do RNA mensageiro, resultando em uma proteína menor, porém funcional (exon skipping)[29] e do nusinerseno na atrofia muscular espinhal para aumentar a produção da proteína SMN de tamanho inteiro a partir do gene SMN2 [30].
RNA interferente
O RNA interferente (RNAi) compreende o uso de conjugados oligonucleotídicos modificados para silenciar o RNA mensageiro através do complexo de silenciamento induzido por RNA (RISC). No final de 2017, um medicamento desse grupo, o patisiran, desenvolvido para o tratamento da polineuropatia amiloidótica familiar, foi submetido para apreciação de agências regulatórias européia e norte-americana [31].
Transplantes
Uma parcela das doenças genéticas decorre da mutação de proteínas que são normalmente produzidas totalmente ou principalmente em órgãos específicos, que podem ser transplantados. Além disso, o transplante de medula óssea é usado para suplementar enzimas e outros produtos gênicos ausentes em determinadas doenças. Exemplos incluem o transplante hepático na polineuropatia amiloidótica familiar [19] e o transplante de medula óssea na Adrenoleucodistrofia ligada ao X e em certas doenças de depósito lisossômico.[32]

Carreira em Genética Médica
A Genética Médica, vista como sinônimo de Genética Clínica, é uma especialidade médica. Para a exercer, é necessário graduar-se em uma escola médica e especializar-se em Genética Médica. No Brasil, esse treinamento leva nove anos, incluindo seis anos de Medicina e três anos de Genética Médica. O termo Medical Genetics é utilizado em sentido mais amplo nos Estados Unidos e outros países, incluindo não só a Genética Clínica (Clinical Genetics), como também a Genética Clínica Bioquímica (Clinical Biochemical Genetics), a Citogenética Clínica (Clinical Cytogenetics) e a Genética Clínica Molecular (Clinical Molecular Genetics).[33] As demais áreas são campos de atuação comuns com outros profissionais de saúde.
Genética Médica no Brasil
A primeira residência em Genética Médica no Brasil foi criada em 1977 no Hospital das Clínicas de Ribeirão Preto da Universidade de São Paulo. O reconhecimento como especialidade médica pelo Conselho Federal de Medicina ocorreu apenas seis anos depois, em 1983, através da resolução Nº 1128/1983.[34] Em 1986, foi fundada a Sociedade Brasileira de Genética Médica - SBGM, a partir da iniciativa dos membros da Sociedade Brasileira de Genética.[35] Em pesquisa da demografia médica em 2015, havia 241 médicos geneticistas, sendo a especialidade médica com menos integrantes.[36]
Conteúdo do Programa de Genética Médica
O conteúdo dos programas de residência médica no Brasil é determinado pela Resolução nº 2, de 17 de maio de 2006.[1] O treinamento proposto para a Genética Médica inclui atividades em ambulatórios de genética e especialidades externas (pediatria incluindo neonatologia, neurologia e/ou endocrinologia e/ou clínica médica e/ou gineco-endócrino), plantões e laboratórios (Citogenética, Genética Bioquímica, Molecular). O conteúdo teórico compreende conhecimentos básicos de Genética e Biologia Molecular, bem como suas aplicações clínicas e técnicas de aconselhamento genético.
Genética Médica no SUS
Apesar de alguns serviços de saúde públicos oferecerem atendimento em Genética Médica, não há uma rede de atenção integrada e de acesso universal nessa área.[37] Essa situação começou a ser solucionada em 2004, com a publicação da portaria Nº 2.380,[38] que instituiu o grupo de trabalho de Genética Clínica, com a finalidade de elaborar a Política Nacional de Atenção à Saúde em Genética Clínica. Tal tarefa foi concluída em 2009, quando foi publicada a portaria Nº 81.[39] Em 2012, entretanto, foi instituído um novo grupo de trabalho para formulação da Política de Atenção às Pessoas com Doenças Raras, com o objetivo de regulamentar a atenção não só aos pacientes com doenças genéticas mas também aos com outras doença raras. As diretrizes assistenciais e as normas para habilitação de hospitais e serviços que farão o atendimento foram publicadas em janeiro de 2014.[40]
Ligações externas
- «Sociedade Brasileira de Genética Médica - SBGM»
- «Lista de Médicos Especialistas em Genética Médica pela SBGM no Brasil, por estado»
- «Sociedade Portuguesa de Genética Humana»
- Colégio da Especialidade de Genética Médica (Portugal)
- «PubMed - Biblioteca de medicina e saúde» (em inglês)
Referências
- ↑ a b «Proposição de Conteúdo dos Programas de Residência Médica». Consultado em 27 de outubro de 2012
- ↑ a b c Kingston, HM. (2001). ABC of clinical genetics. London: BMJ. ISBN 9780727916273
- ↑ «Profiles in Science: The Victor A. McKusick Papers». Consultado em 27 de outubro de 2012
- ↑ «DeCS - Descritores em Ciências da Saúde». Consultado em 27 de outubro de 2012
- ↑ a b Brunoni, Décio (2002). «Aconselhamento Genético». Ciência & Saúde Coletiva. 7 (1): 101-107. ISSN 1413-8123. doi:10.1590/S1413-81232002000100009. Consultado em 27 de outubro de 2012
- ↑ Rickman, L (9 de setembro de 2005). «Prenatal detection of unbalanced chromosomal rearrangements by array CGH». Journal of Medical Genetics. 43 (4): 353-361. ISSN 1468-6244. doi:10.1136/jmg.2005.037648. Consultado em 27 de outubro de 2012
- ↑ Warner, J P; L H Barron; D Goudie; K Kelly; D Dow; D R Fitzpatrick; D J Brock (1 de dezembro de 1996). «A general method for the detection of large CAG repeat expansions by fluorescent PCR.». Journal of Medical Genetics. 33 (12): 1022–1026. ISSN 1468-6244. doi:10.1136/jmg.33.12.1022. Consultado em 9 de novembro de 2014
- ↑ a b Jinnah, H. A.; Albanese, Alberto; Bhatia, Kailash P.; Cardoso, Francisco; Da Prat, Gustavo; de Koning, Tom J.; Espay, Alberto J.; Fung, Victor; Garcia-Ruiz, Pedro J. «Treatable inherited rare movement disorders». Movement Disorders (em inglês): n/a–n/a. ISSN 1531-8257. doi:10.1002/mds.27140
- ↑ Zempleni Janos; Yousef I Hassan; Subhashinee SK Wijeratne (novembro de 2008). «Biotin and biotinidase deficiency». Expert Review of Endocrinology & Metabolism. 3 (6): 715-724. ISSN 1744-6651. doi:10.1586/17446651.3.6.715. Consultado em 27 de outubro de 2012
- ↑ Kaler, Stephen G.; Liew, Clarissa J.; Donsante, Anthony; Hicks, Julia D.; Sato, Susumu; Greenfield, Jacquelyn C. (1 de outubro de 2010). «Molecular correlates of epilepsy in early diagnosed and treated Menkes disease». Journal of Inherited Metabolic Disease (em inglês). 33 (5): 583–589. ISSN 0141-8955. doi:10.1007/s10545-010-9118-2
- ↑ Mistry, Pramod K.; Lukina, Elena; Ben Turkia, Hadhami; Shankar, Suma P.; Baris, Hagit; Ghosn, Marwan; Mehta, Atul; Packman, Seymour; Pastores, Gregory (1 de novembro de 2017). «Outcomes after 18 months of eliglustat therapy in treatment-naïve adults with Gaucher disease type 1: The phase 3 ENGAGE trial». American Journal of Hematology (em inglês). 92 (11): 1170–1176. ISSN 1096-8652. doi:10.1002/ajh.24877
- ↑ Coutinho, Maria Francisca; Santos, Juliana Inês; Alves, Sandra (4 de julho de 2016). «Less Is More: Substrate Reduction Therapy for Lysosomal Storage Disorders». International Journal of Molecular Sciences (em inglês). 17 (7). 1065 páginas. doi:10.3390/ijms17071065
- ↑ Skovby Flemming; Mette Gaustadnes; S. Harvey Mudd (janeiro de 2010). «A revisit to the natural history of homocystinuria due to cystathionine β-synthase deficiency». Molecular Genetics and Metabolism. 99 (1): 1-3. ISSN 1096-7192. doi:10.1016/j.ymgme.2009.09.009. Consultado em 27 de outubro de 2012
- ↑ De Boeck Kris; Anne Munck; Seth Walker; Albert Faro; Peter Hiatt; Geoffrey Gilmartin; Mark Higgins (26 de setembro de 2014). «Efficacy and safety of ivacaftor in patients with cystic fibrosis and a non-G551D gating mutation». Journal of Cystic Fibrosis: Official Journal of the European Cystic Fibrosis Society. ISSN 1873-5010. PMID 25266159. doi:10.1016/j.jcf.2014.09.005
- ↑ Cutting, Garry R. (5 de dezembro de 2017). «Treating Specific Variants Causing Cystic Fibrosis». JAMA. 318 (21): 2130–2131. ISSN 0098-7484. doi:10.1001/jama.2017.16823
- ↑ Germain, Dominique P.; Hughes, Derralynn A.; Nicholls, Kathleen; Bichet, Daniel G.; Giugliani, Roberto; Wilcox, William R.; Feliciani, Claudio; Shankar, Suma P.; Ezgu, Fatih (10 de agosto de 2016). «Treatment of Fabry's Disease with the Pharmacologic Chaperone Migalastat». New England Journal of Medicine (em inglês). 375 (6): 545–555. doi:10.1056/nejmoa1510198
- ↑ European Medicines Agency (23 de maio de 2014). «European Medicines Agency recommends first-in-class medicine for treatment of Duchenne muscular dystrophy» (PDF)
- ↑ Brasil. «PORTARIA Nº 1.306, DE 22 DE NOVEMBRO DE 2013». Diário Oficial da União 228 ed. Brasília. pp. 58–60
- ↑ a b Ueda, Mitsuharu; Yukio, Ando (2014). «Recent advances in transthyretin amyloidosis therapy». Translational Neurodegeneration. 3. 19 páginas. ISSN 2047-9158. PMC 4165622
 . PMID 25228988. doi:10.1186/2047-9158-3-19
. PMID 25228988. doi:10.1186/2047-9158-3-19
- ↑ Martins Ana M.; Clarisse L. Lobo; Elisa A. P. Sobreira; Eugenia R. Valadares; Gilda Porta; José Semionato Filho; Mara A. D. Pianovsky; Marcelo S. Kerstenetzky; Maria F. P. Montoril; Paulo C. Aranda; Ricardo F. Pires; Ronald M. V. Mota; Teresa C. Bortolheiro; Maria T. M. Paula (junho de 2003). «Tratamento da doença de Gaucher: um consenso brasileiro». Revista Brasileira de Hematologia e Hemoterapia. 25 (2). ISSN 1516-8484. doi:10.1590/S1516-84842003000200004. Consultado em 27 de outubro de 2012
- ↑ Schiffmann, R. (6 de junho de 2001). «Enzyme Replacement Therapy in Fabry Disease: A Randomized Controlled Trial». JAMA: The Journal of the American Medical Association. 285 (21): 2743-2749. ISSN 0098-7484. doi:10.1001/jama.285.21.2743. Consultado em 27 de outubro de 2012
- ↑ Giugliani Roberto et al. (2010). «Terapia de reposição enzimática para as mucopolissacaridoses I, II e VI: recomendações de um grupo de especialistas brasileiros». Revista da Associação Médica Brasileira. 56 (3): 271-277. ISSN 0104-4230. doi:10.1590/S0104-42302010000300009. Consultado em 27 de outubro de 2012
- ↑ van der Beek; M L C Hagemans; A T van der Ploeg; A J J Reuser; P A van Doorn (junho de 2006). «Pompe disease (glycogen storage disease type II): clinical features and enzyme replacement therapy». Acta neurologica Belgica. 106 (2): 82-8. ISSN 0300-9009. Consultado em 27 de outubro de 2012
- ↑ MINISTÉRIO DA SAÚDE (2002). Manual de tratamento das Coagulopatias Hereditárias. [S.l.: s.n.] ISBN 85-334-0993-1
- ↑ Hardin, DS (2008). «Treatment of short stature and growth hormone deficiency in children with somatotropin (rDNA origin)». Biologics
- ↑ Wang, Dan; Guangping, Gao (setembro de 2014). «State-of-the-art human gene therapy: part II. Gene therapy strategies and clinical applications». Discovery Medicine. 18 (98): 151–161. ISSN 1944-7930. PMID 25227756
- ↑ «Gene therapy: Glybera approved by European Commission». Consultado em 27 de janeiro de 2013
- ↑ a b Senior, Melanie (7 de junho de 2017). «After Glybera's withdrawal, what's next for gene therapy?». Nature Biotechnology (em inglês). 35 (6): 491–492. doi:10.1038/nbt0617-491
- ↑ Lim, Kenji Rowel; Maruyama, Rika; Yokota, Toshifumi (28 de fevereiro de 2017). «Eteplirsen in the treatment of Duchenne muscular dystrophy». Drug Design, Development and Therapy (em English). Volume11: 533–545. doi:10.2147/dddt.s97635
- ↑ Finkel, Richard S.; Mercuri, Eugenio; Darras, Basil T.; Connolly, Anne M.; Kuntz, Nancy L.; Kirschner, Janbernd; Chiriboga, Claudia A.; Saito, Kayoko; Servais, Laurent (1 de novembro de 2017). «Nusinersen versus Sham Control in Infantile-Onset Spinal Muscular Atrophy». New England Journal of Medicine (em inglês). 377 (18): 1723–1732. doi:10.1056/nejmoa1702752
- ↑ House, SA Editor Douglas W. (18 de dezembro de 2017). «Alnylam files European marketing application for patisiran in hATTR amyloidosis». Seeking Alpha (em inglês)
- ↑ Lange Marcos C.; Hélio A.G. Teive; André R. Troiano; Marco Bitencourt; Vaneuza A.M. Funke; Daniela C. Setúbal; José Zanis Neto; Carlos R. Medeiros; Lineu C. Werneck; Ricardo Pasquini; Carmen M.S. Bonfim (março de 2006). «Bone marrow transplantation in patients with storage diseases: a developing country experience». Arquivos de Neuro-Psiquiatria. 64 (1): 1–4. ISSN 0004-282X. doi:10.1590/S0004-282X2006000100001. Consultado em 8 de novembro de 2014
- ↑ «Specialties of Genetics». ABMG. Consultado em 27 de outubro de 2012
- ↑ «Resolução CFM Nº 1128/1983». Consultado em 27 de outubro de 2012
- ↑ «Histórico da Sociedade Brasileira de Genética Médica». Consultado em 27 de outubro de 2012
- ↑ Scheffer, M (2015). Demografia Médica no Brasil 2015. São Paulo: Conselho Regional de Medicina do Estado de São Paulo e Conselho Federal de Medicina. 283 páginas
- ↑ Novoa, Maria Concepción; Burnham, Teresinha Fróes (janeiro de 2011). «Desafios para a universalização da genética clínica: o caso brasileiro». Revista Panamericana de Salud Pública. 29 (1): 61-68. ISSN 1020-4989. doi:10.1590/S1020-49892011000100010. Consultado em 27 de outubro de 2012
- ↑ «PORTARIA Nº 2380/GM». Consultado em 27 de outubro de 2012
- ↑ «PORTARIA Nº 81 DE 20 DE JANEIRO DE 2009». Consultado em 27 de outubro de 2012
- ↑ Brasil. «PORTARIA Nº 199, DE 30 DE JANEIRO DE 2014». Diário Oficial da União 30 ed. Brasília. pp. 44–54
