Nitrato de sódio
| Nitrato de sódio Alerta sobre risco à saúde | |
|---|---|
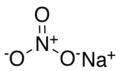
|

|
| Nome IUPAC | Sodium nitrate |
| Outros nomes | caliche; nitrato de soda; salitre do Chile; saltpeter; soda niter; nitratine |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número RTECS | WC5600000 |
| Propriedades | |
| Fórmula molecular | NaNO3 |
| Massa molar | 84.9947 g/mol |
| Aparência | Pó branco ou cristais incolores |
| Densidade | 2,26 g·cm–3 (20 °C) [1] |
| Ponto de fusão |
306–307 °C[1] |
| Ponto de ebulição |
decompõe-se a 380 °C[1] |
| Solubilidade em água | levemente solúvel: 874 g·l-1 (20 °C)[1] |
| Solubilidade | bastante solúvel em amônia; solúvel em álcool |
| Índice de refracção (nD) | 1.587 (trigonal) 1.336 (rhomobohedral) |
| Estrutura | |
| Estrutura cristalina | trigonal and rhombohedral |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
-468 kJ/mol |
| Entropia molar padrão S |
117 J/mol.K |
| Farmacologia | |
| Riscos associados | |
| MSDS | ICSC 0185 |
| Índice UE | Not listed |
| Principais riscos associados |
Oxidant, irritant |
| NFPA 704 | |
| Frases R | R8 R22 |
| Frases S | S22 S41 |
| Ponto de fulgor | Non-flammable |
| LD50 | 1267 mg·kg-1 (rato, oral)[2] |
| Compostos relacionados | |
| Outros aniões/ânions | Nitrito de sódio Sulfato de sódio Cloreto de sódio |
| Outros catiões/cátions | Nitrato de lítio Nitrato de potássio Nitrato de rubídio Nitrato de césio Nitrato de magnésio |
| Compostos relacionados | Ácido nítrico |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O nitrato de sódio é um composto químico de fórmula NaNO3, cristalino inodoro e incolor. Tem semelhança com o nitrato de potássio, inclusive no comportamento químico. Solúvel em água, álcool e amônia líquida.
Algumas aplicações: fabricação de nitrato de potássio, fertilizantes, explosivos. Também usado em algumas carnes enlatadas para preservar a cor.
Encontrado na natureza, sendo esta sua principal fonte comercial. Os maiores depósitos naturais estão no Chile, Peru, Argentina e Bolívia. Por isso, também chamado salitre do Chile.
Suspeito de provocar desequilíbrio osmótico, que leva à secura bucal e sede insaciável, além de sonolência e déficit de atenção, porém de baixa toxicidade e aumento de rendimento na produção de alimentos devido ao poder de conservação e baixo custo de produção.
Ver também[editar | editar código-fonte]
Referências
- ↑ a b c d Registo de Natriumnitrat na Base de Dados de Substâncias GESTIS do IFA.
- ↑ Catálogo da Merck Nitrato de sódio acessado em 19 de janeiro de 2011

