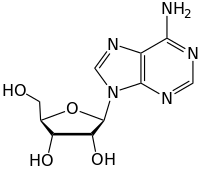
Adenosina
| Adenosina Alerta sobre risco à saúde | |
|---|---|
| |

| |
| Outros nomes | *(2R,3R,4R,5R)-2-(6-Aminopurin-9-yl)- 5-(hydroxymethyl)oxolan-3,4-diol *Ado *6-Aminopurin-9β-D-ribofuranosid |
| Identificadores | |
| Número CAS | |
| PubChem | |
| DrugBank | APRD00132 |
| ChemSpider | |
| Código ATC | C01 |
| SMILES |
|
| Propriedades | |
| Fórmula química | C10H13N5O4 |
| Massa molar | 267.22 g mol-1 |
| Densidade | 0,31 g·cm−3 [1] |
| Ponto de fusão |
234–237 °C [1] |
| Solubilidade em água | pouco solúvel em água [1] e etanol |
| Solubilidade | *gut löslich in heißem Wasser [2] |
| Farmacologia | |
| Biodisponibilidade | Rapidly cleared from circulation via cellular uptake |
| Via(s) de administração | IV or injection |
| Metabolismo | Rapidly converted to inosine and adenosine monophosphate |
| Meia-vida biológica | cleared plasma <30 seconds - half life <10 seconds |
| Ligação plasmática | No |
| Excreção | can leave cell intact or can be degraded to hypoxanthine, xanthine, and ultimately uric acid |
| Classificação legal | ? (AU) |
| Riscos na gravidez e lactação |
C |
| Riscos associados | |
| Frases R | - |
| Frases S | - |
| LD50 | >20 g·kg−1(Camundongo, oral) [1] |
| Compostos relacionados | |
| Compostos relacionados | Adenina Desoxiadenosina Adenosina monofosfato |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
A adenosina é um nucleosídeo, formado pela união de uma adenina e uma ribose. É uma purina endógena sintetizada da degradação de aminoácidos como metionina, treonina, valina e isoleucina assim como AMP.[3]
Função energética[editar | editar código-fonte]
A adenosina desempenha um papel importante na bioquímica, tais como transferência de energia, sob a forma de adenosina tri-fosfato (ATP) e adenosina difosfato (ADP) armazenando energia potencial essencial para o metabolismo energético dos animais.
Função de sinalização[editar | editar código-fonte]
Sob a forma de adenosina monofosfato cíclico (AMPc), colabora em vias de sinalização intracelular.
Função no Sistema Nervoso Central (SNC)[editar | editar código-fonte]
No SNC a adenosina atua[4]:
- Inibindo pré e pós-sináptica (PIPS)
- Reduzindo a atividade motora
- Diminuindo a frequência respiratória
- Induzindo ao sono
- Aliviando a ansiedade.
Função periférica[editar | editar código-fonte]
Os principais efeitos da adenosina fora do SNC incluem[4]:
- Vasodilatação,
- Broncoconstrição,
- Imunossupressão,
- Inibição da agregação plaquetária,
- Diminuição da frequência cardíaca,
- Estimulação de vias aferentes nociceptivas,
- Inibição da libertação de neurotransmissores e,
- Inibição da libertação de factores e hormônios.
Informação Farmacêutica[editar | editar código-fonte]
É utilizada por via endovenosa para reversão de taquicardia supraventricular paroxística ao bloquear o a transmissão via nó atrioventricular. Administrado por via intravenosa deprime a atividade do nó sinusal e é utilizado para re-estabelecer o ritmo sinusal.
A adenosina também atua como um neuroprotector ao inibir a transmissão excitatória do receptor A1 e estimular uma corrente de saída de K+ (potássio) sensível a acetilcolina no átrio e nódulos sinusal e atrioventricular. Isso resulta em redução do potencial de ação, hiperpolarização e automaticidade mais lenta.
É rapidamente captada por eritrócitos e células endoteliais, sendo sua semi-vida de menos de 10s, por isso deve ser administrado como bolo intravenoso rápido (cerca de 6 mg em 2s), usando um catéter venoso central. Caso não seja suficiente, se administra o dobro, 12 mg em 2s, pela mesma via.
A cafeína é a principal substância que antagoniza os efeitos da adenosina no organismo.
Contra-indicações[editar | editar código-fonte]
Contra-indicado em caso de Asma.
Referências
- ↑ a b c d Herstellerangaben der Firma Roth.
- ↑ a b Wissenschaft-Online-Lexika: Eintrag zu Adenosin im Lexikon der Chemie. Abgerufen am 7. Januar 2010
- ↑ «Cópia arquivada». Consultado em 9 de outubro de 2011. Arquivado do original em 9 de outubro de 2011
- ↑ a b http://www.ebi.ac.uk/interpro/entry/IPR001068;jsessionid=D65E37AC7986A2B6184B83203D921DA8
