Gliceraldeído
| Gliceraldeído Alerta sobre risco à saúde | |
|---|---|

| |

| |

| |
| Nome IUPAC | 2,3-diidroxipropanal |
| Outros nomes | aldeído glicérico, gliceral |
| Identificadores | |
| Número CAS | , 56-82-6 [DL-(±)-gliceraldeído] 453-17-8 [D-(+)-gliceraldeído] |
| PubChem | |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C3H6O3 |
| Massa molar | 90.08 g/mol |
| Densidade | 1,46 g·cm−3 (formas D eL)[1] |
| Ponto de fusão |
145 °C[2] |
| Ponto de ebulição |
140–150 °C (a 1,1 hPa)[2] |
| Solubilidade em água | * 30 g·l−1 a 18 °C[2] |
| Solubilidade | solúvel em etanol, praticamente insolúvel em éter dietílico[1] |
| Compostos relacionados | |
| Aldoses relacionados | Eritrose e Treose ((CH2O)4) |
| Compostos relacionados | Glicolaldeído 1,3-Diidroxi-2-propanona (cetose) Glicerol (propano-1,2,3-triol) Ácido glicérico (2,3-diidroxipropanoico) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Gliceraldeído (2,3-diidroxipropanal) é um monossacarídeo do tipo triose, de fórmula química C3H6O3. É a mais simples das aldoses, já que o glicolaldeído e o metanal, cujas fórmulas químicas são, respectivamente, C2H4O2 e CH2O, não são considerados aldoses. Os demais monossacarídeos maiores do tipo aldose derivam do gliceraldeído por alongamento da cadeia carbônica, sendo comum nas células animais e vegetais como ésteres fosfóricos.
O gliceraldeído é um composto orgânico sólido, cristalino e de sabor adocicado. É um intermediário no metabolismo dos carboidratos.
Isomeria[editar | editar código-fonte]
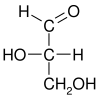
Analisando a estrutura do gliceraldeído pela projeção de Fisher, pode-se constatar a existência de duas configurações, dependendo da posição da hidroxila do carbono assimétrico ou quiral, isto é, o carbono ligado a quatro átomos ou radicais diferentes entre si. No caso do gliceraldeído, o carbono assimétrico é o de número 2 (os átomos de carbono são numerados a partir da extremidade mais próxima do grupo carbonila). Na configuração L-gliceraldeído, a hidroxila encontra-se à esquerda do carbono quiral, enquanto que, no D-gliceraldeído, a hidroxila está localizada à direita.
| D-gliceraldeído | L-gliceraldeído | |
| Projeção de Fisher | 
|
|
| Fórmula esquelética | 
|

|
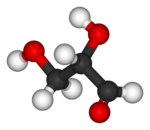
| Modelo bola e bastão | 
|
|
Referências
- ↑ a b Thieme Chemistry, ed. (2009). RÖMPP Online - Version 3.5. Stuttgart: Georg Thieme Verlag KG
- ↑ a b c The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 774, ISBN 978-0-911910-00-1.
